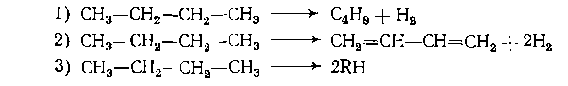|
|
ПАРЦИАЛЬНЫЕ МОЛЯРНЫЕ БАЛАНСЫ
Кроме мольных количеств и потоков в химии и технологии большое значение имеют безразмерные характеристики материального баланса — степень конверсии, селективность и выход. Степень конверсии — доля прореагировавшего исходного реагента относительно его начального количества:
В таком написании степень конверсии может меняться от 0 до 1, но ее нередко выражают в процентах, умножая правые части , предыдущих выражений на 100. При этом обычно степень конверсии определяют по основному исходному реагенту А, но ее можно аналогично записать и для других реагентов [например,
Для простых и обратимых реакций, когда имеются единственное независимое превращение и одно ключевое вещество, степень конверсии — вполне достаточная характеристика мате рассчитать FAпо уравнению (0-7), п (F) по формуле (0-3) и затем все ni (Fi) по уравнению (0-4). Кроме того, для любой простой или обратимой реакции
в дополнение к соотношению (0-7) легко вывести зависимость ni(Fi)от nА,о (FА,о) и степени конверсии основного реагента ХA:
Для сложных реакций, имеющих более одного ключевого вещества, степень конверсии показывает лишь долю превращенного реагента, но не дает представления о направлениях его превращения, которое определяется селективностью и выходом. Селективность — доля (или процент) превращенного исходного реагента, израсходованная на образование данного продукта. При этом всегда учитывают только химические превращения в реакторе, исключая какие-либо иные потери веществ (кроме их расходования на образование побочных продуктов). Другими словами, селективность можно определить как отношение количества полученного продукта к его теоретическому количеству, которое могло бы образоваться из превращенного реагента при отсутствии побочных реакций и потерь. Теоретическое количество легко рассчитать по суммарной реакции образования данного продукта из исходных реагентов, применяя к ней уравнения (0-3):
в котором двойной индекс при Ф означает, что селективность определена для продукта iпо основному реагенту А. Ее можно аналогичным образом выразить и по другому реагенту. Когда исходное вещество является единственным или известно, по какому из реагентов определяется селективность, индекс А (или Y) может быть опущен. В уравнении (0-9) член
соответствует количеству исходного реагента, израсходованному на образование данного ключевого вещества. Очевидно, что сумма их для всех ключевых веществ будет равна Fa,oXa,откуда вытекает соотношение: Селективность по целевому продукту показывает долю полезно использованного сырья; она является важной характеристикой катализаторов, условий проведения процесса и типа реакторов. На практике селективность по целевому продукту изменяется от 50—60 до 100%, причем повышение селективности— одна из важнейших задач химической технологии. Выход — это далеко не однозначное понятие. Иногда под ним понимают абсолютное количество полученного продукта (в г, кг, моль и кмоль), но чаще выход выражают в долях единицы или в процентах на взятое сырье. Кроме того, выход применяют для характеристики систем разного масштаба — только реакционного аппарата (химический выход), какого-либо узла производства или технологической схемы в целом, когда учитывают не только расход сырья на химические реакции, но и различные потери (технологический выход). Далее мы будем применять понятие только химического выхода. Химический выход равен мольному количеству полученного продукта i,отнесенному к его теоретическому количеству. Следовательно, выражение для выхода легко получить из формулы (0-9) приХа.=1:
Выход можно рассчитывать и по второму реагенту (XiY), причем в литературе встречаются и другие обозначения выхода (Xi,если реагент является единственным или определенно известно, по какому реагенту рассчитывается выход, а также х, у, zит.д). Из формул (0-9) и (0-11) вытекает, что выход равен произведению селективности на степень конверсии:
При этом сумма выходов ключевых веществ по основному реагенту А с учетом уравнения (0-10) равна степени конверсии этого реагента: Последние уравнения широко используют в химической кинетике и при расчете реакторов. Очевидно, что при расчете материальных балансов процесса все или часть исходных данных (за исключением пi,о или Fi,о) может быть задана безразмерными характеристиками — степенью конверсии, селективностью или выходом. Тогда, используя выведенные уравнения, легко рассчитывают мольные количества или потоки всех веществ и составляют таблицу материального баланса.
Парциальные молярные балансы. На безразмерных характеристиках.реакций основаны расчеты так называемых парциальных молярных балансов, составляемых на 1 моль основного исходного реагента А. При этом начальный состав смеси также выражают через безразмерные величины, а именно мольные соотношения других веществ, в том числе инертных, к основному реагенту А:
полноты или частная степень конверсии основного реагента по данной суммарной реакции и обозначается как Xj,изменяющаяся от 0 до 1. Если какое-либо ключевое вещество образуется только по этой реакции, то имеем Кроме мольных- количеств или потоков веществ и безразмерных характеристик баланса важное значение имеют концентрации, парциальные давления и мольные доли, на которых основаны расчеты термодинамики и кинетики реакций, а также химических реакторов. Концентрация соответственно для периодических и непрерывных процессов определяется как отношение мольного количества (мольного потока) вещества к объему V (к объемному потоку W), в котором равномерно распределено данное вещество:
При этом объем (в л или м3) и объемный поток (в л или м3 в секунду, минуту или час) особенно для газофазных реакций необходимо привести к давлению и температуре в реакторе, учитывая объем всех компонентов системы, в том числе разбавителей. Нередко объем или объемный поток остаются постоянными во время реакции. Это типично для жидкофазных процессов, а для газофазных встречается в тех случаях, когда реакция про- текает при постоянных общем давлении и температуре без изменения числа молей веществ или без промежуточного разбавления .смеси. Для таких процессов справедливы концентрационные формы всех выведенных ранее уравнений баланса и формул для расчета безразмерных характеристик реакций, т. е. в эти уравнения можно вместо ni (Fi) подставлять Сi. Для идеальных газов их концентрации пропорциональны. парциальным давлениям (Pi = CiRT), и, следовательно, те же- уравнения подходят и для парциальных давлений веществ. При этом последние являются более удобной характеристикой состояния газа, та|к как при постоянном общем давлении они, в- отличие от концентраций, не зависят от температуры. Более сложные соотношения существуют для реакций, протекающих с изменением объема. При жидкофазных процессах это бывает при поглощении какого-либо газа жидкостью или' при разложении жидкого вещества с образованием летучих продуктов. Тогда объем жидкой фазы в любой момент реакции; находят с помощью коэффициента изменения объема в по уравнению
где Vо и V — начальный и текущий объемы, az— некоторая функция, от которой зависит изменение объема (например, степень конверсии или число присоединившихся молей газа). При этом коэффициент изменения объема определяется выражением
и является положительным при увеличении объема смеси во< время реакции и отрицательным при его уменьшении. Тогда текущая концентрация вещества равна: Для газофазных процессов изменение объема обычно происходит из-за неравенства числа молей веществ во время реакции (разложение, присоединение и др.). Его -можно учитывать с помощью введенных выше коэффициентов изменения объема,
Например, для реакции А—>B+Z в отсутствие разбавителей имеем е= (2-1) : 1 =+1, а для превращения А+Y—>В при эквимольном соотношении реагентов и в отсутствие разбавителей е=(1—2): 2 = —0,5. Для первой реакции при мольном соотношении инертного разбавителя в0 получим:
Для второй реакции при мольном избытке второго реагентаBY имеем:
Последние уравнения справедливы приТ=const. Из-за пропорциональности концентраций парциальным давлениям можно записать соотношения, не зависящие от температуры:
где Pобщ — общее давление смеси, которое для большинства процессов можно считать постоянным.
■Составьте стехиометрическую матрицу, найти число независимых реакций, выберите независимые реакции и ключевые вещества. 4.Для предыдущей реакции провести материальный расчет для условий: начальный мольный поток этилена равен 150 кмоль/ч, степень его конверсии 0,40, селективность образования этнленоксида 0,70, мольное соотношение кислорода и этилена Bу=0,60. Составьте таблицу материального баланса. 5.Для реакции из иримера 3 составьте общие уравнения зависимости мольных потоков веществ от начального мольного потока этилена, By, выходовэтнленоксида и диоксида углерода. 6.Какое уравнение связывает между собой степень конверсии, селективность и выход продукта? 7.Составьте парциальный молярный баланс для нростой реакции из нри- мера '1. Выведите уравнения парциальных давлений компонентов смеси в зависимости от начальпого давления бензола и общего давления, если известно, что реакция проводится в газовой фазе без посторонних разбавителей и при начальном мольном отношении Н2: CbH5^Py. 8.При дегидрировании н-бутана протекают следующие суммарные реакции
где RH— молекулы СН4 и СЭН6 или С2Н6 н С2Н4. Составьте парциальный молярный баланс процесса и выразите парциальные давления всех веществ через выходы бутеиа, бутадиена и низших углеводородов, если реакция протекает без посторонних разбавителей. Рассчитайте парциальные давления, если Робщ = 0,02 МПа, xс4н8 = 0,30; xC4H8 = 0,14, а селективность процесса по смеси-С4Н8 и С4Н6 составляет 0,90. ГЛАВА I 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
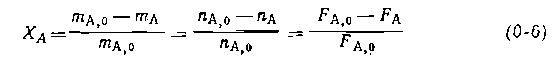


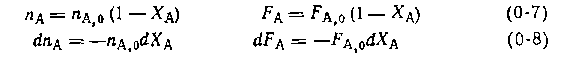
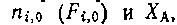



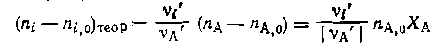
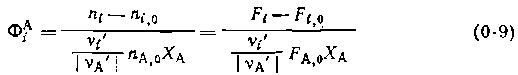
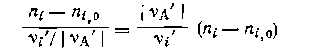




 Рассчитаем выходы и проверим полученные соотношения для примера дегидратации этанола:
Рассчитаем выходы и проверим полученные соотношения для примера дегидратации этанола:




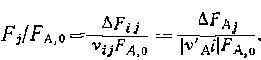


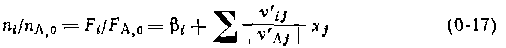

 КОНЦЕНТРАЦИИ, ПАРЦИАЛЬНЫЕ ДАВЛЕНИЯ И МОЛЬНЫЕ ДОЛИ
КОНЦЕНТРАЦИИ, ПАРЦИАЛЬНЫЕ ДАВЛЕНИЯ И МОЛЬНЫЕ ДОЛИ



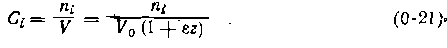
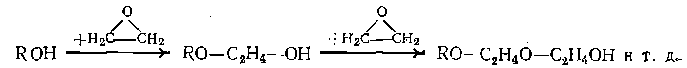



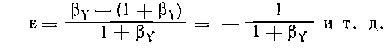

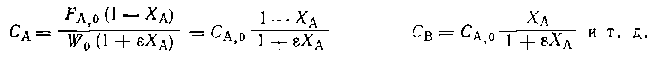

 где — мольное соотношение инертных разбавителей и основного реагента А в исходной смеси. После этого парциальные давления вычисляют по формуле
где — мольное соотношение инертных разбавителей и основного реагента А в исходной смеси. После этого парциальные давления вычисляют по формуле


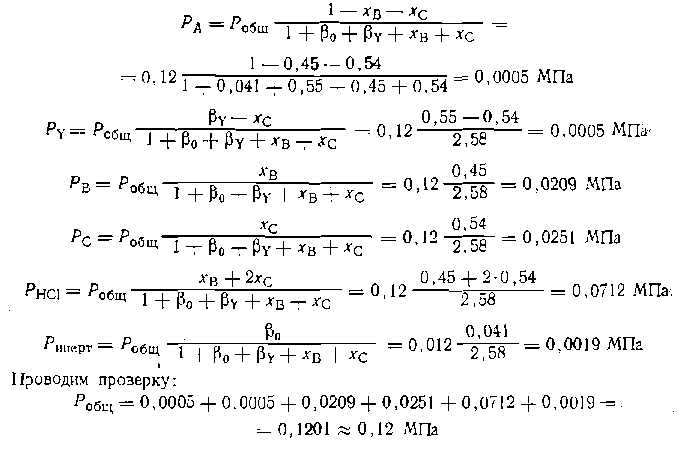 Вопросы а упражнения
Вопросы а упражнения