|
|
Методы получения бензола и его гомологов1. Сухая перегонка каменного угля (~ 1000 °С, без доступа воздуха). 2. Каталитический риформинг (каталитическая ароматизация, то есть повышение содержания аренов в результате прохождения реакций образования ароматических углеводородов) нефтяных фракций. 3. Тримеризация ацетилена (реакция академика Зелинского). 3С2Н2 4. Ароматизация углеводородов. 4.1. Предельных циклических.
4.3. Непредельных алифатических
Получение гомологов бензола 1.1. Дегидрирование.
1.2. По реакции Вюрца.
1.3. По реакции Фриделя-Крафтса
Физические свойства аренов Это обычно жидкости или твердые вещества с характерным запахом, практически нерастворимые в воде, и плотностью равной ~ 0,87 г/см3. Увеличение в молекуле на одну СН2-группу повышает Ткип ~ 30 °С. Таблица 13 Некоторые физические свойства бензола и ряда его производных
Химические свойства Для бензола характерны реакции присоединения и замещения. 1. Реакции присоединения. 1.1. Гидрирование.
2. Реакции окисления. 2.1. Кислородом воздуха.
2.2. Озоном О3. С6Н6 + 2О3 диальдегид
2.3. Мягкое окисление.
3. Горение. 2С6Н6 + 15О2 ® 12СО2 + 6Н2О
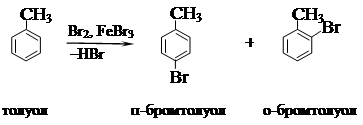
4 а. Галогенирование.
4 б. Сульфирование.
4 в. Нитрование.
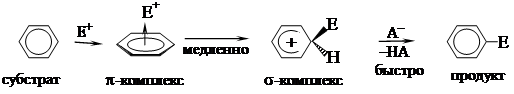
Механизм реакций электрофильного замещения в ароматическом ряду.Для соединений ароматического характера, имеющих замкнутую p -электронную систему, наиболее характерны реакции с электрофильными агентами. С помощью кинетических методов показано, что большинство реакций электрофильного замещения в ароматическом ряду протекает по двухстадийному механизму. На первой, медленной, стадии происходит нарушение ароматической системы и переход атакуемого атома углерода ядра в состояние sp3-гибридизации. Вторая, быстрая, стадия сопровождается восстановлением ароматической структуры и вследствие выигрыша энергии протекает легко и быстро. На первой стадии обычно образуется промежуточный p-комплекс.
p -Комплексы не являются истинными химическими, а представляют собой координационные соединения, в которых донором являются ароматические молекулы, имеющие легко поляризуемые К реакциям электрофильного замещения относятся реакции:
Заместители в кольце делятся на ориентанты I рода и II рода. Ориентанты I рода: алкильные радикалы, группы –ОН, –OR, –NH2, –NHR, –NR2, –SH, атомы галогенов направляют второй заместитель в орто- и пара-положения.
Все заместители I рода, кроме галогенов, обладают электронодонорными свойствами по отношению к бензольному кольцу и ускоряют реакции электрофильного замещения по сравнению с незамещённым бензолом. Ориентанты II рода: карбонильные и сложноэфирные группы, группы –СООН, –SO3H, –NO2, –CºN направляют второй заместитель в мета-положение.
Все заместители II рода обладают электроноакцепторными свойствами по отношению к бензольному кольцу и замедляют реакции электрофильного замещения по сравнению с незамещённым бензолом. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 С6Н6
С6Н6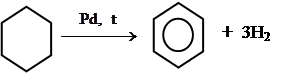
 4.2. Предельных алифатических.
4.2. Предельных алифатических.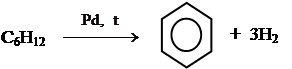




 1.2. Галогенирование (галоидирование).
1.2. Галогенирование (галоидирование).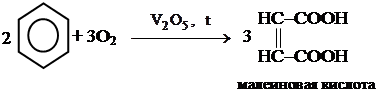
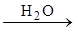 3НОС-СОН
3НОС-СОН

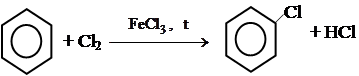 4. Реакции электрофильного замещения.
4. Реакции электрофильного замещения.