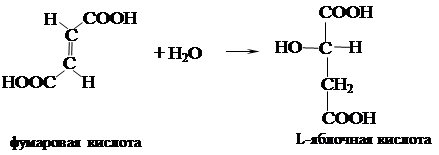|
|
Направление и селективность химической реакцииНаправление химической реакции определяется совокупностью многих факторов. 1) Статические факторы. Реакционная способность соединений существенно зависит от распределения в их молекулах частичных электрических зарядов, которые, в свою очередь, определяются электронными эффектами заместителей и наличием сопряженных и ароматических фрагментов. Характерная для большинства соединений неравномерность в распределении электронной плотности является причиной появления в молекулах реакционных центров, предопределяющих направление атаки тем или иным реагентом (электронный фактор). Рассмотрим в качестве примера реакцию щелочного гидролиза, протекающую по механизму нуклеофильного замещения: СН3СН2СН2Cl + NaОН ® СН3СН2СН2ОН + NaCl 1-хлорпропан гидроксид натрия 1-пропанол хлорид натрия
Атом галогена в 1-хлорпропане, будучи более электроотрицательным, оттягивает на себя электронную пару, обслуживающую связь хлор – углерод. Вследствие этого на атоме галогена появляется частичный отрицательный заряд, а на атоме углерода – положительный. Поэтому нуклеофильная частица ОН– атакует именно тот атом углерода, который связан с атомом галогена. Пространственное строение молекулы определяет пространственный (стерический) фактор, при наличии которого из-за относительно большого пространственного объема заместителей, окружающих реакционный центр, к нему может быть затруднен подход атакующей частицы. При этом реакция либо не будет осуществляться совсем, либо будет идти по иному пути с участием другого, более доступного реакционного центра, если, конечно, он имеется в молекуле. Например, при сульфировании и сульфохлорировании алканов атомы водорода у третичного атома углерода не замещаются, реакция протекает по вторичному или первичному атомам. 2) Динамические факторы. Многостадийные процессы обычно включают стадии промежуточного образования нестабильных интермедиатов, обладающих высокой реакционной способностью. Часто можно предположить образование не одного, а нескольких интермедиатов. Реакция предпочтительно будет проходить через стадию образования относительно более устойчивого интермедиата. Относительная устойчивость интермедиатов, в частности, часто выступающих в качестве высокореакционных промежуточных частиц карбокатионов, карбанионов и свободных радикалов, определяется возможностью делокализации в этих частицах дробного электрического заряда. Так, например, галогенирование алканов протекает, преимущественно по третичному атому углерода. Одной из причин этого является большая устойчивость образующегося интермедиата – третичного радикала.
Региоселективность – предпочтительное протекание реакции по одному из нескольких реакционных центров молекулы. Например, при взаимодействии пропана с бромом есть два различных реакционных центра: вторичный и первичный атомы углерода. При УФ-облучении в реакции преимущественно участвует один реакционный центр – связь С–Н вторичного атома углерода. СН3 – СН2 – СН3 + Вr2 пропан 2-бромпропан
Второй возможный изомер, 1-бромпропан, в этом процессе практически не образуется. Хемоселективность – предпочтительное протекание реакции по одной из родственных функциональных групп.
Стереоселективность – предпочтительное образование в реакции одного из нескольких возможных стереоизомеров. Например, при катализируемом ферментом присоединении воды к фумаровой (транс-бутендиовой) кислоте в организме образуется только один из двух возможных здесь L- и D- стереоизомеров – L-яблочная кислота:
На способность соединений вступать в реакции также оказывают влияние индуктивный и мезомерный эффекты заместителей. Контрольные вопросы 1. Скорость этерификации для первичных спиртов выше, чем для третичных. Влиянием какого фактора это объясняется? 2. При взаимодействии 1-бутена с бромоводородом получается, преимущественно, 2-бромбутан, а не 1-бромбутан. следует считать эту реакцию регио- или хемоселективной? 3. Какие электронные эффекты проявляет нитрогруппа в п-нитротолуоле и нитроэтане? А гидроксильная группа в этаноле и феноле? 4. Атом углерода в хлорметане обладает частичным положительным зарядом. Какой электронный эффект галогена является причиной этого заряда? 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 3) Селективность реакций. Во многих случаях в органическом соединении присутствуют несколько неравноценных реакционных центров. Следовательно, реакция может протекать с образованием продуктов различного строения. В зависимости от строения продуктов реакции говорят о региоселективности, хемоселективности и стереоселективности реакции.
3) Селективность реакций. Во многих случаях в органическом соединении присутствуют несколько неравноценных реакционных центров. Следовательно, реакция может протекать с образованием продуктов различного строения. В зависимости от строения продуктов реакции говорят о региоселективности, хемоселективности и стереоселективности реакции. СН3 – СНВr – СН3 + НВr
СН3 – СНВr – СН3 + НВr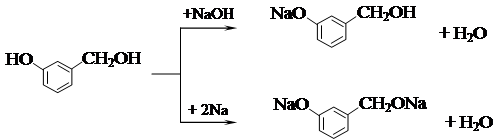 Например, из двух нижеприведенных реакций с участием п-гидроксибензилового спирта только взаимодействие его с гидроксидом натрия относится к хемоселективным процессам. Гидроксид натрия является более слабым основанием, чем металлический натрий, поэтому преимущественно реагирует с гидроксильной группой, обладающей более высокой кислотностью.
Например, из двух нижеприведенных реакций с участием п-гидроксибензилового спирта только взаимодействие его с гидроксидом натрия относится к хемоселективным процессам. Гидроксид натрия является более слабым основанием, чем металлический натрий, поэтому преимущественно реагирует с гидроксильной группой, обладающей более высокой кислотностью.