|
|
Получение бромфенолов и их производных – антипиренов
Несмотря на успехи, достигнутые в создании трудносгораемых пластиков, проблема пожароопасности полимерных материалов остается актуальной. Удель-ный вес галогенсодержащих соединений в общем объеме потребляемых в мире антипиренов довольно высок и непрерывно возрастает. Около трети производимо-го брома используется для производства огнестойких материалов и антипиренов. Практическое значение нашли одно- и двухатомные фенолы с различной степенью бромирования. К числу самых многотоннажных продуктов относятся бромиро-ванный бисфенол А, а также 2,4,6-трибром- и пентабромфенолы. Фенолы являются довольно рекционноспособными соединениями и в боль-шинстве случаев их бромирование не вызывает затруднений. Бромирование фено-лов в воде протекает через арилоксидный анион, который протонируется и броми-руется. Медленной стадией процесса является конечная стадия отщепления про-тона. Промежуточный аддукт образуется быстро и обратимо, как только в раство-ре появляется бромирующий агент: OH-O O
+ B r 2 -Н+ Brили
Быстро БыстроМедленно HBr O-OH
Н+
Быстро
Br Br
Бромирование избытком брома проходит по схеме OH O OH
BrBrBrBr
3Br2Br2
-HBr Br Br Br
Естественно, что при получении 2,4,6-трибромфенола как конечного про-дукта в водной среде большой избыток брома недопустим. Тетрабромфенол явля-ется бромирующим агентом ароматических соединений. Он может также восста-навливаться 1%-ным раствором КI в присутствии 20%-го НСl до 2,4,6-трибромфенола. В связи с этим сначала ведут бромирование избытком брома, за-тем добавляют иодид калия и оттитровывают выделившийся иод. Тетрабромфенол (в хиноидной форме) отдает при этом четвертый атом бро-ма и переходит в 2,4,6-трибромфенол: OH
OBrBr
BrBr + 2I-+ HO + Br-+ - I + OH Br Br Br
Промышленный метод получения 2,4,6-триброфенола и дибромрезорцина осно-вывается на окислительном бромировании фенола в присутствии хлора: OH OH
BrBr
+ 1,5Br + 1,5Cl + 3HCl . Br
Основным бромирующим средством в промышленности является молеку-лярный бром или молекулярный бром в смеси с молекулярным хлором. Хлор вво-дят потому, что бром - дефицитное сырье. В отсутствие хлора улавливание выде-ляющегося HBr и его утилизация в виде бромоводородной кислоты не решают проблемы, так как потребность в этой кислоте не велика. Эффективным решением данной задачи является применение окислителей для перевода бромида водорода в бром. В качестве окислителя в процессах бромирования фенолов обычно ис-пользуют пероксид водорода. 2,4,6–Трибромфенол может быть получен таким образом: OH OH
BrBr
+ 1,5Br + 1,5HO + 3HO . Br
Выход целевого продукта достигает 85% при селективности ~ 90%. МОНОМЕРЫ ДЛЯ КАРБАМИДО-АЛЬДЕГИДНЫХ ПОЛИМЕРОВ Карбамидо-альдегидные полимеры (мочевино-формальдегидные олигоме-ры, смолы) - синтетические термореактивные продукты поликонденсации карба-мида с формальдегидом. Эти полимеры бразуются в результате поликонденсации первичных продуктов присоединения карбамида и формальдегида – метилкарба-мидов НNCОNНСНОН и СО(NНСНОН) -друг с другом, карбамидом и фор- мальдегидом и содержат повторяющуюся группу —NH—С(О)—NH—. Карбамидо-формальдегидные полимеры - смесь олигомеров различ-ной молекулярной массы линейного, разветвленного или циклоцепного строения, содержащих реакционноспособные NH-и ОН-группы. Получают и применяют карбамидо-формальдегидные олигомеры в виде водных растворов (преимущест-венно 40-70%-х) и порошков. Твердые сетчатые олигомеры бесцветны, светостой-ки, устойчивы в органических растворителях и маслах, легко окрашиваются. Од-нако они характеризуются пониженной водостойкостью, хрупкостью, низкой ус-тойчивостью к деструктивным воздействиям, выделением свободного формальде- гида. Для устранения этих недостатков олигомеры либо модифицируют при син-тезе путем замены части карбамида на модифицирующий агент, либо модифици-руют уже готовый олигомер, например путем частичной этерификации метилоль-ных групп. Карбамидо-формальдегидные олигомеры используют для производства кар-бамидо-формальдегидных пенопластов – заливочных теплоизоляционных мате-риалов. Для этих целей олигомеры получают при мольном соотношении карба-мид:формальдегид, равном 1:(1,3-1,7). Карбамидо-формальдегидные пенопласты применяют в строительстве: жидкой пеной заполняют полые стены из кирпича или других материалов при постройке и ремонте зданий. Пенопласты используют также для защиты овощей от промерзания в буртах, для закрепления песчаных почв, откосов и отвалов, как средство защиты растений от мороза, иногда для за-щиты почвы от промерзания. Карбамидо-формальдегидные олигомеры применяют в основном как свя-зующие в производстве древесностружечных плит и аминопластов, как основу клеев в производстве фанеры и древесных конструкций. Их используют также в производстве декоративных бумажно-слоистых пластиков, влагостойкой бумаги, в текстильной промышленности для аппретирования тканей с целью придания им несминаемости.Карбамидо-формальдегидные смолы, модифицированные бутано-лом, используют для получения карбамидо-алкидных лакокрасочных материалов. Полиметиленкарбамид – аморфный или кристаллический нерастворимый порош-кообразный продукт белого цвета, образующийся при взаимодействии карбамида и формальдегида при мольном соотношении 1:1, - используется в качестве пиг-мента в производстве бумаги, добавоки для эластомеров, адсорбента масел и ор-ганических продуктов. Получение карбамида Карбамид (диамид угольной кислоты, мочевина) (NН)СО представляет со- бой бесцветные кристаллы без запаха, растворяется в воде (51,8 г в 100 г воды при 293 К), в этаноле (5,4) и других спиртах (в меньших количествах). Взаимодействие карбамида с формальдегидом в соотношении менее 1:1 (моли) приводит к образованию карбамидо-формальдегидных смол. Этими смо-лами покрывают дерево, керамику, металлы и пр. При изготовлении лаков про-дукты конденсации пластифицируют полиэфирами. При получении карбамидо-формальдегидных смол клеевого назначения применяют полигликоли, фуриловый спирт или фурфурол совместно с метанолом или этанолом. Карбамидо-формальдегидные смолы широко используют для получения литьевых аминопластов. При этом в качестве наполнителей применяют волокни-стые материалы, например стеклянную вату. Использование в качестве наполни-телей гипса и каолина в присутствии некоторого количества волокнистых
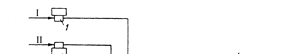
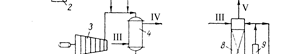
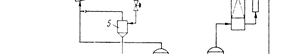
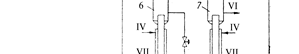
Рис. 15.5. Принципиальная технологическая схема процесса получения карбамида с полным рециклом горячих газов (процесс фирмы "Хемико") 1 – компрессор для СО2; 2 – компрессор для NH3; 3 – циркуляционный турбокомпрессор для газовой смеси; 4 – реактор-теплообменник; 5 – сепара- тор; 6 и 7 – аппараты для разложения карбамата 1-й и 2-й ступени; 8 – скруб- бер; 9 – холодильник; 10 – циркуляционный насос.Потоки: I – СО2; II - NH3; III – вода; IV – пар; V – инертные газы; VI - карбамид; VII – конден- сат
материалов позволяет получать аминопласты с хорошими механическими свойствами. Положительными качествами аминопластов являются стойкость к окислению, стабильность светлой окраски при кратковременном пребывании в пресс-формах до 442 К, нерастворимость в органических полярных и неполярных растворителях, хорошая теплопроводность и прочность. Однако аминопласты раз-рушаются под воздействием горячей, особенно кипящей воды, а также кислот и щелочей. Карбамид применяют также в качестве концентрированного азотного удоб-рения, заменителя естественного белка в кормах для жвачных животных и в этом качестве был известен уже давно. Карбамид впервые был синтезирован Ф. Вёлером в 1818 г. из цианата аммо-ния; это был первый синтез продукта животного происхождения из неорганиче-ского вещества. Позднее были разработаны и другие лабораторные методы синте-за карбамида. Одним из первых промышленных методов получения карбамида яв-ляется метод на основе цианамида кальция. В настоящее время в промышленности карбамид получают по реакции База-рова, который в 1868 г. установил, что при нагревании карбамата аммония в запа-янной трубке происходит образование карбамида. Он предложил получать карба-мид из аммиака и диоксида углерода:
2NН + СО NНСООNН DН = 125,6 кДж/моль, Карбамат аммония
NНСООNН (NН)СО + НО DН = - 15, 49 кДж/моль.
Процесс проводят при 453-503 К и давлении 12-25 МПа. Реакция протекает через образование аммонийных солей угольной кислоты. Все известные в настоящее время схемы производства карбамида из аммиа-ка и диоксида углерода различаются главным образом способом рекуперации не-прореагировавших веществ. На рис 15.5 представлена принципиальная технологическая схема процесса получения карбамида фирмы "Хемико" (США). Газообразные аммиак и диоксид углерода сжимаются компрессорами 1 и 2 до давления синтеза и смешиваются с горячим циркуляционным газовым потоком, подаваемым компрессором 3. Газовая смесь нагревается до 465-540 К, направля-ется в реактор-теплообменник 4, в котором происходит образование карбамида. Газовая фаза из аппарата для разложения карбамата аммония поступает в скруб-бер с насадкой 8, где раствором, циркулирующим через холодильник 9, поглоща-ются аммиак и диоксид углерода. Получение меламина Меламин (2,4,6-триамино-1,3,5-триазин, триамид циануровой кислоты) – NH 5 N 4 3 N N 6 2 NN H N 1 NH 2 2N бесцветные кристаллы, темп. пл. 637 К, не растворяется в органических раство рителях, растворяется в воде. Меламин является ценным химическим соединением, которое применяют для получения меламино-формальдегидных полимеров, обладающих высокой ме-ханической прочностью, стойкостью в горячей воде и органических растворите-лях, малой электропроводностью и высокой термостойкостью. Продук-ты,синтезируемые на основе меламино-формальдегидных полимеров, используют в различных отраслях промышленности: в электротехнической - для изготовления изоляторов, в текстильной – для производства безусадочных и не мнущихся тка- ней и для придания им блеска, в бумажной – для получения водонепроницаемой бумаги, в мебельной – для изготовления лаков, клеев, а также для приготовления дубителей, ионообменных смол, дезинфицирующих веществ, медицинских препа- ратов, негорючих составов и др. Меламин образуется из карбамида по реакции
6СО(NН) СНN + 6NН + 3СО 22 36632.
Реакция протекает при ~600 К с образованием в качестве промежуточного про- дукта циануровой кислоты. Зависимость равновесного выхода меламина от давле- ния и температуры показана на рис. 15.6. Как видно из рисунка, с возрастанием давления при постоянной температуре выход меламина уменьшается, так как рав- новесие реакции смещается в сторону образования карбамида. Наоборот, при по- вышении температуры и постоянном давлении выход меламина увеличивается. В зависимости от условий реакции можно добиться выхода меламина более 95%.
Рис. 15.6. Зависимость равновесного выхода 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|