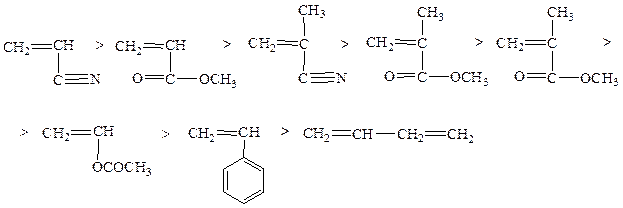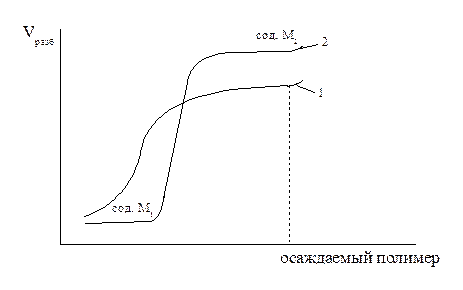|
|
Свободнорадикальная сополимеризацияКак и полимеризация включает в себя стадии: инициирования, роста и обрыва цепи. При реакции мономеров М1 и М2 со свободными радикалами инициатора R·, образуется новые радикалы, один из которых имеет концевое звено М1, а другой – М2. каждый из образовавшихся радикалов может реагировать как с мономером М1, так и М2, причем вероятность каждой стадии будет определяться ее константой скорости. Допуская, что активность растущего радикала определяется только активностью концевого звена и не зависит от числа и строения присоединившихся звеньев, можно различить четыре типа элементарных реакций соответствующие им константы скорости: 1) 2) 3) 4) Этими четырьмя элементарными реакциями определяется общая скорость расходования мономеров. Мономер М1 участвует только в реакциях 1 и 4, поэтому скорость его исчезновения равна:
Аналогично скорость исчезновения М2 равна:
Разделим
Т.к. за время роста цепи многократно осуществляются реакции 2 и 4, очень скоро равенство:
отсюда: Подставив уравнение (4) в уравнение (3), заменив
В уравнение (5) обозначим
Уравнение (6) описывает зависимость дифференциального мономерного состава сополимера от соотношения мономеров в данный момент сополимеризации. Величины r1 и r2 называют константами сополимеризации или относительными активностями мономеров. Они представляют собой отношение константы скорости реакции каждого радикала со своим мономером и константу скорости реакции с «чужим» мономером. Константы r1 и r2 определяют опытным путем для каждой пары мономеров. Для этого проводят сополимеризацию при различных соотношениях мономеров в исходной смеси, прерывая на малых степенях превращения (~5%). Определяют состоав полученного сополимера и, считая концентрацию мономеров М1 и М2 постоянными и равными исходным, решают уравнение (6) относительно одной из констант. r1 и r2 определяют вид кривой «мономерный состав – полимерный состав». При совместной полимеризации константы r1 и r2 могут принимать следующие значения: 1. Обе константы меньше единицы (r1 < 1и r2 < 1). Это значит, радикал 2. Одна из констант больше единицы, другая меньше: r1 > 1и r2 < 1 оба радикала r1 < 1и r2 > 1 сополимер будет обогащен мономером М2 (кривая 1). 3. При значении обеих констант больше 1 протекает раздельная полимеризация и образуется смесь полимеров. Если r1 и r2 существенно больше 1, то возможно образование блок-сополимера. 4. r1 и r2 = 1. Мономеры отдельно не полимеризуются, но дают сополимер. Независимо от соотношения мономеров в исходной смеси наблюдается строгое чередование М1 и М2 в макромолекуле сополимера:
Например: малеиновый ангидрид и 1,2-дифенилэтилен (r1 =0,03±0,03 и r2 = 0,003±0,003) отдельно не полимеризуются, но весте дают сополимер регулярного строения. 5. Если одна из констант, например r2 = 0, т.е. мономер М2 не может гомополимеризоваться, то образуется сополимер, который содержит участки состоящие из остатков мономера М1, соединенных с 1 остатком М2:
6. r1 = r2 = 1 – азеотропный сополимер, состав которого равен составу смеси мономеров.
На r1 и r2 не влияют многие параметры реакции (vин, наличие ингибиторов и агентов передачи цепи, типа инициатора), т.к. соответствующие константы скоростей не входят в уравнение сополимеризации. Произведение В большинстве случаев состав сополимера изменяется со времен проведения реакции. Вследствие этого у сополимеров наряду с неоднородностью по степени полимеризации, появляется неоднородность по составу (композиционная неоднородность). Такое течение процесса сополимеризации напоминает непрерывное изменение состава дистиллята при перегонке жидкостей. И точно также существует азеотропная смесь, у которых состав перегоняемого продукта и дистиллята совпадают. Могут образовываться азеотропные сополимеры с таким же соотношением М1 и М2 в их макромолекулах, как и в исходной смеси мономеров. Для получения азеотропного сополимера, т.е. достижения равновесия:
отношение
Уравнение имеет реальный физический смысл, всегда Для уменьшения композиционной неоднородности и сохранения заданного соотношения компонентов в сополимере используются следующие приемы: 1.Сополимеризацию проводят при непрерывном добавлении небольших количеств более реакционноспособного мономера с тем, чтобы его концентрация оставалась постоянной. 2.Сополимеризацию проводят в растворителе, в котором хорошо растворим менее реакционноспособный мономер и ограниченно растворим более реакционнспособный. Тогда более реакционноспособный мономер постепенно переходит в раствор и т.о. его концентрация в растворе поддерживается постоянной. Доказательства наличия сополимеризации осуществляется методом фракционного осаждения полимера из разбавленного раствора при помощи разбавителя (разбавитель - вещество смешивающееся с растворителем, но не растворяющее полимер). Кривые осаждения сополимера и смеси полимеров:
При осаждении сополимера осадок выпадает плавно и равномерно по мере добавления растворителя. При образовании смеси полимеров
ИОННАЯ СОПОЛИМЕРИЗАЦИЯ Наиболее ярко различие между радикальными, анионными и катионными процессами проявляется в реакциях сополимеризации, а именно в составе сополимеров. Это объясняется различной реакционной способностью одних и тех же мономеров в реакциях роста цепи при радикальной и ионной сополимеризациях. Пример: Система: стирол – ММА 1. Катионный механизм r1 = 10; r2 = 0,1; r1• r2 = 1 2. ЦРП r1 = 0,52; r2 = 0,46; r1• r2 = 0,24 3. Анионный механизм r1 = 0,1; r2 = 6; r1• r2 = 0,6
ЦРП:
Менее активный радикал взаимодействует с более активным мономером и наоборот, поэтому будет наблюдаться более или менее правильное чередование звеньев. Кроме того, скорости присоединения каждого мономера к растущему радикалу отличаются незначительно поэтому оба мономера расходуются почти с одной и той же скоростью, а состав сополимера мало отличается от состава мономерной смеси.
КП: Растущий катион с любым концом:
будет предпочтительно реагировать со стиролом, обладающим более высокой электронной плотностью, и содержание стирольных остатков в сополимере будет большим, чем остатков ММА.
АП: Растущий анион:
будет реагировать с ММА, обладающим низкой электронной плотностью. Таким образом , при КП более активным мономером (r1 = 10) оказывается стирол, при АП – ММА (r2 = 6), а при ЦРП активности оказываются приблизительно одинаковыми. Катионная полимеризация:

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|

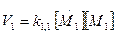 - гоморост
- гоморост
 - перекрестный рост
- перекрестный рост
 - гоморост
- гоморост
 - перекрестный рост
- перекрестный рост (1)
(1) (2)
(2) на
на  получим:
получим: (3)
(3)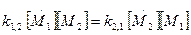
 (4)
(4) на
на  и проведя ряд преобразований, получим:
и проведя ряд преобразований, получим: (5)
(5) и
и  , и получим дифференциальное уравнение сополимеризации Майо и Льюиса:
, и получим дифференциальное уравнение сополимеризации Майо и Льюиса: (6)
(6) легче реагирует с мономером М2, а радикал
легче реагирует с мономером М2, а радикал  с мономером М1, т.е. оба мономера склонны к сополимеризации (кривая 3). Причем до точки перегиба полимер обогащен мономером М2, а после М1.
с мономером М1, т.е. оба мономера склонны к сополимеризации (кривая 3). Причем до точки перегиба полимер обогащен мономером М2, а после М1. и
и 
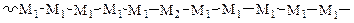
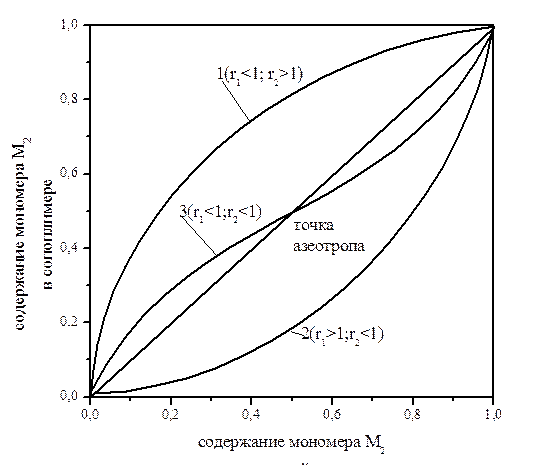
 определяет склонность звеньев к чередованию. При
определяет склонность звеньев к чередованию. При  звенья обоих типов присоединяются по закону случая. При
звенья обоих типов присоединяются по закону случая. При  вероятность чередования звеньев увеличивается. В пределе когда
вероятность чередования звеньев увеличивается. В пределе когда  , можно получить регулярно чередующийся сополимер. Почти во всех изученных бинарных системах
, можно получить регулярно чередующийся сополимер. Почти во всех изученных бинарных системах  .
. в уравнении
в уравнении 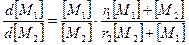
 должно быть равно 1, т.е.
должно быть равно 1, т.е. 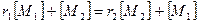 , откуда заменив
, откуда заменив  ,
, 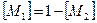 , получим
, получим 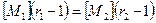
 -условие азеотропа
-условие азеотропа ,т.к. отношение концентраций не может быть отрицательной величиной. Такое условие будет соблюдено, если одновременно r1 > 1и r2 > 1 или r1 < 1и r2 < 1, чтобы оба растущих радикала предпочтительно реагировали с одноименными (своими) мономерами или разноименными (чужими). При r1 = r2 = 1 азеотроп получится при любом соотношении мономеров.
,т.к. отношение концентраций не может быть отрицательной величиной. Такое условие будет соблюдено, если одновременно r1 > 1и r2 > 1 или r1 < 1и r2 < 1, чтобы оба растущих радикала предпочтительно реагировали с одноименными (своими) мономерами или разноименными (чужими). При r1 = r2 = 1 азеотроп получится при любом соотношении мономеров.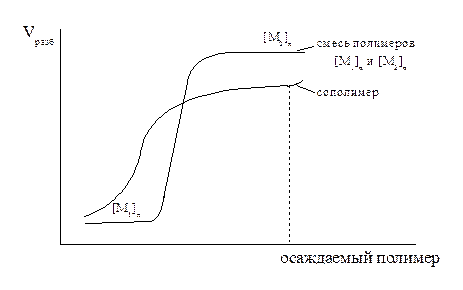
 и
и 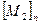 наблюдается резкий переход от продукта содержащего звенья М1 к продукту, содержащему звенья М2.
наблюдается резкий переход от продукта содержащего звенья М1 к продукту, содержащему звенья М2.
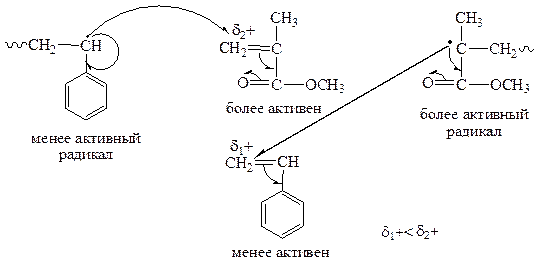
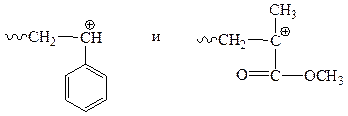
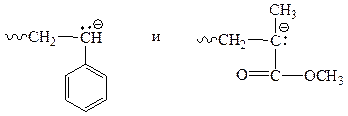
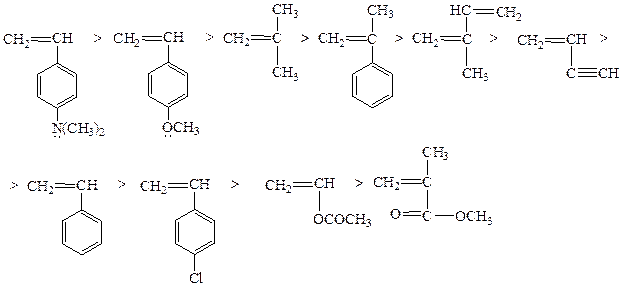 Анионная полимеризация:
Анионная полимеризация: