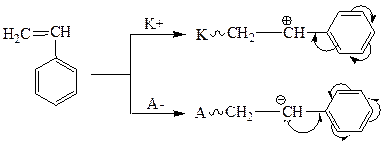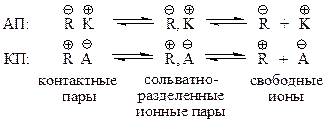|
|
Ионная полимеризация (ИП)Ионная полимеризация протекает в присутствии катализаторов, которые в отличии от инициаторов не расходуются в процессе полимеризации и не входят в состав полимера. Разрыв двойной связи происходит по гетеролитическому механизму с образованием либо катиона, либо аниона и полимеризация идет по цепному механизму. В зависимости от знака заряда различают полимеризацию катионную и анионную. Если при ионной полимеризации реакция роста цепи сопровождается координацией мономера на поверхности катализатора, то полимеризация называется ионно-координационной. Особенности ИП: 1. Высокая координирующая способность катализатора приводит к образованию линейных макромолекул регулярного строения, а в ряде случаев и стереорегулярного. 2. Полученные полимеры характеризуются высокой молекулярной массой и узким ММР. 3. Энергия активации ИП ниже чем ЦРП, поэтому ИП идет при более низких температурах, часто отрицательных, с очень высокой скоростью. 4. Функция катализатора не ограничивается только участием в реакции инициирования: катализаторы влияют на реакцию роста и обрыва цепи, участвует в реакциях передачи цепи. Это определяет кинетику процесса. При ЦРП инициатор не оказывает влияние на структуру полимера. 5. ИП характеризуется ярко выраженной селективностью. Мономеры, содержащие электронодонорные заместители участвуют в катионной полимеризации, а электроноакцепторные – в анионной.
Но для стирола, когда сопряжение стабилизирует и катион, и анион, возможна как катионная, так и анионная полимеризация:
6. В некоторых случаях ИП отсутствуют реакции обрыва и передачи цепи. В этом случае образуются т.н. «живущие» полимеры, макромолекулы которых сохраняют активные центры (после исчерпания всего мономера) и способны к присоединению новых порций мономера, т.е. к продолжению роста цепи. Активные центры при ионной полимеризации состоят из растущего иона (R+ или R-) и противоиона (А- или К+). Стабильность и структура ионной пары зависят от их свойств и сольватирующей способности растворителя при сильной сольватации ноны могут быть изолированы друг от друга. Различают три основные формы существования ионов в растворе:
Свободные ноны характеризуются гораздо большей активностью, чем ионные пары, поэтому реакционная способность активных центров при ионной полимеризации в отличие от радикальной ИП в значительной степени зависит от свойств реакционной среды. Часто устойчивость карбониевых ионов и карбанионов настолько мала, что они практически вовсе не образуются или, если образуются, быстро разрушаются. Вместе с тем в присутствии растворителей, сольватирующих их с выделением значительной энергии сольватации, или при достаточно низких температурах стабильность ионов возрастает настолько, что они успевают присоединиться к мономеру и вызвать полимеризацию. Хотя при этом желательны растворители высокой полярности с максимально возможной энергией сольватации, многие из них неприменимы, так как они (например, вода, спирты) разлагают большинство ионных катализаторов или, как кетоны, образуют с ними прочные комплексы, что препятствует инициированию полимеризации. Кроме того, используемые растворители должны оставаться жидкими при температуре реакции, иногда находящейся ниже — 100° С. Этим требованиям отвечают такие сравнительно малополярные растворители, как хлористый метил, пентан и нитробензол, в которых обычно и проводят ионную полимеризацию. В подобных растворителях ионы представляют собой не изолированные частицы, а находятся в виде прочно связанных ионных пар, состоящих из растущего иона и иона противоположного заряда (противоион), причем расстояние между ними растет с увеличением сольватирующей способности растворителя.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 Катионная полимеризация: заместители стабилизируют карбокатион.
Катионная полимеризация: заместители стабилизируют карбокатион.
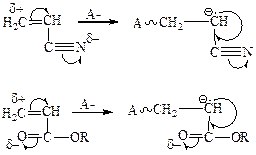 Анионная полимеризация: заместители стабилизируют карбоанион.
Анионная полимеризация: заместители стабилизируют карбоанион.