|
|
Детерминация половых клеток у насекомыхЯйца некоторых насекомых также содержат зародышевую плазму, функция которой, по-видимому, очень сходна с функцией зародышевой плазмы у Parascaris. У галлицы Wuchtiella persicariae большая часть ядер утрачивает 32 из 40 исходных хромосом! Однако на заднем полюсе яйца находятся два ядра, в которых не происходит диминуции хроматина и которые в течение некоторого времени не делятся (рис. 7.22). Потомки этих двух ядер в конечном счете включаются в первичные половые
Гилберт С. Биология развития: В 3-х т. Т. 2: Пер. с англ. – М.: Мир, 1994. – 235 с. 26________________ ГЛАВА 7______________________________________________________________________________
клетки1. Если препятствуют миграции этих ядер в область заднего полюса путем наложения лигатуры, тο в каждом ядре происходит диминуция хроматина и возникающая из такого яйца галлица оказывается стерильной Если ослабить лигатуру и позволить таким ядрам переместиться в область заднего полюса, то первичные половые клетки образуются, но они никогда не становятся функциональными гаметами (Geyer-Duszynska. 1959). Было показано (Kunz et al.. 1970), что элиминированный хроматин содержит гены, являющиеся активными в период образования первичных половых клеток. Герминативная цитоплазма насекомых отличается от любой другой цитоплазмы яйца. Хегнер (Hegner, 1911) обнаружил, что при удалении или разрушении этой области до формирования клеток на заднем полюсе яиц некоторых жуков зародыши, развившиеся из таких яиц, не имеют половых клеток и оказываются стерильными. Очень удачно, что эта задняя полярная плазма маркирована полярными гранулами (рис. 7.23). Роль этих гранул в детерминации половых клеток неизвестна, однако их постоянная связь с полярной плазмой и с происходящими из нее полярными клетками делает полярные гранулы удобными маркерами этой области яйца. Данную область полярных клеток легко идентифицировать с помощью сканирующего электронного микроскопа (рис. 7.24). Современные исследования полярной цитоплазмы проводятся преимущественно на зародышах дрозофилы. В течение первых двух часов после оплодотворения зародыш дрозофилы развивается как синцитий. Иными словами, происходит только деление ядер без соответствующего деления цитоплазмы. В результате формируется слой неклеточной синцитиальной бластодермы, содержащий около 3500 ядер. Каждое ядро окружается клеточной мембраной, и бластодермальный слой становится клеточной бластодермой. Опыты по трансплантации (Zalokar. 1971; Illmensee. 1968. 1972) показали, что все ядра синцития эквивалентны и тотипотентны. Однако клетки в клеточной бластодерме строго детерминированы. К сходному заключению пришли и другие исследователи (Schubiger. Wood. 1977). которые накладывали лигатуры на яйца дрозофилы, находящиеся на разных стадиях развития. В ядрах дрозофилы диминуции хроматина не происходит и ядро синцитиальной стадии может дать начало либо первичным половым, либо соматическим клет-
1 Пример галлицы и Parascaris выглядит как очень убедительное доказательство в пользу гипотезы Вейсмана о сегрегации ядерных детерминантов (которая обсуждается в гл. 8). Эти случаи диминуции хроматина и элиминации хромосом являются исключениями из общего правила (гл. 9 и 10), поскольку обычно в ядрах дифференцированных клеток сохраняются неиспользуемые гены; мы не располагаем данными о том, что в различных соматических клетках Wachtiella или Parascaris сохраняются разные части их генома.
Гилберт С. Биология развития: В 3-х т. Т. 2: Пер. с англ. – М.: Мир, 1994. – 235 с. __________________ ДЕТЕРМИНАЦИЯ ПОСРЕДСТВОМ ЦИТОПЛАЗМАТИЧЕСКОЙ СПЕЦИФИКАЦИИ___________ 27
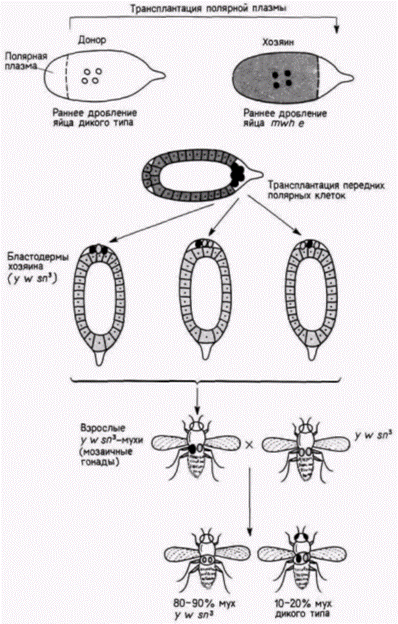
кам. Их детерминация зависит от области яйца. в которую они мигрируют. Одной из этих областей является задняя полярная плазма. Таким образом, полярная плазма, по-видимому, содержит морфогенетические детерминанты для образования половых клеток. Было обнаружено (Geigy, 1931), что облучение полярной плазмы ультрафиолетом приводит к стерильности мух. развившихся из облученных яиц, a Окада и др. (Okada et al.. 1974). продолжившие эту линию исследований, показали, что введение полярной плазмы из необлученных зародышей-доноров в облученные яйца устраняет их стерильность (рис. 7.25). Введение любой другой части цитоплазмы в их опытах не приводило к такому результату. В том же, 1974 г. автономность этой цитоплазматической области и ее способность детерминировать любое ядро дрозофилы была доказана остроумными опытами Илменси и Мэховалда (lllmensee, Mahowald, 1974). В этих опытах (рис. 7.26) неправдоподобно малое количество (5-100 пиколитров) энуклеированной полярной плазмы было перенесено из яиц дрозофилы дикого типа (донор) в область переднего полюса генетически маркированных яиц (хозяин) до их целлюляризации. (Эти яйца хозяина несли хромосомные мутации multiple wing hair (mwh и ebony (e).) После формирования клеточной бластодермы клетки переднего полюса зародыша-хозяина напоминали нормальные полярные клетки заднего полюса, содержали включенные в них полярные гранулы и их морфология была типичной для нормальных полярных клеток. Чтобы проверить, станут ли эти клетки предшественниками функциональных половых клеток, Мэховалд и Илменси трансплантировали модифицированные клетки переднего полюса в заднюю область дробящихся зародышей, содержащих свои собственные генети-
Гилберт С. Биология развития: В 3-х т. Т. 2: Пер. с англ. – М.: Мир, 1994. – 235 с. 28 ГЛАВА 7
чески маркированные полярные клетки1. Эти новые зародыши-хозяева были маркированы по другим мутациям рецессивным yellow (y), while (w) и sinqed (sn3). Все мухи, развившиеся из таких зародышей, несли мутации yellow, white и singed. Этих мух скрестили с другими мухами, несущими такие же мутации. В большинстве случаев (88 из 92 скрещиваний) в потомстве появились особи, идентичные обоим родителям. Однако в четырех случаях возникли потомки дикого типа. Их появление указывало на то. что некоторые половые клетки у этих мух произошли из трансплантированных клеток, следовательно, половая плазма одного зародыша была способна побудить ядра клеток в области переднего полюса другого зародыша детерминировать развитие функциональных половых клеток! Использован-
1 Это было сделано для того, чтобы дать им возможность включиться в развивающуюся гонаду. Имеются данные, полученные на других организмах, о том. что полярная плазма содержит также детерминанты для соответствующей миграции половых клеток в гонады (Züst, Dixon, 1977; Ikenishi, Kotani, 1979).
Гилберт С. Биология развития: В 3-х т. Т. 2: Пер. с англ. – М.: Мир, 1994. – 235 с. __________________ ДЕТЕРМИНАЦИЯ ПОСРЕДСТВОМ ЦИТОПЛАЗМАТИЧЕСКОЙ СПЕЦИФИКАЦИИ_________________ 29
ная методика оказалась также полезной для установления времени локализации этого детерминанта. Илменси и др (Illmensee et al.. 1976) обнаружили, что детерминант первичных половых клеток способен функционировать до оплодотворения и локализуется в развивающемся ооците примерно в то же самое время, когда желток достигает его заднего конца. Сама природа предоставляет в наше распоряжение свидетельства о значении полярной плазмы и полярных гранул для развития половых клеток. Самка дрозофилы, гомозиготная по мутации qrand-childless, продуцирует фенотипически нормальное, но стерильное потомство [GG (самец) х дд (самка) ® Gg (стерильны)]. Мэховалд и др. (Mahowald et al., 1979) показали, что если таких самок спарить с нормальными самцами, то ядра зародышей, получившихся в результате скрещивания, никогда не мигрируют в полярную плазму яйца. У этих зародышей полярные клетки не образуются, а у получившихся взрослых особей нет первичных половых клеток, из которых развиваются гаметы. Другая мутация с материнским эффектом – agametic - вызывает отсутствие первичных половых клеток примерно у половины потомков, полученных от гомозиготных самок. В этом случае у потомков формируется нормальное число полярных клеток, но полярные гранулы разрушаются вскоре после оплодотворения (Engstrom et al.. 1982). Опыты по трансплантации показали, что дефект заключается в самой полярной плазме, а не в яичнике. Таким образом, теперь получены очень четкие доказательства того, что полярные гранулы имеют прямое отношение к образованию половых клеток. Эти полярные гранулы были выделены из зародышей дрозофилы (Waring et al.. 1978): оказалось, что они содержат белок и РНК. Молекулярная масса этого белка ( в гранулах, по-видимому, преобладает один белок) равна 95000: он обладает основными свойствами и синтезируется заново в период оогенеза, так что полярные гранулы не наследуются непосредственно через цитоплазму яйца. РНК присутствует в полярных гранулах ооцита. но не обнаруживается после того, как сформировались полярные клетки (Mahowald. 1971a. b). Возможно, что эта РНК чрезвычайно важна для формирования половых клеток. Окада и Кобаяси (Okada. Kobayashi. 1987) инъецировали РНК из яиц и ранних дробящихся зародышей дрозофилы зародышам, у которых полярные клетки были убиты ультрафиолетом. Эти зародыши-хозяева формировали полярные клетки и развивались в мух, имевших половые клетки. Полярные гранулы изменяются в процессе развития. До оплодотворения плотные гранулы, содержащие мембраны, группируются вокруг митохондрий, а затем диспергируются, прежде чем ядра достигнут полюса. Впоследствии полярные клетки включают в себя эти гранулы. Когда полярные клетки мигрируют в половой валик, полярные гранулы деконденсируются на филаменты. называемые nuage. Этот материал скапливается около оболочки ядра. Такое поведение полярных гранул обнаружено у всех изученных представителей животного царства (Eddy. 1975) и, вероятно, имеет важное значение для гаметогенеза. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|





 1
1