
|
|
ФАКТОРЫ ХИМИЧЕСКОЙ РЕГУЛЯЦИИ ПРИ ИШЕМИЧЕСКИХ И НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЯХ МОЗГА.IV-1. ИШЕМИЧЕСКИЕ ЗАБОЛЕВАНИЯ ГОЛОВНОГО МОЗГА · Структура цереброваскулярных заболеваний. · Нейромедиаторы. Система возбуждающих аминокислот. · Роль оксида азота. · Регуляторные пептиды. · Нейротрофические и ростовые факторы. Интерлейкины. · Регуляция трансмембранных процессов при ишемии мозга. · Гормоны при ишемии мозга. · Ишемия неонатального мозга. · Интракраниальные геморрагии. · Нейропротекция и терапия ишемических заболеваний мозга. IV-2. НЕЙРОДЕГЕНЕРАТИВНЫЕ ЗАБОЛЕВАНИЯ МОЗГА · Структура нейродегенеративных заболеваний. · Нарушения медиаторной системы мозга. · Пептиды. Нейротрофические и ростовые факторы мозга. Цитокины. · Амилоидные пептиды: молекулярная основа болезни Альцгеймера. · Генетические аспекты патологии Альцгеймера. Литература к разделу IV.
РАЗДЕЛ V. ЦЕРЕБРОЛИЗИН. ОПЫТ КЛИНИЧЕСКИХ И ЭКСПЕРИМЕНТАЛЬНЫХ ИССЛЕДОВАНИЙ. ВВЕДЕНИЕ · Экология «современного мозга». · История открытия и внедрения Церебролизина как медицинского препарата.
V-1. КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ · Обоснования применения Церебролизина. Концепция нейротрофической терапии. · Церебролизин и деменциальные расстройства различной этиологии. · Церебролизин и терапия ишемического инсульта. · Церебролизин и терапия экстрапирамидных расстройств мозга. · Церебролизин и терапия психосоматических расстройств, обусловленных экстремальными воздействиями. · Церебролизин и травма мозга. · Церебролизин и детская психоневрология. · Церебролизин и другие заболевания.
V-2. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ ЦЕРЕБРОЛИЗИНА. · Токсикологические исследования. Оценка безопасности. · Анализ побочных реакций в клинических исследованиях ЦР.
V-3. ЭКСПЕРИМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ. · Исследования на тканевых препаратах и культурах нейронов. · Влияние Церебролизина на окислительный метаболизм. · Влияние на медиаторные процессы. · Влияние Церебролизина на функциональные белки. · Влияние Церебролизина на поведение и память. · Исследования на моделях поврежденного мозга. · Церебролизин и концепция «программируемой смерти» нервных клеток.
V-4. СОВРЕМЕННАЯ СТРАТЕГИЯ КЛИНИЧЕСКОГО ПРИМЕНЕНИЯ ЦЕРЕБРОЛИЗИНА · Теоретические предпосылки. Опыт клинических и экспериментальных работ. Литература к разделу Y.
Р А З Д Е Л I.
НЕЙРОТРОФИЧЕСКИЕ И РОСТОВЫЕ ФАКТОРЫ. ЦИТОКИНЫ ВВЕДЕНИЕ Ростовые и нейротрофические факторыявляются полипептидами, которые, воздействуя на различные типы клеток, участвуют в реализации их функций в широком спектре жизненного цикла. Действие ростовых и нейротрофических факторов заключается в модуляции биологических процессов, осуществляемых на различных уровнях; в общем виде это влияние состоит в регуляции экспрессии генов функционально значимых белков, рецепторов, медиаторов и, соответственно, включении и/или выключении альтернативных регуляторных звеньев (систем). Основная роль этих факторов состоит в регуляции переживания, дифференцировки и роста клеток различных тканей и организации основных физиологических процессов. Исходно факторы синтезируются в лимитированных количествах, активно экспрессируясь в соответствии с функциональной потребностью. Часть этих факторов действует, как правило, локально в пределах ограниченной популяции клеток (ауто- или паракринная регуляция), другие (или в других ситуациях) - дистантно, циркулируя с током крови. Структурно нейротрофические и ростовые факторы представлены полипептидами в несколько десятков (до 100-150) аминокислотных остатков (существенное отличие от регуляторных пептидов, см. ниже), организованных в одно- или двухдоменные формы. Реализация активности любого фактора происходит при взаимодействии с рецептором; специфичность взаимодействия лиганда и рецептора отвечает характеру запускаемых сигнальных реакций и определенному типу биологического процесса. Полная трансдукция сигнала осуществляется комплексом взаимодействий между активированным рецептором и другими сигнальными молекулами. Нейротрофические и ростовые факторы, цитокины и гормоны, опосредуют межклеточную коммуникацию, участвуя в регуляции специфических функций. Молекулы, осуществляющие транслокацию сигнала, проходя через ядерную мембрану, связываются с промотерным регионом ДНК и стимулируют экспрессию гена. Структура рецептора обычно включает два основных компонента: лиганд-связывающий и эффекторный домены. Лиганд-связывающий домен определяет специфичность лиганда. Эффекторный домен инициирует начало биологического ответа после связывания лиганда. Димерные рецепторные комплексы активируют индивидуальные сигнальные пути, представленные различными эффекторными белками. Димеризация вызывает цепь процессов, начинающихся реакцией фосфорилирования и завершающихся различными типами биологического ответа, таких как пролиферация и апоптоз.
Ни по химическим признакам, ни по характеру биологической активности нет четких градаций между РОСТОВЫМИ и НЕЙРОТРОФИЧЕСКИМИ факторами. Однако анализ современной информации позволяет акцентировать некоторые аспекты: (а) Нейротрофические факторы - Фактор роста нервов (NGF), Нейротрофический фактор мозга (BDNF), Нейротрофины -3 и 4/5 (NT-3, -4/5), Глиальный и Цилиарный нейротрофические факторы (GDNF и CNTF) контролируют дифференцировку, рост, и сохранение клеток преимущественно центральной и периферической нервной систем. Для них характерен ретро- или антеградный транспорт зрелых молекул по аксону или локальный синтез в прилегающих клетках. (б) Ростовые факторы – Эпидермальный ростовой фактор (EGF), Инсулиноподобный ростовой фактор (IGF), Эндотелиальный фактор роста сосудов (VEGF), Тромбоцитарный ростовой фактор (PDGF), Трансформирующий ростовой фактор (TGF), Фактор некроза опухоли (TNF) участвуют в регуляции роста, дифференцировки, локомоции и сократимости клеток большинства тканей на периферии, включая клетки крови. По типу запускаемых сигнальных реакций ростовые факторы характеризуются в большинстве случаев как МИТОГЕНЫ, т.е. промотеры активности ядерного аппарата клетки. Ростовым факторам в большей мере присущ эндокринный принцип влияния на ткани и потому изначальное наименование отдельных факторов может не соответствовать профилю их действия. (в) Несмотря на большое разнообразие типов (молекулярных структур) рецепторов, соединяющихся с теми или иными группами факторов, можно выделить определенные различия для нейротрофических и ростовых полипептидов. Доменная структура рецепторов, их изоформ и типов сигнальных реакций, запускаемых с того или иного лиганда, оказывается чрезвычайно вариабельной и не вполне ясно классифицированной. (г) Ростовые факторы по ряду структурных и функциональных признаков сходны с цитокинами. Потому, взаимодействуя с рецепторами, они могут влиять на активность клеток иммунной системы и участвовать в контроле воспалительных реакций, включая локальные провоспалительные явления в мозге при развитии нейродеструктивных процессов. (д) Исследование химической структуры нейротрофических и ростовых факторов позволяет анализировать трехмерную конфигурацию фактора и профиль его биологической активности. В этом контексте выявляются закономерности пространственного контакта фактора (лиганда) с соответствующей структурой рецептора и индукции сигнальных реакций (см. Ibanes, 1998). Сравнение деталей пространственной организации различных факторов и цитокинов позволяет выделить некоторые пограничные различия. В структурах PDFG-A, PDFG-B; VEGF’s; NGF; BDNF; NT-3; NT-4; TGF-beta1-5 и активина основным является длинный участок (аминокислотная последовательность) бета-складчатой структуры, включающий сульфгидрильную «связку». В структуре Инсулиновых факторов (IGF-I, -II), а также самого инсулина базовым служит короткое спиральное построение с бета-складчатой организацией в виде “свитка”. Эпидермальный фактор (EFG), Фактор некроза опухоли (TNF-alpha) и Гепарин- связывающий эпидермальный фактор (HB-EFG) представлены короткой аминокислотной цепью в виде бета-складчатой структуры, богатой сульфгидрильными группами. Цилиарный фактор (CNTF), Ингибирующий фактор лейкемии (LIF) и гормональный фактор лептин включают длинный 4альфа-спиральный участок. Структура короткого 4альфа-спирального участка является характерной для интерферона-гамма и большинства интерлейкинов (IL-2, IL-3, IL-4, IL- 7, IL-9, IL-13), а также для семейства факторов CSF (Colony Stimulating Factor 1).
Анализ данных, суммированных в таблице 1, позволяет оценить «динамику интереса» исследователей, то есть, в конечном счете, отражает значимость того или иного нейротрофического/ростового фактора в процессе выбранного десятилетнего срока изучения. Другая позиция, анализируемая по данным таблицы, позволяет оценить вероятное значение вещества в отношении функций, относящихся к мозгу. 1. Первые строчки в ранге общего числа публикаций (совпадающих в целом как за десятилетний срок, так и за последние два года) занимают исследования по интерлейкинам и тесно связанные с ними работы по Фактору некроза опухоли (TNF). Число этих публикаций в среднем четырехкратно превышает число работ последующих рангов (VEGF, NGF, IGF, EGF). 2. Иными оказываются ранги числа публикаций, связанных с исследованием нервной системы. Здесь первые места принадлежит Фактору роста нервов (NGF), Нейротрофическому фактору мозга (BDNF) и далее, с двукратным уменьшением, интерлейкинам, Фактору некроза опухоли (TNF) – в первую очередь за счет превалирования общего числа работ, а также Инсулиноподобному ростовому фактору (IGF) и Эпидермальному ростовому фактору (EGF). 3. Оценивая интерес по отдельным факторам, связанным с исследованиями мозга (графа «СОЕДИНЕНИЕ + мозг» в таблице 1), следует выделить несомненное лидерство BDNF (около 90% общего числа работ по фактору), Нейротрофины-3 и –4/5 (соответственно, 71,6 и 87,5%%); для Цилиарного и Глиального факторов эти значения составляют около 50%. Для факторов, следующих под титулом «ростовые», эти цифры по исследованию мозга составляют лишь от 7,9 до 5,2 %%. 4. Оценивая рост числа работ по каждой позиции в течение десятилетнего срока, следует отметить в целом равномерный темп для большинства факторов. Тем не менее, интересно значительное увеличение числа ссылок за последние 2-5 лет для TNF (+1,3 раза), GDNF (+1,5), BDNF (+1,4) и особенно по VEGF (+2,0), и, наоборот, снижение интереса по CNTF почти вдвое. Эти данные относятся как в числу публикаций в целом, так и к количеству работ по мозгу. Приведенные информационные данные относятся как непосредственно к статьям, посвященным изучению определенного соединения (фактора), так и сопутствующему или косвенному его упоминанию в публикации. В целом приведенные в таблице сведения в существенной мере отражают уровень интереса – читай, уровень значимости – в организации и финансировании экспериментальных и клинических работ в мире по проблеме нейро- трофических и ростовых регуляторных факторов.
ТАБЛ. 1. ЧИСЛО ПУБЛИКАЦИЙ, ПОСВЯЩЕННЫХ НЕЙРОТРОФИЧЕСКИМ И РОСТОВЫМ ФАКТОРАМ ПО ДАННЫМ PUBMED (март 1994-март 2004)
В таблице указан ранг по числу публикаций за последние пять лет (I-YI) и процент публикаций по мозгу в сравнении с общим числом работ (упоминаний) по соединению. НЕЙРОТРОФИЧЕСКИЕ ФАКТОРЫ
ОБЩАЯ ХАРАКТЕРИСТИКА.Нейротрофические факторы включают группы (подсемейства) структурно гомологичных пептидов, исходно оцениваемых по сходству с первым из открытых представителей ростовых факторов вообще – NGF. Основанные на структурной гомологичности аминокислотных последовательностей, типичных для цитокинов, нейротрофины делятся на три подсемейства. (А) Собственно “нейротрофины”, куда относятся NGF, BDNF, NF-3, NF-4/5. (Б) Подсемейство Глиального фактора, которое включает: собственно GDNF, Neurturin (NTR), Artemin (ART), Persephin (PSP). (В) Подсемейство Цилиарного (реснитчатого) фактора, включающего CNTF, Ингибирующий фактор лейкемии (LIF) и интерлейкин-6 (IL-6). Нейротрофические факторы играют ключевую роль в развитии и сохранении структур центральной и периферической нервной системы. Большую роль в распределении нейротрофинов в локальных структурах мозга играет антеградный и ретроградный транспорт. Среди многих функций нейротрофинов описывается их роль в широком спектре явлений, характеризующих деятельность ЦНС в норме и патологии. Главным можно считать их участие в контроле процессов физиологического развития нейронов, фенотипической деафферентации и сохранения структурной и функциональной целостности нервных или глиальных клеток. Существенна роль нейротрофинов в апоптических процессах, связанных нейродеструкцией. См. также посвященный нейротрофинам обзор Dechant & Neuman (2002). РЕЦЕПТОРЫ. Нейротрофины активируют тирозинкиназные рецепторы семейства trk (trk-A, trk-B, trk-C), которые представляют собой подструктуру низкоаффинного рецептора tp75NTR, или p75, суперсемейства рецепторов Некротического фактора опухолей (TNF). Хотя tp75NTRне передает непосредственно сигнал от NGF, этот рецептор, по-видимому, повышает реактивность trk рецепторов и играет роль в ретроградном транспорте сигнала нейротрофинов из терминалий аксона в тело клетки. NGF соединяется высокоаффинной связью и активирует trk тирозинкиназный рецептор, ответственный за сигнальную трансдукцию BDNF, как и NT-4 активирует trk-B тирозинкиназный рецептор; NT-3 активирует trk-C рецептор, но может также взаимодействовать в некоторых клеточных системах с остальными рецепторами группы trk (РИС. 1).

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|

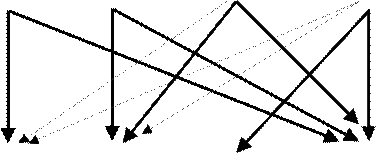
 ЛИГАНДЫ: NGF BDNF NT-4 NT-3
ЛИГАНДЫ: NGF BDNF NT-4 NT-3