|
|
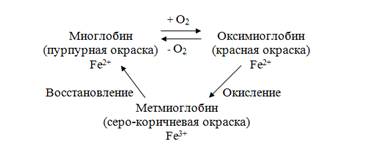
Зависимость ВСС от состояния мяса.Наибольшей влагоемкостью и способностью удерживать воду обладает парное мясо, рН нативного мяса 7,2. В начале автолиза рН парного мяся относительно высок и близок к нативному 6,6-7,0. Незначительное снижение рН в первые часы после убоя обусловлено медленным накоплением молочной к-ты и противодействием буферных систем тканей изменению рН.Белки мяса находятся в ионизированном состоянии и обладают высокой водосвязывающей способностью. Высокая ВСС парного Мяса имеет большое значение в производстве вареных колбасных изделий, так как от нее зависят сочность, консистенция и выход готовых изделий.По мере развития окоченения ВСС мяса уменьшается и достигает минимума к моменту наиболее полного развития окоченения. В результате накопления молочной, пировиноградной и ортофосфорной к-т, а также потери буферной способности белками рН мяса резко сдвигается в кислую зону до 5,6-5,2, вследствие чего уменьшается ВСС белков.С началом разрешения окоченения постепенно повышается ВСС мяса. Как следствие фермтивных гидролитических превращений, а также физико-химических изменений белков разрушаются структурные элементы мышечного волокна. "Разрыхление" белковых структур и увеличение числа свободных гидрофильных групп вызывают повышение ВСС мяса. Интенсивность нарастания ее наибольшая в первые сутки после окоченения. 30Реакции цветообразования. Факторы, влияющие на цветообразование Цвет свежего несоленого мяса обусловлен содержанием в нем пигментов — миоглобина, гемоглобина, цитохрома. Последние два пигмента практически не влияют на окраску мышц; основным красящим пигментом мясопродуктов является миоглобин, составляющий 90% общего содержания пигментов.Миоглобин отличается от гемоглобина по белковому компоненту. Гем — пигмент миоглобина и гемоглобина представляет собой комплексное соединение четырех пироловых ядер с центральным атомом железа. Миоглобин играет важную роль в формировании окраски мяса и мясопродуктов. Миоглобин построен из белковой части - глобина (94 %) и простетической - гема (6 %). Основой гема является протопорферин, построенный из 4-х пирольных колец, объединенных в молекулы кольцевой формы. Центральное место в молекуле гема занимает атом железа, имеющий 6 координационных связей: одну - с молекулой глобина, четыре - с атомами азота пирольных колец, шестая связь участвует в образовании комплексов миоглобина с различными соединениями (О2, Н2О, NО, СО и др.). Цвет миоглобина определяется окраской гема, который зависит от валентности железа. У нативного миоглобина железо в геме двухвалентное, белок окрашен в красный цвет. Окисление железа до трехвалентного сопровождается изменением окраски гема с образованием серо-коричневых оттенков разной интенсивности. Миоглобин способен обратимо связывать кислород без окисления гема (прижизненная функция миоглобина). Эта форма белка носит название - оксимиоглобин. Длительное воздействие кислорода и других окислителей приводит к окислению миоглобина с образованием формы пигмента - метмиоглобина, имеющего серо-коричневую окраску. Метмиоглобин может быть вновь восстановлен в миоглобин.
Количественное соотношение этих трех форм белка: нативного миоглобина (Мв), оксимиоглобина (МвО2) и метмиоглобина (МеtМв) определяет цвет мяса. Установлено, что при содержании МеtМв больше 50 % от общего количества Мв в мясе цвет его становится серо-коричневым. Содержание миоглобина в мышечной ткани зависит от вида мяса, анатомического происхождения мышц, что объясняется различиями в интенсивности их прижизненной физической нагрузки. Таким образом, цвет мяса и его интенсивность зависят от концентрации миоглобина в мышечной ткани и от количественного соотношения различных форм этого белка. Так как окраска мяса может изменяться под влиянием различных факторов, для ее стабилизации используют специальные технологические приемы. Миоглобин взаимлодействуя с нитритом натрия способен сохранять свою окраску даже при термообработке. Факторы: 1. кол-венное содержание миоглобина в мясе кол-во содерж нитрита натрия и срок хранения рас-ра. - При избытке может снизится безвредность продукта, могут образовываться канцерогены, п-нитрозоаммин и пигментные пятна.При дифиците образ окиси азота не хватит для вступления в р-цию со всеми молекулами миоглобина. 2. равномерность распределения нитрита натрия в объеме сырья 3. применение ускорителей посола (аскорбин к-ты, сахара и др0 4. Присутствие кислорода, света, темпер и продолжительности выдержки сырья. Вызывают окисление NO-миогобина до метмиоглобина 5. рН. Чем выше рН, тем медленней идёт скорость цветообразования. Оптимум 5,6-6,0 6. Поваренная соль усоряет окисление гемма с образованием метмиоглобина. 7. МБ процессы. В результате деят денитрофицир бактерий образуется азотистая к-та, окись и двуокись азота. 8. термообработка – нагрев ускоряет процесс распада нитрита натрия до окиси и его взаимодействие с миоглобином. 9. Влияние копчения на цвет. Изменение цвета обусловлено осаждением на поверхности продукта окрашенных компонентов дыма (углеводная фракция – красно-коричневый, фенолы – светло-коричневый). При взаимодействии миоглобина с СО2 – вишнёво-красный цвет. 31 Характеристика мышечных белков. Белки мышечной ткани разнообразны по аминокислотному составу, строению и св-вам. По форме белковых молекул и отношению к растворителям их делят на три группы: саркоплазматические, миофибриллярные и белки стромы. Саркоплазматические белки На их долю приходится около 40 % мышечных белков. Они имеют глобулярное строение, извлекаются из мяса путем экстракции водой. Миоген. группа белков, выполняющих фермтивные функции; составляет около 20% от суммы мышечных белков; по физико-химическим св-вам - альбумин;хорошо растворяется в воде;изоэлектрическая точка рН=6,0-6,6;температура денатурации 55-66 оС; полноценный белок. Глобулин Х. смесь белков с фермтивными функциями;составляет около 20 % от суммы мышечных белков; по физико-химическим св-вам - псевдоглобулин;из мяса экстрагируется водой;изоэлектрическая точка рН=5,2;температура денатурации 50 оС;полноценный белок. Миоальбумин. составляет 1-2 % от суммы белков мышечной ткани; по физико-химическим св-вам - альбумин; хорошо растворяется в воде; изоэлектрическая точка рН=3,0-3,5; температура денатурации 45-47 оС; полноценный белок. Миоглобин. составляет 0,5-1 % от суммы белков мышечной ткани;пигмент мышечной ткани;сложный белок хромопротеид;растворим в воде;изоэлектрическая точка рН=7,0; температура денатурации 60-70оС; полноценный белок. Миоглобин играет важную роль в формировании окраски мяса и мясопродуктов. Миоглобин построен из белковой части - глобина и простетической – гемма. Кальмодулин - белок, обратимо связывающий ионы кальция; влияет на процесс мышечного сокращения, изменение консистенции мяса при его хранении. Миофибриллярные белки (сократительные, контрактильные). По строению - это нитевидные, волокнистые белки, которые значительно хуже извлекаются из ткани, чем саркоплазматические. Растворяются в солевых растворах высокой ионной силы (например, 0,6М КСl). Миозин. составляет около 40 % от суммы мышечных белков и количественно преобладает в мышечной ткани; обладает фермтивными св-вами (АТФазная активность); выделяется из мышечной ткани солевыми растворами, при диализе экстракта осаждается; изоэлектрическая точка рН=5,4; температура денатурации 45-50 оС; полноценный белок; высокая способность к гидратации за счет наличия в молекуле большого количества полярных групп; высокая гелеобразующая и эмульгирующая способности; способен взаимодействовать с актином, образуя актомиозин. Молекула миозина построена из двух белковых цепочек, образующих «двойную спираль», так называемый «хвост» молекулы. Продолжением молекулы являются несколько коротких полипептидных цепочек, создающих глобулярную «голову» молекулы. Соединяясь «хвост к хвосту», молекулы миозина образуют толстые нити (А-диски) миофибрилл. Важнейшим св-вом миозина является его способность катализировать расщепление АТФ. АТФазная активность миозина характерна для «головы» молекулы. Актин. составляет около 15 % от суммы мышечных белков; трудно извлекается из мяса; изоэлектрическая точка рН=4,7; температура денатурации около 50-55 оС; полноценный белок; способен взаимодействовать с миозином, образуя актомиозин. Актин обладает св-вом существовать в двух формах: глобулярной (G-актин) с молекулярной массой 46000 и фибриллярной (F-ак-тин) с молекулярной массой 1500000. Обе формы могут переходить друг в друга, причем F-актин является полимеризованным, нитевидным производным G-актина с двухспиральной структурой. Каждая спираль состоит из 200-300 глобул G-актина. Этот переход осуществляется под влиянием критических концентраций ионов кальция и магния. Установлено, что из F-актина построены тонкие нити миофибрилл (I-диски). Актомиозин - это сложный комплекс, состоящий из белков актина (1/3) и миозина (2/3). При образовании актомиозина молекулы миозина прикрепляются своими «головами» к глобулам двойной спирали актина, а «хвост» располагается виде спирали вдоль оси актомиозина. В зависимости от физиологического состояния мышц миозин может находиться или в комплексе с актином, или в диссоциированном состоянии. В присутствии АТФ и в зависимости от ее концентрации актомиозин частично или полностью диссоциирует на актин и миозин. Это явление тесно связано с сокращением и посмертным окоченением мышц. Актомиозин растворим в растворах солей высокой концентрации. Температура денатурации белка 42-48 оС. Тропомиозин, тропонин, десмин - белки, участвующие в построении миофибрилл. Кроме тропомиозина (нет триптофана) - все полноценные. Составляют около 2,5-3,0 % от массы мышечных белков. Белки ядер включают три белковые фракции: нуклеопротеиды, кислый и остаточный белок. Белки стромы. Эти белки входят в состав сарколеммы, соединительнотканных оболочек, участвующих в построении мышц (эндомизий, перимизий, эпимизий). Основными белками стромы являются коллаген и эластин. В межклеточном в-ве мышечной ткани содержатся муцины и мукоиды - сложные белки глюкопротеиды. К белкам стромы относят также нейрокератины и липопротеиды. Содержание соединительнотканных белков в составе мышечной ткани зависит от вида, возраста, породы, пола, категории упитанности животного, анатомического происхождения части туши. От их количества зависит качество мяса: пищевая, биологическая ценность, органолептические св-ва (в частности жесткость). 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|