
|
|
В. Работа гальванического элемента в режиме заряда
1. Собрать электрическую цепь по схеме 2 (обратить внимание на изменение полярности при подключении амперметра). 2. Ручку резистора поставить в крайнее левое положение и оставить так до окончания измерений. 3. Включить выпрямитель и, вращая его ручку, повышать ток в цепи (на 10–12 делений амперметра). 4. Записывать показания вольтметра и амперметра в таблицу ( измерения вести до напряжения 2 В). R = 16,4∙103 Ом
На основании полученных данных
1. Рассчитать теоретическое значение ЭДС, принимая активности ионов цинка и меди равными 1, и сравнить с опытными данными. 2. Построить зарядную и разрядную вольт-амперные кривые. 3. Записать уравнения электродных процессов при разряде и заряде гальванического элемента. 4. Объяснить влияние плотности тока на напряжение гальванического элемента при его разряде и заряде.
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ 1. Что называется поляризационной кривой? 2. Какие причины вызывают поляризацию электродов? 3. Что такое коэффициент активности и как он связан с концентрацией раствора? 4. Возможно ли за счет изменения концентрации ионов меди и цинка в элементе Якоби–Даниэля изменить направление тока в нем? 5. Вычислите ЭДС свинцового аккумулятора Pb, PbSO4 │H2SO4 (aq) │PbSO4, PbO2 при 298 К и 1 М концентрации кислоты. Стандартные потенциалы электродов Pb, PbSO4 │SO42- (aq) и PbSO4, PbO2 │SO42- (aq) соответственно равны -0,359 и 1,685 В. Средний коэффициент активности H2SO4 в 1 М растворе равен 0,137. Напишите уравнения электрохимических реакций, происходящих при разряде и заряде аккумулятора. Работа № 12. Изучение окислительно-восстановительных гальванических элементов Цель работы – изучение устройства и принципа работы гальванических элементов − химических источников тока (ХИТ) с окислительно-восстановительными электродами. Знакомство с методом измерения электродных потенциалов и электрохимических характеристик ХИТ. Использование результатов электрохимических измерений для расчета термодинамических параметров реакций. Оборудование
1. Высокоомный вольтметр – рН-метр (рН-340) для измерения потенциалов. 2. Хлорсеребряный электрод сравнения. 3. Штатив с измерительными бюретками. 4. Электролитический ключ (U-образная стеклянная трубочка, заполненная КС1 и агар-агаром для увеличения вязкости раствора). 5. Штатив с двумя пробирками. 6. Два угольных (инертных) электрода. Последовательность выполнения работы 1. Получить у преподавателя вариант окислительно-восстановительного гальванического элемента. 2. Включить рН-метр для прогрева на 15 мин. 3. Приготовить два полуэлемента. Полуэлемент (окислительно-восстановительный электрод) состоит из смеси растворов, содержащих ионы одного и того же элемента, но различного заряда, т.е. валентности (окисленная и восстановленная формы), в которую погружен угольный (нерастворимый) электрод. Для приготовления раствора первого полуэлемента необходимо взять 4 мл окисленной и 2 мл восстановленной формы, а второго полуэлемента – 3 мл окисленной и 4 мл восстановленной формы. 4. Подключив электроды к рН-метру (описание прилагается к прибору), измерить (при комнатной температуре) разность потенциалов трех гальванических элементов, составленных из: а) первого полуэлемента и хлорсеребряного электрода сравнения (Ag, AgС1|КС1нас), соединив растворы электролитов электролитическим ключом; б) второго полуэлемента и хлорсеребряного электрода. в) первого и второго полуэлементов. Отсчеты производить по нижней шкале прибора, поставив переключатель пределов на 1,5 В, а «род работы» – на «+mV» (или «-mV»). 5. Записать схемы исследованных гальванических элементов и уравнения протекающих в них токообразующих реакций. На основании полученных данных 1. Рассчитать опытные значения потенциалов Еоп 1-го и 2-го окислительно-восстановительных электродов, учитывая, что измеренная разность потенциалов 2. Рассчитать по формуле Нернста теоретические значения этих потенциалов Етеор, используя справочные данные по стандартным потенциалам исследованных электродов и учитывая, что в формуле Нернста соотношение концентраций окисленной и восстановленной форм участников электродной реакции ввиду их одинаковой концентрации можно приравнять к соотношению объемов в мл. Сравнить теоретические значения потенциалов с опытными результатами. 3. Определить ЭДС исследованного окислительно-восстановительного гальванического элемента по вычисленным теоретическим значениям потенциалов окислительно-восстановительных электродов и сравнить ее с опытной величиной; 4. Записать суммарное уравнение реакции, происходящей в окислительно-восстановительном гальваническом элементе, подобрав стехиометрические коэффициенты методом составления электронно-ионного баланса.
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ 1. Какие гальванические элементы называются окислительно-восстановительными (или редокс-системами)? 2. Рассчитайте величину потенциала окислительно-восстановительного электрода С│Сr3+,Сr2+ при следующих концентрациях ионов: Сr3+ = 0,1 г-ион/л, Сr2+ = 0,1г-ион/л. 3. Определите катод и анод данной окислительно-восстановительной цепи и рассчитать ее ЭДС по стандартным значениям потенциалов: Pt│Со+2,Со+3││Sn+2 ,SnО32-│Pt .

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
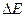 = Ео-в-Ех-с, (потенциал хлорсеребряного электрода при комнатной температуре равен 0,201В).
= Ео-в-Ех-с, (потенциал хлорсеребряного электрода при комнатной температуре равен 0,201В).