
|
|
Работа № 7. Буферные растворыЦель работы − изучение равновесия в буферных растворах – физико-химических системах с постоянным значением кислотности среды − и определение их свойств.
Оборудование 1. pН-метр (рН-340) с датчиком. 2. Пять стеклянных колб. 3. Штатив с измерительными бюретками. 4. Мерные цилиндры. Последовательность выполнения работы Опыт 1 I. Приготовить пять буферных растворов, смешав О,1 н раствор уксусной кислоты СН3СООН и О,1 н раствор ацетата натрия СН3СООNa в соотношениях, указанных в таблице:
2. Измерить рН буферных растворов на рН-метре (описание прилагается к прибору) и результаты записать в таблицу. 3. По формуле (2.34) рассчитать значения рН для приготовленных буферных растворов, записать в таблицу, сравнить с опытными значениями.
4. Построить график, отложив на оси абсцисс отношение объема соли к объему кислоты, а на оси ординат − значения рН. Опыт 2. Свойства буферных растворов. Буферная емкость I. Приготовить 90 мл буферного раствора, смешав 27 мл О,1 н раствора СН3СООН и 63 мл 0,1 н раствора СН3СООNa. Разлить раствор в три колбы по 30 мл. Раствор в первой колбе оставить без изменения, во второй разбавить в два раза, в третьей − в три раза дистиллированной водой. 2. Измерить рН всех трех растворов, результаты записать. Сделать вывод о чувствительности буферного раствора к разбавлению. 3. Приготовить 150 мл буферного раствора № 1, смешав 75 мл 0,1 н раствора СН3СООН и 75 мл 0,1 н раствора СН3СООNa. Разлить раствор в пять колб по 30 мл. Добавить в колбы 0,1 н раствор щелочи в количествах, указанных в нижеследующей таблице. 4. Измерить рН полученных растворов и результаты записать в таблицу.
5. Приготовить раствор № 2, смешав 75 мл 0,1 н раствора СН3СООН и 75 мл 0,05 н СН3СООNa. Разлить его в пять колб по 30 мл., добавить щелочи ( см. таблицу) и определить рН. Как изменится рН буферного раствора при добавлении умеренного количества сильной щелочи? 6. По полученным данным построить кривые, отложив на оси абсцисс объем приливаемой щелочи, а на оси ординат − значения рН. Определить буферную емкость по формуле β = tgα, где α − угол наклона кривой к оси абсцисс. Сравнить величины буферной емкости растворов. КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ 1. Каково практическое значение буферных растворов в природе и технике? Каков механизм их действия? 2. Какими свойствами обладают буферные растворы? Что такое буферная емкость? 3. Определите практическую значимость величин рН и рК растворов электролитов. 4. Как изменится рН раствора, если к 1.л чистой воды прибавить 0,01 моль соляной кислоты? Работа № 8. Ионообменная хроматография Цель работы – изучение метода очистки воды методом ионообменной хроматографии и изучение механизма адсорбционных процессов. Оборудование 1. Ионообменные колонки с катионитом (R-H) и анионитом (R-OH). 2. Реохордный мост для измерения электропроводности раствора. 3. Ячейка с платиновыми электродами. 4. Мерный цилиндр. Последовательность выполнения работы 1. Приготовить смесь двух окрашенных растворов солей, смешав по 25 мл 0,2 н раствора сульфата меди CuS04 и 25 мл 0,04 н раствора бихромата калия К2Сг207. 2. При помощи реохордного моста (см. инструкцию) измерить электрическое сопротивление раствора и рассчитать электропроводность как величину, обратную сопротивлению, или измерить электропроводность с помощью кондуктометра и результаты записать в таблицу, отметив окраску раствора. 3. Пропустить раствор через колонку с катионитом, предварительно слив из колонки воду. Скорость пропускания раствора − I капля в сек. 4. Измерить сопротивление и рассчитать электропроводность фильтрата, отметить его окраску. 5. Пропустить раствор через колонку с анионитом. 6. Измерить сопротивление и рассчитать электропроводность вторичного фильтрата, отметить его окраску.
7. По окончании опыта промыть колонки 50 мл 1 н раствора: а) серной кислоты H2SO4 для катионита, б) соды Na2CO3 для анионита, приливая реактив небольшими порциями. Колонки промыть несколько раз дистиллированной водой и оставить заполненными ею на 1 см выше уровня ионита. 8. Написать ионные уравнения реакций, происходящих на поверхности ионитов при работе колонок и их регенерации. 9. На основании уравнений реакций и табличных значений подвижностей соответствующих ионов (см. справочник) объяснить изменение электропроводности раствора после пропускания через катионит и анионит.
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ 1. Объясните механизм ионообменной адсорбции. Какие другие виды адсорбции вам известны? 2. Где применяется ионообменная хроматография? 3. Какие вещества могут использоваться в качестве ионитов? 4. Как изменится электропроводность и окраска раствора NiSO4 (изумрудно-зеленого цвета) при прохождении его сначала через катионит, затем через анионит? Работа № 9. Коллоидные растворы Цель работы – изучение физико-химических свойств коллоидных растворов, определение порога коагуляции и защитного числа золя гидроксида железа (III). Оборудование 1. Штатив с десятью пробирками. 2. Измерительные бюретки. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
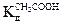 = 1,8 10-5 .
= 1,8 10-5 .