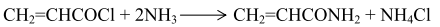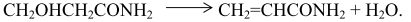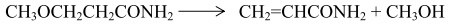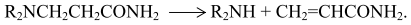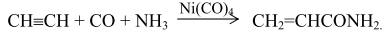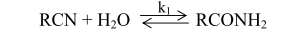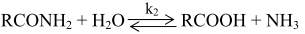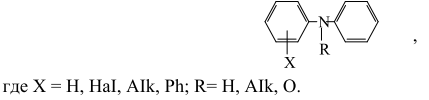|
|
Препаративные методы получения акриламида
Акриламид СН2=СН-С(О)NH2 представляет собой белое кристаллическое вещество с т. пл. 357,5 К, Акриламид впервые был получен Муре в 1893 г. медленным насыщением бензольного раствора хлорангидрида акриловой кислоты сухим аммиаком при 283 К:
Далее раствор нагревали до кипения и отфильтровывали от выпавшего осадка хлорида аммония. При охлаждении бензольного раствора выпадал кристаллический акриламид. Позднее были предложены другие методы синтеза. Так, акриламид получали взаимодействием ангидрида акриловой кислоты с аммиаком в растворе дихлорэтана или хлороформа
а также разложением β-гидроксипропионамида
Эту реакцию проводили в присутствии безводного карбоната натрия в вакууме при температуре ~ 428 К. Известны методы разложения β-метоксипропионамида над фосфатом лития при 523-773 К и над титаном при 498-673 К. При этом акриламид и метиловый спирт образуются согласно следующему уравнению реакции:
Акриламид и соответствующие амины можно получить также нагреванием β-аминопропионамида при 373-573 К:
При взаимодействии ацетилена, аммиака и оксида углерода в присутствии катализатора - карбонила никеля - также образуется акриламид:
Промышленные методы получения акриламида Акриламид и акриловую кислоту получают омылением акрилонитрила серной кислотой при 353-373 К. Выход акриловой кислоты зависит от продолжительности процесса омыления и концентрации серной кислоты. Метод сернокислотного гидролиза нитрила акриловой кислоты с последующей нейтрализацией хлорида водорода или сульфата акриламида едким кали либо водным раствором щелочи впервые реализован в 1954 г. в промышленной масштабе фирмой "Америкен Цианамид" (США). В Советском Союзе промышленный способ получения кристаллического акриламида освоен в 1961 г. По этому способу акрилонитрил омыляют моногидратом 80-85%-ной серной кислоты при 358-373 К:
Эта реакция обычно протекает с образованием небольшого количества акриловой кислоты (до 4%):
На следующей стадии происходит нейтрализация сульфата акриламида гидроксидом кальция и выделение акриламида в свободном состоянии в виде водного раствора:
Полученный при омылении акрилонитрила сульфат акриламида нейтрализуют в водной среде Са(ОН)2, аммиаком, карбонатом натрия или калия, а также соединениями щелочных или щелочноземельных металлов с добавлением воды или органического растворителя. Суспензию, образующуюся после нейтрализации, фильтруют с получением раствора мономера и соответствующих солей серной кислоты. Сернокислотный гидролиз акрилонитрила до акриламида успешно применялся в промышленности до 1970 г. В процессе получения акриламида гидролизом акрилонитрила в присутствии серной кислоты для предотвращения полимеризации мономера применяют ингибиторы, например, нитробензол, нитро-о-крезол, дифениламин, диэтиламин, дициангидрохинон. Наиболее перспективным является получение акриламида каталитической гидратацией акрилонитрила в акриламид в присутствии твердого катализатора - металлической меди. Медный катализатор может быть получен путем напыления меди в среде органического растворителя либо восстановлением внутрикомплексного соединения меди, нанесенного на оксид алюминия или активированный уголь. В результате каталитической гидратации обычно получают 10%-е водные растворы акриламида. Однако для полимеризации используют более концентрированные растворы, содержащие 30-50% (мас.) акриламида. Основным способом получения концентрированных растворов является упаривание воды, которое часто проводят при одновременном контактировании раствора с потоком воздуха: кислород является ингибитором полимеризации.
АКРИЛОВАЯ КИСЛОТА
Акриловая (пропеновая, этиленкарбоновая) кислота СН2=СН-СООН - бесцветная жидкость с резким запахом; т. пл. 285-286,5 К, т. кип. 413,9-414,6 К, Акриловую кислоту и ее соли применяют для изготовления водорастворимых полимеров и сополимеров, которые используют в качестве аппретур, связующих, диспергаторов. Примерно половина выпускаемых эфиров акриловой кислоты – акрилатов - расходуется на производство красок для внутренних и наружных покрытий. Покрытия отличаются стойкостью к истиранию, быстро сохнут и не желтеют. Лаки на основе акрилатов применяют для окраски бытовых приборов и кузовов автомобилей методом распыления. Значительную часть производимых акрилатов используют в текстильной промышленности. В бумажной промышленности полиакрилаты применяют для мелования бумаги и картона, а также для получения покрытий. Полимеры этил-, бутил- и 2-этилгексилакрилат часто в комбинации со стиролом, винилацетатом или виниловыми эфирами являются составными частями многих клеев. Сополимеры этилакрилата и этилена представляют собой ценные эластомеры. В промышленности реализуются следующие способы получения акриловой кислоты: - гидролиз этиленциангидрина (этот способ особенно широко использовался в Германии и США во время Первой мировой войны); - гидролиз акрилонитрила; - гидрокарбоксилирование ацетилена; - окисление пропилена в паровой фазе с промежуточным образованием акролеина; - гидролиз β-пропиолактона; - окислительное карбонилирование этилена. Гидролиз акрилонитрила Гидролиз нитрилов является одним из наиболее распространенных способов синтеза карбоновых кислот. Процесс катализируется кислотами или щелочами и протекает через промежуточную стадию образования амидов:
Реакцию осуществляют в водной среде при 323-353 К. Соотношение скоростей обеих реакций зависит от строения нитрилов, природы применяемого катализатора и условий проведения гидролиза. Если k1>>k2, то, несмотря на избыток воды, реакцию можно остановить на стадии образования амида. При гидролизе серной кислотой соотношение k1:k2 зависит от концентрации кислоты. Например, при гидролизе пропионитрила серной кислотой получают только пропионовую кислоту (k1:k2>100). С увеличением концентрации кислоты скорости обеих реакций становятся соизмеримыми. При обработке многих нитрилов 50%-ной и более разбавленной серной кислотой, как правило, получают карбоновые кислоты. При взаимодействии нитрилов с более концентрированными кислотами реакция часто прекращается на стадии образования амида. Таким образом, применение высококонцентрированных минеральных кислот способствует получению амида, а в области низких концентраций кислот (k2>>k1) образуются карбоновые кислоты. При получении акриловой кислоты сернокислотным гидролизом процесс проводят в две стадии: сначала синтезируют сульфат акриламида, а затем сульфат акриламида омыляют с выделением акриловой кислоты. После термообработки смеси, полученной гидролизом сульфата акриламида водой, акриловую кислоту отгоняют при пониженном давлении. Однако при этом вследствие полимеризации кислоты в паровой фазе ее значительное количество теряется. Выделение кислоты из смеси после гидролиза сульфата акриламида может быть осуществлено отгонкой вместе с органическим растворителем, добавленным в гидролизованную реакционную смесь. При этом смесь паров поступает в конденсатор, в который подают дополнительное количество воды. Образующаяся смесь разделяется на слой органического растворителя и слой водного раствора кислоты, концентрация которого регулируется количеством добавленной воды. В качестве растворителей могут использоваться о-, м-, п-крезолы, нафтол и масляные фракции керосина. Побочные реакции при гидролизе акрилонитрила.При сернокислотном гидролизе акрилонитрила, наряду с основной реакцией образования сульфата акриламида, протекают пробочные реакции, приводящие к образованию сульфата амида пропионовой кислоты, акриловой кислоты и др. Этерификацию проводят в реакторе с мешалкой, изготовленном из антикоррозионного материала - стекла, керамики, эмалированных материалов, политетрафторэтилена. На стадии этерификации в качестве побочных продуктов образуются алкили и алкоксиалкилпропионаты, диалкиловый эфир, сульфат аммония. На стадии этерификации сульфата акриламида в кислой среде возможна реакция дегидратации спирта с образованием простого эфира, который при контакте с воздухом легко превращается в пероксидные соединения, являющиеся активными инициаторами полимеризации. Ингибиторы полимеризации акриловой кислоты. При очистке акриловой кислоты ректификацией она полимеризуется, и это происходит значительно быстрее в газовой фазе, чем в жидкой, так как обычно применяемые при синтезе ингибиторы полимеризации – гидрохинон, метилгидрохинон, фенотиазин, метиленовый голубой и другие - в газовой фазе содержатся в меньшем количестве, чем необходимо для стабилизации кислоты. Образующийся полимер акриловой кислоты, не растворимый в кислоте и других растворителях, быстро заполняет дистилляционную колонну, и непрерывный процесс становится невозможным. Для предотвращения полимеризации кислоты при дистилляции добавляют различные ингибиторы полимеризации, например гидрохинон, фенол или его производные и кислород, дифениламин или его производные общей формулы
В качестве ингибитора полимеризации при перегонке акриловой кислоты может быть использован и хлорид аммония, 1%-ный раствор которого подается в верхнюю часть дистилляционной колонны. Во избежание образования полимера на поверхности аппаратов из стали при перегонке акриловой кислоты их покрывают политетрафторэтиленом, который наносят на поверхность испарителя в виде пленки. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
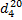 = 1,127,
= 1,127, 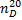 = 1,46; хорошо растворим в воде, спиртах, ацетоне.
= 1,46; хорошо растворим в воде, спиртах, ацетоне.