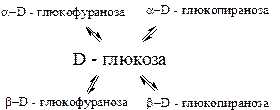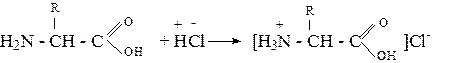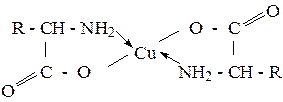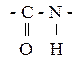|
|
Упражнения по теме «Простые сахара»1. Напишите структурные формулы: а) метил - β-D-глюкофуранозида; б) метил - a- D-глюкофуранозида; в) этил - a- D-фруктофуранозида; г) пропил β-D- фруктофуранозида. 2. Напишите реакции окисления (в разных условиях) и восстановления моноз: а) D-глюкозы; б) D-фруктозы. 3. Напишите реакции с хлорангидридом этановой кислоты: а) β-D-галактопиранозы; б) β-D-фруктофуранозы; в) a- D-глюкофуранозы. Назовите образующиеся соединения. 4. Напишите уравнения реакции D-рибозы: а) с синильной кислотой; б) с гидроксиламином; в) с ангидридом этановой кислоты. 5. Сколько металлического серебра можно получить при взаимодействии 18 г глюкозы с аммиачным раствором оксида серебра, если выход реакции составляет 75% от теоретического? 6. Напишите уравнения реакций взаимодействия избытка этановой кислоты со следующими моносахаридами: а) a- D- фруктофуранозой; б) β-D- глюкофуранозой. 7. Какое вещество получится при действии безводного метанола в присутствии HCl на: а) β-D-рибофуранозу; б) a- D-дезоксирибофуранозу. 8. Напишите уравнения образования фруктозо-3-фосфата и рибозо-5-фосфата. 9. Напишите схему перехода в щелочной среде глюкозы во фруктозу. 10. Напишите уравнения реакций образования фруктозо-1,6-дифосфата из фруктозы и фосфорной кислоты. 11. Напишите реакции гидрирования: а) D-глюкозы; б) D-галактозы; в) D-фруктозы. 12. В приведенной ниже схеме таутомерного равновесия в растворе D-глюкозы замените названия проекционными формулами:
13. Напишите схемы реакций образования озазона из глюкозы и фруктозы. 14. В чем проявляются особые свойства полуацетального (гликозидного) гидроксила по сравнению со спиртовыми гидроксилами? Напишите схемы взаимодействия (в присутствии HCl как катализатора): а) a- D-глюкопиранозы с этанолом; б) β-D-глюкофуранозы с изопропиловым спиртом; в) β-D-фруктопиранозы с бензиловым спиртом. Назовите полученные вещества. 15. Напишите реакции окисления до сахарных кислот: а) D-глюкозы; б) D-рибозы.
Аминокислоты
Аминокислотами называются соединения, в молекуле которых содержатся одновременно аминные и карбоксильные группы. Аминокислоты проявляют свойства, характерные как для кислот, так и для аминов. Кроме того, аминокислоты обладают специфическими свойствами, характерными для соединений содержащих две различные по своей природе функциональные группы. В связи с наличием аминогрупп аминокислоты дают соли с кислотами, например:
При действии азотистой кислоты на аминокислоты реакция протекает так же, как и в случае аминов. Из первичных аминов образуются спирты, из аминокислот - оксикислоты. В качестве ацилирующих агентов применяют галогенангидриды и ангидриды кислот. При алкилировании галогеналкилами образуются моно-, ди-, триалкилпроизводные. Аминокислоты, как и алифатические кислоты, образуют соли, сложные эфиры, галогенангидриды и другие производные. Особую группу составляют реакции, связанные с наличием и взаимными влиянием амино- и карбоксильных групп. Это отношение аминокислот к нагреванию. a-Аминокислоты при нагревании, отщепляя воду, образуют циклические соединения – дикетопиперазины. b-Аминокислоты при нагревании выделяют аммиак и превращаются в непредельные кислоты. g- и d-Аминокислоты легко отщепляют воду и циклизуются, образуя циклические амиды – лактамы. a-Аминокислоты при взаимодействии с гидроксидом меди (II) образуют комплексные соли:
Аминокислоты могут вступать в реакции поликонденсации с образованием пептидов и полипептидов. Повторяющаяся в полипептидной цепи группа атомов
называется пептидной, а связь C – N – пептидной связью.
Лабораторная работа
Цель работы: изучение химических свойств аминокислот Реактивы и оборудование: гликокол – 0,2н, метилрот – 0,2%, CuO – порошок, NaOH – 2н, HNO3 – 2н, NH4OH – 2н, Pb(CH3COO)2, формалин 40%, тонкие стеклянные капилляры, пробирки и спиртовки.
Опыт 11.1 Отсутствие кислой реакции у глицина Поместить в пробирку 3 капли 0,2 н раствора аминоуксусной кислоты и добавить 1 каплю 0,2% раствора индикатора метилрот. Убедитесь в том, что аминокислота не имеет кислой реакции. Зона перехода от красной окраски к желтой для метилового красного находится при рН 4,4 - 6,2. Объяснить отсутствие кислой реакции у глицина и написать схему реакции. Опыт 11.2 Образование комплексной медной соли глицина Поместить в пробирку очень небольшое количество (на кончике стеклянной лопатки ) окиси меди (II). Добавить 3 капли 0,2н. раствора глицина и нагреть над пламенем спиртовки. Дать отстояться избытку черного порошка окиси меди, обратить внимание на образование темно-синего раствора медной соли глицина. Опыт показывает, что, несмотря на отсутствие свободного водорода карбоксильной группы, глицин способен образовывать медную соль. К отстоявшемуся синему раствору (не отделяя его от черного осадка) прибавить I каплю 2н. раствора NaОН. Выпадение осадка гидрата окиси меди (II) не происходит. Сделать необходимый вывод и написать формулу этого соединения. Опыт 11.3 Действие формальдегида на аминокислоты. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|