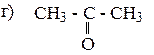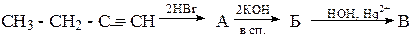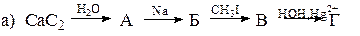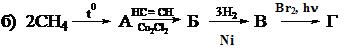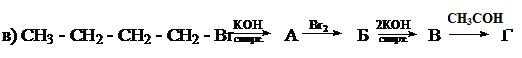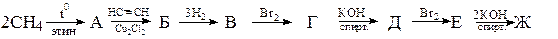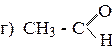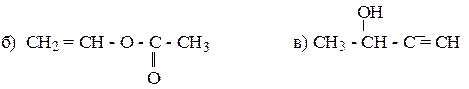|
|
Упражнения по теме «Алкины»1. Из метана получите пропин. 2. Из этана получите этин, не прибегая к реакции дегидрирования. 3. Из этина получите 2-хлорбутадиен-1,3. 4. Напишите реакции гидратации для следующих углеводородов: а) этин б) бутин-1 в) пропин 5. Напишите для пропина уравнения реакций со следующими веществами: а) СН3ОН б) HBr в) HOH
6. Какие соединения получаются в результате следующих превращений:
7. Какие соединения получаются при гидрохлорировании следующих веществ: а) бутин-1
8. Из карбида кальция получите бутин-1. 9. Напишите формулы промежуточных и конечных веществ в следующих схемах:
10. Получите любым способом бутин-1. Напишите для него уравнения реакций: а) HBr б) KMnO4 (H2O) в) НОН г) HCOH 11. Какие соединения получаются в результате следующих превращений:
12. На этин подействуйте следующими веществами: а) СН3СН2ОН б) СН3СООН в) HCN
13. Из карбида кальция получите: а) СН2 = СН - СN
14. Из 1-бромбутана получите бутин-2. 15. Из пропанона и йодметана получите 2-метилбутин-3-ол-2.
Ароматические углеводороды
АРЕНЫ К ароматическим соединениям, или аренам, относится большая группа соединений карбоциклического ряда, молекулы которых содержат устойчивую циклическую группировку, обладающую особыми физическим и химическими свойствами. К таким соединениям относятся прежде всего бензол и его гомологи и производные. Главной особенностью ароматических соединений является равномерное распределение р-электронной плотности в молекуле. Наличие единой замкнутой системы р-электронов в молекуле – основной признак ароматичности. Ароматические соединения подчиняются правилу Э. Хюккеля: плоские моноциклические соединения, имеющие сопряженную систему р-электронов, могут быть ароматическими, если число этих электронов равно 4n+2 (где n = 0,1,2,3, и т.д.), т.е. число р-электронов может быть 2,6,10,14 и т.д.). Эти особенности обуславливают все важнейшие физические и химические свойства ароматических соединений. Например, они вступают преимущественно в реакции замещения, а не присоединения. В основном это реакции электрофильного замещения (SЕ). К ним относятся реакции галоидирования, нитрования, сульфирования, реакции алкилирования и ацилирования (реакция Фриделя – Крафтса) и др. Для ароматических углеводородов известны реакции замещения, идущие по нуклеофильному (SN) и радикальному (SR) механизмам. Однако эти реакции менее характерны для ароматических углеводородов. Ароматические соединения вступают в реакции присоединения в очень жестких условиях (гидрирование, присоединение галогенов). Гомологи ароматических углеводородов относительно легко окисляются по a-углеродному атому по отношению к бензольному кольцу.
Лабораторная работа Цель работы: изучение физических и химических свойств ароматических углеводородов. Реактивы и оборудование: 0,1н. KMnO4; 2н. H2SO4; H2SO4 конц.; Br2 в Н2О; Br2 в СCl4; бензол; толуол; нитрат аммония NH4NO3 (сухое вещество). штатив с пробирками; держатель для пробирок; газоотводная трубка; спиртовка. Опыт 2.1 Растворимость бензола в воде 1. В пробирку с 5 каплями воды добавляют 5 капель бензола и перемешивают. После стояния делают вывод о растворимости бензола в воде. 2. Отношение бензола к бромной воде. В пробирку с 3 каплями бромной воды добавляют 3 капли бензола. Содержимое тщательно перемешивают. Бензол легче воды и в ней не растворяется. Поэтому после встряхивания смеси бензола он всплывает наверх при стоянии. Нижний слой бромной воды при этом обесцвечивается. Однако такое обесцвечивание объясняется не тем, что бром присоединяется по месту двойных связей, как это наблюдалось, например, у этена, а тем, что бром лучше растворяется в бензоле, чем в воде, и поэтому переходит в верхний слой бензола, окрашивая его в желтый цвет. Это процесс физический, а не химический. 3. Отношение бензола к раствору перманганата калия в кислоте. В пробирку с 5 каплями воды добавляют 1 каплю 0,1н KMnO4 и 1 каплю H2SO4. К полученному розовому раствору добавляют 1 каплю бензола и встряхивают. Что происходит с раствором? На основе своих наблюдений сделайте выводы о реакционной способности бензола. Опыт 2.2 Окисление боковых цепей гомологов бензола В пробирку с 5 каплями воды помещают 1 каплю 0,1н. KMnO4 и 1 каплю 2н. H2SO4. Добавляют 1 каплю толуола и, энергично встряхивая, нагревают над пламенем горелки. Какие изменения происходят при нагревании? Опыт 2.3Получение динитробензола (реакция Степанова) В сухую пробирку помещают 1 лопаточку нитрата аммония (NH4NO3), растворяют его в 1 мл конц. H2SO4 под вытяжным шкафом и к охлажденному раствору добавляют 1-2 капли бензола. При хорошем перемешивании бензол растворится (иногда надо слегка подогреть). Реакционную смесь выливают в другую пробирку с холодной водой. Что при этом происходит?
Вопросы для контроля 1. Понятие ароматичности. Правило Хюккеля. 2. Классификация ароматических углеводородов. Изомерия. Номенклатура. 3. Способы получения ароматических углеводородов. 4. Химические свойства ароматических углеводородов.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|