
|
|
Распространение в природеСера, единственный известный с древности неметалл, встречающийся в природе в самородном состоянии (на территории России, Японии, США, Сицилии и т.д.). К важнейшим природным соединениям серы относятся сульфаты: Na2SO4 Получение В промышленных условиях серу получают из залежей самородной серы, из сероводорода и оксида серы (IV) (отходов коксохимического производства) и сульфидов. Полученную серу очищают перегонкой. Порошкообразную серу, образующуюся при быстром охлаждении пара, называют серным цветом. Серу высокой частоты получают перекристаллизацией из сероуглерода. Физические свойства серы Чистая сера − хрупкое кристаллическое вещество желтого цвета, хорошо растворяется в органических растворителях, особенно в сероуглероде, в воде практически не растворима. Сера существует в нескольких аллотропных модификациях: желтая ромбическая (или - октаэдрическая) устойчива при обычной температуре, моноклинная - устойчива в температурном интервале 95,5 - 119,3 °С. Эти две модификации состоят из молекул S8, которые имеют цик-лическое строение. Если расплавленную и нагретую почти до кипения серу быстро охладить получается коричневая резиноподобная, липкая и тягучая масса - пластическая сера. При обычных условиях пластическая сера малоустойчива и состоит из нерегулярно расположенных зигзагообразных цепочек S Химические свойства При низких температурах серу характеризует низкая реакционноспо-собность, при высоких температурах сера непосредственно взаимодействует со всеми элементами, за исключением азота, золота и платины. Все реакции с ее участием можно разделить на 3 группы: I) реакции окисления: а) с простыми веществами: S +O2 б) со сложными веществами: S+2HNO3конц =H2SO4+2NO 2) реакции восстановления: H2+S 3) реакции дспропорционирования: 3S 0+6KOH
Соединения серы Степень окисления –2 С водородом сера образует ряд соединений общей формулы H 2Sn, которые называют сероводородами или сульфанами. Простейший из наиболее важных представителей сульфанов H2S - сероводород. Его обычно получают при прямом синтезе из серы и водорода при повышенной температуре S+H2 В лабораторных условиях при действии кислот на сульфиды металлов : FeS+2HCl=FeCl2+H2S Достаточно чистый сероводород можно получить реакцией гидролиза сульфида алюминия : Al2S3+6H2O=2Al(OH) 3+3H2S Сероводород – это бесцветный газ, с неприятным запахом «тухлых яиц», очень ядовит, температура кипения 60 0С, температура плавления – 86 0С. Молекула Н2S имеет угловую форму, угол связи равен 920. Н2S обладает восстановительными свойствами. На воздухе горит:
2H2S+3O02=2SO2+2H2O При ограниченном доступе воздуха реакция протекает по уравнению:
2H2S+O2=2S0 В присутствии сильных окислителей H2S окисляется, в зависимости от условий реакции, до свободной серы или до сульфат-иона : -2 +6 +3 3H2S+K2Cr2O7+4H2SO4=3S0
1 Cr2O72-+6e+14H+=2Cr3++7H2O 3H2S+Cr2O7 2-+8H+=3S+2Cr3++7H2O -2 -1 +6 3H2S+4HCl+5O3 В воде сероводород довольно хорошо растворим (3 об.ч. на I об.ч.H2O при 20 °С), при этом образуется слабая двухосновная киcлота : H2S HS- Кислые соли, содержащие ион НS- называются гидросульфидами, средние соли сероводородной кислоты называют сульфидами, большинство сульфидов малорастворимы в воде (кроме сульфидов щелочных металлов и аммония) и ярко окрашены, например, CuS, NiS, РbS-черного цвета, CdS-желтого цвета, MnS - телесного, ZnS- белого цвета. Это свойство сульфидов широко используется в аналитической химии. Получают сульфиды реакциями обмена в растворе: MnCl2+Na2S=MnS NiCl2+H2S=NiS Сульфиды, как и оксиды можно разделить на кислотные , основные и амфотерные. Изменение характера сульфидов можно проследить по изменению реакции среды при гидролизе : Na2S+H2O Cr2S3+6H2O=2Cr(OH)3+3H2S. Р2S5+8HOH При взаимодействии основных и кислотных сульфидов приводят к образованию тиосолей : Al2S3+3Na2S=2Na3 AlS4. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 10H 2О - мирабилит, СаSO4
10H 2О - мирабилит, СаSO4 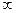 (где
(где 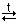 SO2
SO2 .
. +2H2O
+2H2O 3 H2S-2e=S+2H+
3 H2S-2e=S+2H+ 4HCl+3H2SO4.
4HCl+3H2SO4. H++HS- (Kg / =1 10-7)
H++HS- (Kg / =1 10-7)