|
|
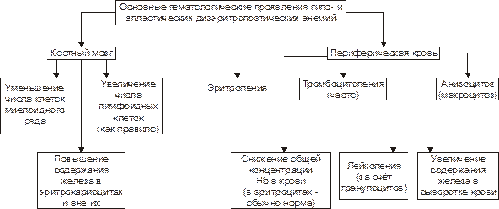
Гипопластическая и апластическая анемииГипо‑ и апластические анемии являются следствием повреждения стволовых клеток, сочетающегося с подавлением функций костного мозга. По происхождениюэти анемии подразделяют на: – первичные (наследуемые и врожденные, например, анемия Фанкони) и – вторичные(приобретенные) гипо- и апластические дизэритропоэтические анемии. Причины и патогенез гипо- и апластических анемий Причиной гипо- и апластических анемий являются факторы различной природы: – физической(например, ионизирующего облучения), – химической (чаще всего ЛС, например, левомицетина, бутадиона, иммунодепресантов, мепробамата, аминазина, цитостатиков и др.), – биологической (главным образом, вирусов, например, вызывающих гепатит, инфекционный мононуклеоз и др., а также антиэритроцитарных АТ и T-цитотоксических лимфоцитов). Так, воздействие физических факторов (например, высоких доз ионизирующей радиации) обусловливает гипоплазию костного мозга. Выраженность её зависит от дозы облучения. В основе гипоплазии кроветворной ткани лежат необратимое повреждение и гибель стволовых клеток, вплоть до их полного исчезновения, наблюдающегося при аплазии. Химические и биологические факторы (например, вирусы и ЛС) тормозят синтез нуклеиновых кислот и белка в стволовых клетках, нарушают клеточное и/или физико‑химическое микроокружение их;это ведёт к расстройствам их пролиферации, повреждению и гибели стволовых клеток. Любой из указанных механизмов (или их комбинация) обусловливает нарушение пролиферации и/или гибель стволовых гемопоэтических клеток, включая эритропоэтические. Это и ведёт к развитию гипо‑ или апластическим анемиям. Проявления. Для гипо‑ и апластических анемий характерен комплекс изменений в костном мозге и периферической крови, приведенный на рис. 22–9. Ы ВЁРСТКА Вставить файл «ПФ Рис 21 10 Основные гематологические проявления дизэритропоэтических анемий»
Рис. 22–9. Основные гематологические проявления гипо‑ и апластических дизэритропоэтических анемий.
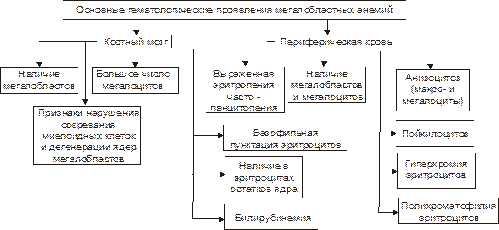
Анемия вследствие нарушения синтеза глобиновых ДНК Анемии, развивающиеся в результате нарушения синтеза глобиновых ДНК, как правило, гиперхромные макроцитарные с мегалобластным типом кроветворения. Мегалобластный эритропоэз возникает вследствие нарушения синтеза ДНК в условиях дефицита витамина B12 (цианкобаламина) или фолиевой кислоты, а также при недостаточности метионинсинтетазы и дигидрофолатредуктазы. При макроцитарной мегалобластной анемии эритроидный росток костного мозга представляют аномальные эритроидные клетки – мегалобласты. В эту группу анемий входят пернициозная анемия и другие B12‑дефицитные анемии, а также фолиеводефицитная анемия. Указанные анемии протекают тяжело и трудно поддаются лечению. Поэтому мегалобластные анемии ранее называли пернициозными (витамин B12‑дефицитными анемии, в том числе анемия Аддисона–Бирмера). Патогенез мегалобластных анемий см. в статьях «Анемии витамин В12-дефицитные», «Анемия фолиеводефицитная», «Витамин B12», «Гиповитаминоз B12», «Кислота фолиевая», «Недостаточность фолиевой кислоты» приложения «Справочник терминов» . Гематологические проявления мегалобластных анемий приведены на рис. 22–10. Ы ВЁРСТКА Вставить файл «ПФ Рис 21 11 Основные гематологические проявления мегалобластых анемий»
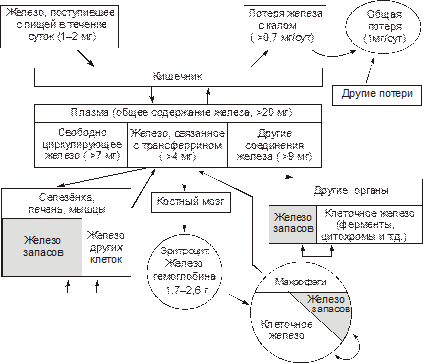
Рис. 22–10. Основные гематологические проявления мегалобластных анемий. Анемии, развивающиеся при нарушениях обмена железа К анемиям, развивающимся при нарушениях обмена железа, относят: – железодефицитные (сидеропенические) и – железорефрактерные (сидероахрестические) анемии. Обмен железа в организме Железо участвует в функционировании всех биологических систем организма. Суточная потребность в железе составляет для мужчин 10 мг, для женщин 18 мг (в период беременности и лактации – 38 и 33 мг соответственно). Общее количество железа в организме составляет 4–4,5 г. Различают клеточное железо, внеклеточное железо и железо запасов (рис. 22–11). Ы ВЁРСТКА Вставить файл «ПФ Рис 21 12 Схема обмена железа в организме»
Рис. 22–11. Схема обмена железа (Fe) в организме здорового мужчины с массой тела 70 кг. Клеточное железо составляет значительную часть от общего количества железа в организме. Оно участвует во внутреннем обмене железа и входит в состав гемсодержащих соединений (гемоглобина, миоглобина, ферментов, например, цитохромов, каталаз, пероксидазы), негемовых ферментов (например, НАДН-дегидрогеназы), металлопротеидов (например, аконитазы). Внеклеточное железо. К нему относят свободное железо плазмы и железосвязывающие сывороточные белки (трансферрин, лактоферрин), участвующие в транспорте железа. Железо запасов. Оно находится в организме в виде двух белковых соединений: ферритина и гемосидерина с преимущественным отложением их в печени, селезёнке и мышцах и включается в обмен при недостаточности клеточного железа Железодефицитные анемии Дефицит железа в организме развивается в тех случаях, когда потери его превышают 2 мг/сут. К этому Причинами этого могут быть: – снижение поступления железа в организм вследствие общего голодания, значительного уменьшения в рационе продуктов питания, содержащих железо, нарушения всасывания железа в ЖКТ (всасывается главным образом двухвалентное железо, входящее в состав гема; нарушение этого процесса развивается при хронических гастритах, энтеритах, резекциях желудка и особенно тонкой кишки); – увеличение потерь железа органзмом при хронических, повторных кровопотерях (желудочных, кишечных, маточных и др.), а также массированных кровоизлияниях; – возрастание расхода железа организмом при беременности и последующем вскармливании ребёнка (за этот период теряется в общей сложности более 800 мг железа), особенно на фоне ещё не проявляющегося клинического дефицита железа). Общая и клиническая характеристика железодефицитных анемий дана в статье «Анемия железодефицитная» (приложение «Справочник терминов»). Патогенез железодефицитных анемий Дефицит железа в плазме крови и клетках организма обусловливает снижение его содержания в митохондриях эритроидных клеток костного мозга. Это тормозит синтез гема, соединение его с глобином и, следовательно, образование Hb (рис. 22–12). Одновременно с этим нарушается синтез и других железосодержащих соединений(как в эритроидных клетках: каталазы, глутатионпероксидазы, так и в клетках паренхиматозных органов: цитохромов, миоглобина, пероксидазы, каталазы и др.). Недостаток указанных ферментов в эритроцитах приводит к снижению резистентности к повреждающему действию перекисных соединений, повышенному их гемолизу и укорочению времени циркуляции в крови.
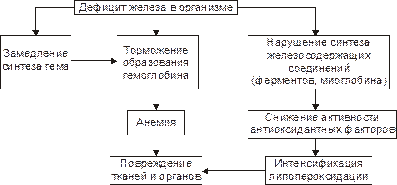
Ы ВЁРСТКА Вставить файл «ПФ Рис 21 13 Основные звенья патогенеза железодефицитных анемий»
Рис. 22–12. Основные звенья патогенеза железодефицитных анемий. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|