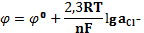|
|
Окислительно-восстановительные электродыВ отличие от описанных электродных процессов в случае окислительно-восстановительных электродов процессы получения и отдачи электронов атомами или ионами происходят не на поверхности электрода, а только в растворе электролита.
40.Окислительно-восстановительный потенциал (редокс-потенциал ) — мера способности химического вещества присоединять электроны (восстанавливаться). Окислительно-восстановительный потенциал выражают в милливольтах (мВ). Примером окислительно-восстановительного электрода: Pt/Fe3+,Fe2+ Окислительно-восстановительный потенциал определяют как электрический потенциал, устанавливающийся при погружении платины или золота (инертный электрод) в окислительно-восстановительную среду, то есть в раствор, содержащий как восстановленное соединение (Ared), так и окисленное соединение (Aox). Если полуреакцию восстановления представитьуравнением: Aox + n·e− → Ared, то количественная зависимость окислительно-восстановительного потенциала от концентрации (точнее активностей)реагирующих веществ выражается уравнением Нернста. Окислительно-восстановительный потенциал определяют электрохимическими методами с использованием стеклянного электрода с red-ox функцией и выражают в милливольтах (мВ) относительно стандартного водородного электрода встандартных условиях.
Окислительно-восстановительные электроды – представляют электрод из инертного металла, который не принимает участия в реакции и погружен в р-р содержащий ионы одного и того же в-ва с разной степенью окисления. (хингидронный) Стандартный окислительно-восстановительный потенциал Е равен потенциалу системы, в которой активность окисленной и восстановленной форм данного вещества равны единице.
41. уравнение Петерса = Нернста
где φ0 – стандартный электродный потенциал R – универсальная газовая постоянная 8,31 T- абсолютная температура n – число моль электронов F – постоянная Фарадея 96500 Men+ - активность металла 42. Элетроды сравнения и определения.Хлорсеребряныйэлектрод.обратимые электроды по назначению делятся на индикаторные (определения). Определения – называют электроды потенциал которых однозначно менятся с изменением концентрации определяемых ионов. Сравнения – электроды, потенциал которых точно известен, точно воспроизводим и не зависит от концентрации определяемых ионов. Хлорсеребряный электрод представляет собой серебрянуюпровооку, покрытую слоем AgCl, опущенную в насыщенный р-р KCl, находящийся в сосуде с микрощелью для контакта с исследуемым р-ом. Обозначается: Ag/AgCl/KCl ОВ процессом на этом электроде является раекция: Ag++e=Ag0
43.Ионоселективные электоды.Стеклянный электрод. К ионоселективным электродам относятс электроды, состоящие из ионита и р-ра, потенциал на границе фаз которых возникает за счет избирательного ионообменного процесса между фазами. Иониты обладают избирательной способностью к определенному виду ионов, находящихся в р-ре. Могут быть обратимы относительно ионов натрия, калия, кальция. Стеклянный электрод имеет обозначение: (А) Ag,AgCl/Cl- (K) Схема цепи: стекло/Н+//AgCl-/AgCl,Ag Представляет собой тонкостенный шарик из специального токопроводящего стекла (мембраны), наполненный р-ом НClконц 0,1 моль/л. В р-р HCl погружен вспомогательный хлорсеребряный электрод. Е=φк– φА φст =φст0- 0,059рН; Е=φхс0 – φст0+0,059рН 44.Потенциометрическое определение рН среды.Потенциометрический метод требует оборудования лабораторий специальными приборами - pH-метрами. Потенциометрический метод основан на измерении ЭДС электродной системы, состоящей из индикаторного электрода и электрода сравнения. Электрод сравнения иногда называют вспомогательным электродом. Наибольшее практическое применение нашел стеклянный индикаторный электрод, который можно использовать в широком диапазоне pH и в присутствии окислителей. Кроме стеклянного электрода, для определения величины pH применяются также водородный, хингидронный, сурьмяный и другие электроды. Однако широкого распространения они не получили. Е=φхс0 – φст0+0,059рН рН= Е - φхс0 + φст0 / 0.059 определение коэффициента активности осуществляют на основании измерения эдс гальванических элементов без переноса. Причина в том что для таких элементов возможно точное термодинамическое описание. Электроды следует выбирать так, чтобы один из них бал обратим относительно катиона, а другой аниона, например, если в кач-ве электролита использовать хлороводородную кислоту, то один из электродов должен быть водородным, в др хлорный или серебряный. В последнем случае: (-) (Pt)/H2/HCl//AgCl/Ag(+) Эдс такого элемента равна: Е = Е0 – RT/zF * lgaHCl/pH, учитывая, что р=1, следует: Е = Е0 – RT/zFzF * lgb² γcp ², где b – моляльность, а γcp ² средний коэффициент активности. Потенциометрическое титрование является разновидностью титриметрических методов анализа. Титрованием называют группу количественных методов анализа, основанных на измерении количества реагента, израсходованного на взаимодействие с определяемым в-ом. Реагент обычно применяют в виде р-ра с известной концентрацией – титрант. Титрант небольшими порциями доб в исследуемый р-р, пока не будет достигнуто эквивалентное соотношение реагирующих в-в. Потенциометрическое титрование – это титриметрический метод анализа, основанный на выявлении эквивалентного соотношения реагирующих в-в путем измерения О-В потенциала исследуемой системы. 45. потенциометрическое определение стандарт. Энергии Гиббса.∆Gº = - nFEº, где n – заряд, Eº - стандартнаяэдс. Расчет константы химического равновесия: К = exp(zFEº/RT) 46. Химическая кинетика её значение.Особенности кинетики гетерогенныхРеакций .химическая кинетика является разделом физической химии, занимающимся изучением скоростей и механизмов протекания реакций. Чтобы выявить механизм реакции, исследуют влияние концентраций исходных в-в, продуктов реакции, катализаторов и ингибиторов, температуры, природы растворителя, концентрации электролита и тд. Значение для фармации: действие различных лек-ыхв-в обусловливается в значительной степени скоростью реакций, происходящих в организме. При хранении лф могут протекать различные реакции, скорость которых определяет срок годности лекарств. Простые реакции – состоят из одной элементарной реакции. Сложные – из двух или более. Гомогенные реакции - хим. р-ции, протекающие полностью в одной фазе. Примеры Г. р. в газовой фазе. ГЕТЕРОГЕННЫЕРЕАКЦИИ, хим. р-ции с участием в-в, находящихся в разл. фазах и составляющих в совокупности гетерог. систему. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
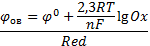
 ,
, 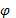 - электродный потенциал
- электродный потенциал