|
|
Лектиновый: Активация на основе распознавания микробных углеводов.подробнее: зависит от образования комплекса MBL-MASP (Mannose-binding lectine - протеаза). А он образуется при активации мбл при взаимодействии с маннозой/N-ацетилглюкозамином. Им же активируются фиколины - тоже такие коллектины. МАSP 1 и 2 соответствуют С1r и С1s классического пути, при их активации расщепляется С3, а дальше как в классическом пути 61. Эффекторные механизмы и малые фрагменты комплемента. По словам С.А.Недоспасова (41 мин, лекция 4): В результате всех 3х путей активации комплемента образуются 3 малых фрагмента комплемента, имеющие важные эффекторные механизмы: под действием С3 конвертазы образуется 1) С3а (функция: хемотаксис) 2) С3b (функция: будучи пришитой к поверхности патогена, выполняет роль опсонина(ковалентно облепляет клетку патогена), а на фагоцитах есть рецепторы к C3b, что облегчает фагоцитоз) под действием С5 конвертазы образуется не только С5b - > литический комплекс, но и 3) C5a (функции: 1. хемотаксис; 2. повышение проницаемости сосудов, что позволяет облегчить выход к очагу воспаления не только клеток иммунной системы, но и дополнительных молекул систем комплемента). 62. Три основные результата активации комплемента. ● Опсонизация, образование литического комплекса - лизис клетки, привлечение клеток врожденного иммунитета 63. В каких путях активации комплемента участвует молекула С5? Во всех, расщепление С5 одна из последних стадий, ведет к формированию литического комплекса.
64. Какой белок системы комплемента гомологичен перфорину? ● С9 65. Механизмы поддержания барьеров на границе иммунологически привилегированных органов. Иммунологически привилегированные органы - органы, при трансплантации в которые чужеродных тканей не происходит их отторжения при условии, если не происходит васкуляризации трансплантата. Пример: внутренние камеры глаз, головной мозг, семенники, яичники, волосяные фолликулы, плацента, щечные мешки хомячков :3. Изоляция. Тканевой барьер (образован эндотелиальными, мезотелиальными или эпителиальными клетками) и отсутствие лимфооттока. Изоляция никогда не бывает полной и есть T-клетки, которые могут ее преодолеть. Локальная иммуносупрессия. Цитокины (TGFβ, IL-10 ), гормоны, нейропептиды, быстрая инактивация комплемента. В органах много естественных регуляторных Т-клеток и мало АПК. На тканевом барьере FasL и TRAIL активируют апоптоз активированных лимфоцитов через CD95. Системная иммунорегуляция. Ограничение иммунного ответа, ослабленная гиперчувствительность, формирование антител не связывающих комплемент, образование адаптивных регуляторных Т-клеток. 66. Роль отрицательной селекции, дендритных клеток и регуляторных Т-клеток в естественной толерантности к аутоантигенам. Отрицательная селекция приводит к элиминации клеток, имеющих высоким сродством к аутоиммуногенам. T-клетки получают сигнал апоптоза от медуллярных эпителиальных и дендритных клеток в тимусе, В-клетки от стромальных клеток в костном мозге. Презентация АПК при отсутствии костимуляции вызывает у Т-клеток анергию (утрату иммунологической реактивности). Может также вызываться редактировании рецепторных генов (повторная перестройка). Регуляторные Т-клетки подавляют ответ эффекторных Т-клеток по контактному механизму, супрессируют цитокинами и внутриклеточными сигналами. Также возможна функциональная девиация развития CD4+ клеток в регуляторные Т-лимфоциты, которые препятствуют активации аутоспецифичных Т-лимфоцитов, если те избежали элиминации и анергии на других стадиях.
67. Механизмы предотвращения отторжения плода при беременности. 1. Синцитиотрофобласты плодов человека не экспрессируют полиморфных молекул MHC классов I и II за исключением HLA-C 2. Экспрессия клетками плаценты неклассической молекулы MHC HLA-G, которая является лигандом для ингибиторных рецепторов CTL и NK-клеток 3. Отсутствие в плаценте MHC класс II позитивных дендритных клеток 4. Экспрессия в плаценте Fas-лиганда, убивающего активированные Т-клетки 5. Плацентарный прогестерон вызывает иммунную девиацию в сторону предпочтения развития Th2-ответов. Il-4, IL-10 и TGFβ2 предотвращают развитие воспалительных Т-клеточных ответов. 6. Молекулы DAF (decay accelerating factor) и мембранный кофакторный протеин (MCP) разрушают или блокируют связывание комплемента антителами 7. Индоламин-2,3-диоксигеназа подавляет активацию Т-лимфоцитов 8. Система регуляторных Т-клеток, мобилизуемых в зоне контакта плода и матки.
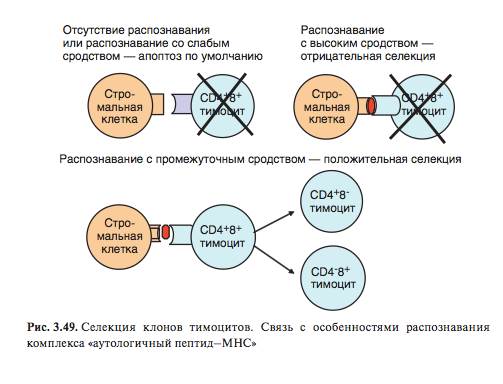
68. Механизм повреждения плода при резус-конфликте. В зависимости от человека, на поверхности красных кровяных телец может присутствовать или отсутствовать «резус-фактор» - антиген D. ● Резус-конфликт происходит при беременности резус-отрицательной (dd) матери резус-положительным (Dd) ребенком. При первой беременности никаких иммунных нарушений не происходит, но происходит сенсибилизация матери за счет проникновения эритроцитов плода и образования IgM анти-D-антител (через плаценту они не проникают). При последующих беременностях происходит реиммунизация матери D-антигеном, что приводит к синтезу IgG антител, специфичных к D-антигену и легко проникающих через плаценту. Эти антитела вызывают гемолиз эритроцитов плода и повреждение его тканей. (Ярилин) 69. Какие типы Т-клеток присутствуют в плаценте при нормальном течении беременности и какие Т-клетки связаны с прерыванием беременности? При нормальной беременности в плаценте присутствуют Th3 (естественные регуляторные Т-клетки), еще NKT и γδТ. Th1 практически нет. Увеличение количества Th1 в плаценте приводит к отторжению плода и прерыванию беременности. Также к аборту может привести снижение кол-ва регуляторных Т-клеток в плаценте. 70. Роль клеток медуллярного эпителия тимуса в формировании толерантности к собственным антигенам. Медуллярные эпителиальные клетки тимуса наравне с дендритными клетками участвуют в отрицательной селекции Т-лфц. Они экспрессируют МНС обоих классов и костимулирующие молекулы, с ними связываются тимоциты. Если тимоцит связывается с комплексом МНС-аутологичный пептид с высоким сродством, он подвергается апоптозу. Если с умеренным сродством - остается жить и может мигрировать в периферические отделы иммунной системы. 71. Органоспецифические и системные аутоиммунные патологии. Аутоимм. заболевания - появление аутореактивных антител и аутоагрессивных Т-лфц. Если антигены, на которые развилась аутоимм реакция, органоспецифичны - органоспец патология, если во многих органах - системная. Граница условна, основной смысл деления в том, что можно лечить местно, а можно системно. Органоспецифические аутоиммунные заболевания: ● Инсулинзависимый сахарный диабет типа I ● Аутоиммунные заболевания щитовидной железы (тиреоидит Хашимото, первичная микседема, тиреотоксикоз) ● Болезнь Аддисона ● Пернициозная анемия ● Псориаз ● Витилиго ● Миастения гравис ● Болезнь Крона Системные аутоиммунные заболевания ● Склеродермия ● Синдром Шегрена ● Системная красная волчанка (СКВ) ● Ревматоидный артрит
72. Трансплантационный иммунитет - индукция и механизмы. Трансплантационный иммунитет — состояние повышенной иммунной реактивности организма, возникающее в ответ на пересадку органа или ткани, взятых от другой, генетически отличающейся особи. Трансплантационная реакция сочетает цитотоксическую и воспалительную формы клеточного имм ответа, участвуют CD8+ Т-клетки (основные эффекторные клетки, ответственные за гибель трансплантата), CD4+ Т-клетки (развитие иммунного воспаления, способствующего гибели пересаженной ткани через нарушение трофики и активацию факторов врожденного иммунитета). Индукция: -Прямое распознавание: Дендритная/клетка Лангерганса донора, содержащаяся в трансплантате, мигрирует в региональный лимфатический узел и активирует Т-лфц, представляя ему МНС1. При этом основную роль в распознавании играет не антигенный пептид в МНС1, а то, что сам МНС1 другой. В прямом распознавании преимущественно участвуют CD8+. -Непрямое распознавание: молекулы МНС донора вместе с другими молекулами трансплантата эндоцитозом в АПК реципиента, АПК выставляет их в составе МНС2 и мигрирует в региональный лимфатический узел, взаимодействует с Тлфц и активирует его. В результате распознавания формируются эффекторные Т-киллеры, циркуляция и миграция в очаги воспаления, начало отторжения ткани. Также в трансплантат мигрируют NK(в трансплантате нет “родных” МНС, уничтожает) и макрофаги (на воспаление). 73. Механизмы действия иммуносупрессантов. 1. Подавление воспаления - кортикостероиды. 2. Подавление пролиферации лимфоцитов за счёт ингибирования синтеза ДНК - цитостатики. (азатиоприн, микофеноловая кислота) 3. Подавление продукции ИЛ-2 и пролиферации Т-клеток за счёт ингибирования NFAT через кальциневрин - циклоспорин А. 4. Подавление пролиферации Т-клеток за счёт ингибирования киназы mTOR - рапамицин. 5. Подавление трофики Т-клеток за счёт ингибирования сигнала от рецептора сфингозин-1-фосфата - финголимод 6. Антитела-иммуносупрессанты против CD, против рецепторов интерлейкинов, против TNFα(удаление лимфоцитов,подавление активации и пролиферации Т-клеток, подавление противовоспалительного действия TNFα и ИЛ-6)- это о чем, расшифруйте кто-нибудь[3] [4] !
74. Прямое и непрямое аллогенное распознавание. Реализуется при индукции трансплантационного иммунитета. -Непрямое распознавание: молекулы МНС донора вместе с другими молекулами трансплантата эндоцитозом в АПК реципиента, АПК выставляет их в составе МНС2 и мигрирует в региональный лимфатический узел, взаимодействует с Тлфц и активирует его. -Прямое распознавание: Дендритная кл/клетка Лангерганса донора, содержащаяся в трансплантате, мигрирует в региональный лимфатический узел и активирует Т-лфц, представляя ему МНС1. При этом основную роль в распознавании играет не а/г пептид в МНС1, а то, что сам МНС1 другой. В прямом распознавании преимущественно участвуют CD8+. 75. Группы крови человека системы АВ0 и агглютинины.0 ● Группа крови АВO – это система, отражающая наличие или отсутствие антигенов на поверхности эритроцитов и антител в плазме крови.0 =1, А=2, В=3, АВ=4 гр. ● На поверхности эритроцитов есть гликолипиды и гликопротеиды, в состав у/в остатков которых могут входить разные моносахариды. У людей, у которых есть ген А, есть спец гликозилтрансфераза и поэтому N-ацетилгалактозамин в составе углеводных остатков (агглютиноген А). У людей с геном В есть D-галактоза в составе у/в остатков (агглютиноген В). Кровь таких людей относится к группам А и В соответственно, если нет ни А, ни В - группа О, если есть оба - группа АВ. ● В норме организм вырабатывает естественные антитела (агглютинины, класс IgM, реже IgG ) против тех антигенов=агглютиногенов (А или В), которых нет на эритроцитах . То есть у лиц с гр крови А в крови будут содержаться антитела к антигенам В – обозначаются как β-агглютинин. Так как одноименные антитела и антигены (A и α, B и β) вступают друг с другом в реакцию и приводят к склеиванию эритроцитов, они не могут содержаться в крови у одного человека - есть правила переливания крови. 76. Разновидности миелоидных клеток. Цитокины, контролирующие миелопоэз. Миелоидные клетки: ● Нейтрофилы ● Эозинофилы ● Тучные клетки и базофилы ● Моноциты и макрофаги ● Дендритные клетки (есть миелоидные, есть лимфоидные) ● MDSC - myeloid-derived suppressor cells (не получившие стимул от врожденного иммунитета и вызывающие не активирующие, а супрессорное действие на CD4 T-клетки) а про тромбоциты забыли?? Гемопоэтические цитокины -относятся к цитокинам, в основном сигналящим через Jak/STAT: СSF (Colony Stimulating Factors): ● GM-CSF (гранулоцитарный-макрофагальный), М-CSF (моноцитарно-макрофагальный), G-CSF (гранулоцитарный), ● эритропоэтин, тромбопоэтин ● ИЛ-1α (гемопоэтин-1) ● ИЛ-3 (=полипоэтин, мульти СSF) ● ИЛ-5 (для эозинофилов) ● с-kit - лиганд (SCF - stem cell factor) ● Flt3-L
Негативные регуляторы гемопоэза[5] ● TNFα ● TGFβ - лучше пишите английские аббревиатуры ● хемокин MIPальфа (для ранних предшественников гемопоэза) Подтверждения красному не нашла-только в этом вопрос Это из Хаитова 77. Функции дендритных клеток Через MHC II (активация), через CD80, CD86 (выживание), через цитокины ИЛ-4, 6, 12, TGF-beta (дифференцировка). ● Переносит сигнал из тканей в лимфоузлы и другие иммунные органы. ● Презентация антигенов Т-клеткам. TLR на поверхности взаимодействуют с PAMP (+Fc-рецепторы-АТ-WHAT?ЗАЧЕМ? - ну как, опсонировали антитела патоген, он к антителам Fc рецептором присоединился и съел..) патогена, внутрь клетки идёт сигнал, клетка выносит белковые эпитопы в составе MHCII на свою мембрану (сигнал 1). Экспрессия ко-рецепторов к Т-клеткам (сигнал 2). Параллельно продуцирует сигнальные молекулы (хемокины, цитокины, сигнал 3). «Узнавание» антигена сопровождается активацией T-клеток с последующим превращением их в Т-хелперы и запуском каскада взаимодействий, конечный результат которых — выработка специфических антител В-клетками.
78. Роль Th1-клеток в активации макрофагов при воспалении. Th1, которым уже презентировала а/г дендритная клетка, взаимодействуют с макрофагами, представляющими этот же а/г. При взаимодействии формируется иммунный синапс. В результате генерируются активирующие сигналы, поступающие как в макрофаг, так и в Т-клетку.Допмеханизм активации - через действие IFNγ, который выделяют Th1. 79. Каковы функции костного мозга для иммунной системы? ● Место генерации всех предшественников- центральный орган иммунной системы ● Развитие клеток миелоидного ростка - моноциты, эозинофилы, нейтрофилы, базофилы ● Место созревания и иммунного ответа В-клеток, в частности, вторичного иммунного ответа(?) - там клетки памяти; 80. Основные направления гемопоэтической дифференцировки.
81. Какие мембранные молекулы являются абсолютными маркерами Т- и В-клеток?[6] [7] [8] ● B-клетки: BCR, CD19, CD23 (маркёр фолликулярных В2 клеток) + CD21 и CD81 (менее строго) ● T-клетки: TCR, CD3, CD28, CD44, CD45.
82. Механизмы поддержания постоянства численности лимфоцитов.[9] [10] [11] [12] [13]
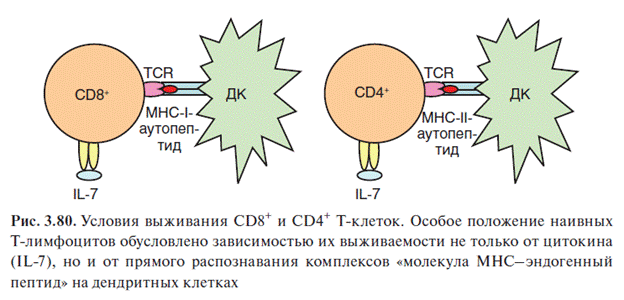
Гомеостатический контроль наивных Т-клеток реализуется с помощью как гуморальных, так и контактных механизмов. 1) Основную роль в гомеостазе наивных Т-клеток играет IL-7. Варьируя его содержание в организме, можно повышать или понижать численность наивных Т-лимфоцитов. IL-47 вырабатывают стромальные клетки вторичных лимфоидных органов, а также эпителиальные клетки тимуса. так 47 и 2) Второй механизм гомеостатического контроля Т-клеток реализуется при помощи того же процесса, что и положительная селекция тимоцитов, только происходит этот процесс не в тимусе, а в периферических лимфоидных органах, прежде всего в паракортикальных зонах лимфатических узлов. Суть его состоит в распознавании TCR αβТ-клеток молекул MHC и презентируемого ими эндогенного пептида (аналогичного пептидам, распознаваемым при положительной селекции). Для поддержания жизнеспособности и включения гомеостатической пролиферации CD8+ Т-клеток требуется распознавание молекул MHC-I, для гомеостаза CD4+ Т-клеток — молекул MHC-II. В последнем случае распознавание может осуществляться только в тимусзависимых зонах лимфоидных органов и только с участием дендритных (интердигитальных) клеток. Для CD8+ Т-клеток условия распознавания MHC-I менее жесткие: считают, что оно может происходить и вне лимфоидных органов, но обязательно с участием дендритных клеток.
83. Какой цитокин служит фактором выживания и гомеостаза В-лимфоцитов? ● IL-4, APRIL, BAFF
84. Структура и гистогенез вторичных лимфоидных органов. К ним относят лимфатические узлы, контролирующие определенные области организма, от которых к ним поступает лимфа; селезенку, под контролем которой находятся гематогенные пути распределения чужеродных агентов; лимфоидные структуры барьерных тканей — слизистых оболочек и кожи, через которые в организм проникает основная масса патогенов. В эмбриогенезе лимфатические узлы образуются в результате накопления мезенхимных клеток вокруг кровеносных сосудов. Это LTIC (Lymphoid tissue inducing cells). Наружный слой мезенхимы дифференцируется в соединительнотканную капсулу, от которой внутрь узла отходят трабекулы - перегородки. В лимфатическом узле различают корковый слой, расположенный по периферии и организованный в первичные и вторичные фолликулы, и мозговое вещество, находящееся в центре узла. Корковый слой - тимуснезависимая зона, или В-зона. Область между корой и мозговым веществом (паракортикальная территория) - тимусзависимая зона. Характерной чертой строения селезенки является наличие двух гистологически хорошо различающихся участков - красной и белой пульпы. Белая пульпа ( мальпигиевы тельца ) представляет собой скопление лимфоцитов вокруг эксцентрично расположенного артериального канала. Четких границ между белой и красной пульпой нет, и между ними происходит частичный клеточный обмен. Для понимания иммунологических процессов наибольший интерес представляют белая пульпа и пограничная область между белой и красной пульпой. Именно здесь локализуются Т-лимфоциты и В-лимфоциты , мигрирующие из центральных органов иммунной системы . Они распределяются по двум зонам: тимусзависимой, где скапливаются Т-лимфоциты вокруг пронизывающих пульпу артериол, и тимуснезависимой - места накопления В-лимфоцитов. В этой зоне хорошо различимы фолликулы с центрами размножения , которые образуются в ответ на антигенный стимул. Т-клетки, располагаясь вокруг артериол, образуют периартериальные муфты.
85. Структура и клеточный состав тимуса. Клеточный состав ● Соединительнотканная строма. ● Эпителиальный ретикулум. ● Клетки костномозгового происхождения — мигрирующие в процессе созревания лимфоциты (подавляющее большинство — Т-клетки) 86. Факторы и механизмы селекции клонов тимоцитов. В коре тимуса дважды положительные клетки (4+8+) очень чувствительны к апоптозу из-за низкой экспрессии антиапоптотических факторов Bcl-2 и Bcl-XL. Сигналом для выживания служит +селекция, при которой на основании взаимодействия ++ клеток со стромальными отбираются клетки с низким сродством TCR и MHC и они в апоптоз. Остальные живы-здоровы и по мере продвижения к кортикомедуллярному слою у нас уже отобраны 4-8+ и 4+8- клетки. В передачу сигнала вовлечены MAPK (на cFOS) и Ca2+ на NFAT. В медуллярном слое эпителиальные медуллярные клетки и ДК, экспрессирующие CD80, 86 и 40 отбирают клонов с очень высоким сродством TCR и MHC и через Nur77 сигнал апоптозируют их. Маркер отрицательной селекции - киназа MINK и передача сигнала обычно заканчивается на cJun. Ремарка: выживание CD4+ с высоким сродством возможно, если есть костимуляция IL-2, которая приводит к экспрессии FoxP3 и развитие из этой клетки Treg. ● Мораль: +селекция если низкое сродство за счет тестирования стромальными клетками CD4+8+ Tлимф, - если очень высокое за счет тестирования ДК 4+8-/4-8+. 87. Субпопуляции Т-лимфоцитов и корецепторы. корецепторы на картинке - это CD всякие У NKT: TCR–CD3 и типичные молекулы NK-клеток CD56 и CD16, а также ингибирующие (KIR, NKRG2) и активирующие (NKG2D) рецепторы.
88. Экспрессия каких молекул определяет названия «двойные отрицательные тимоциты» и «двойные положительные тимоциты»? CD4, CD8
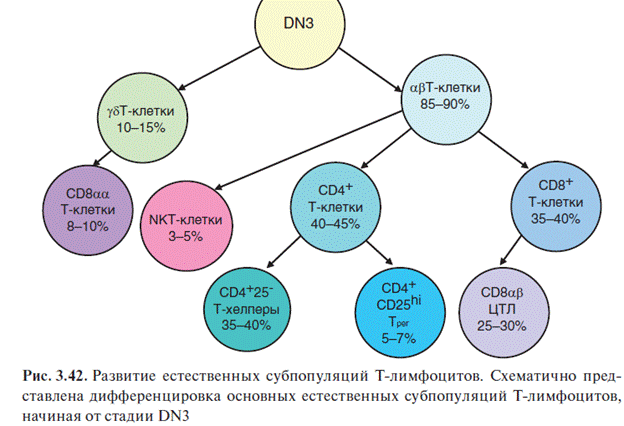
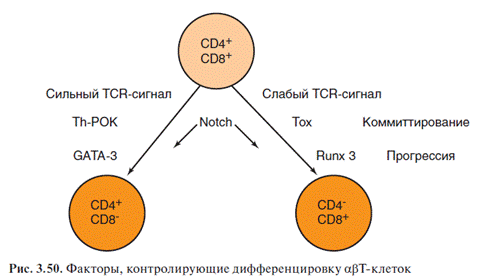
89. Выбор путей развития тимоцитов на стадии DN. DN- это дважды негативные. То есть у них нет CD 8+ и CD4+. В квадратиках на картинке факторы, направляющие дифференцировку. В конце DP - дважды положительные - дифференцируются на CD 8+ и CD4+.
http://www.nature.com/ni/journal/v11/n8/fig_tab/ni.1887_F1.html
90. Выбор путей развития тимоцитов на стадии DP.
91. Процессинг антигенов как условие Т-клеточного распознавания. Структура комплекса антигенного пептида с молекулами MHC. альфа-бета Т-клетки не могут распознавать целые АГ, их распознавание основано на принципе “чужое в контексте своего”. Поэтому необходимо расщепление АГ до линейных пептидов в протеасомах и представление их в составе МНС. Перед презентацией многие антигены сначала щепятся в протеасомах, и детерминанта, которая затем представляется Т лф, становится очень маленькой. Т клетки распознают поверхность МНС+ кусочек АГ. АГ в составе МНС располагается вдоль двух альфа-спиралей, образующих желобок, дно которого - бета-слои. в МНС 1 полость замкнута, поэтому можно презентировать только очень короткие участки, а в МНС 2 - ограничена только с боков, поэтому можно презентировать бОльшие молекулы куски АГ. МНС без АГ нестабильны Корецепторы Т-лимфоцитов связываются с МНС разных классов - МНСII+СD4, МНСI+СD8. 92. MHC-рестрикция и ее молекулярный механизм. Особенность Т-лимфоцитов, называемая MHC-рестрикцией - Т-лимфоциты одного организма не распознают МНС другого. Она определяется специфичностью их рецепторов, взаимодействующих с антигеном только в том случае, если он связан молекулой главного комплекса гистосовместимости (MHC). Это обуславливается высоким разнообразием Т клеточных эпитопов. Т-лимфоциты проходят позитивную селекцию на молекулах MHC, которые у каждого индивидуума свои, и пептидах, которые способны с этими аллелями связаться. У другого индивидуума набор молекул MHC будет другой, пептиды получатся тоже другие, в результате репертуар специфичностей зрелых лимфоцитов также будет отличаться. При наличии чистых линий при попытке применить Т-клетки одного индивидуума против зараженных клеток другого Т-клетки не будут распознавать антиген в составе МНС. Будет абсолютная рестрикция: Т-клетки одной линии вообще "не видят" клеток-мишеней другой линии, несмотря на то, что они заражены тем же самым вирусом.В случае гетерогенной естественной популяции возможны частичные перекрывания.
93. Роль молекул MHC в адаптивном иммунитете. 1)В иммунных ответах на обычные чужеродные антигены они выполняют функцию презентации антигенных пептидов Т-лимфоцитам. 2)Взаимодействие с собственными молекулами МНС необходимо для развития Т-лимфоцитов в тимусе.В ходе этого взаимодействия формируется репертуар Т-лимфоцитов, способный различать “своё” и “чужое”. 3)В трансплантационном иммунитете они (молекулы МНС) являются сильными трансплантационными антигенами,вызывающими интенсивный иммунный ответ.Наиболее сильный ответ развивается при аллельных различиях донора и реципиента по молекулам МНС класса1 +МНС класса 2.Развивается острое отторжение трансплантата. 4)В течение жизни организма они поддерживают гомеостаз Т-лимфоцитов.
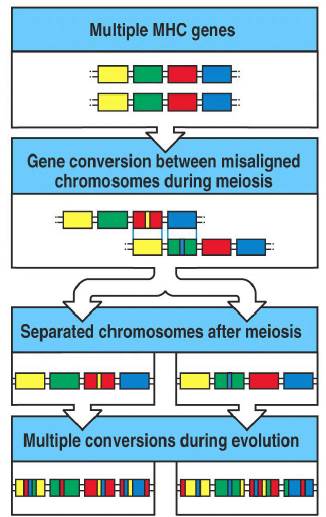
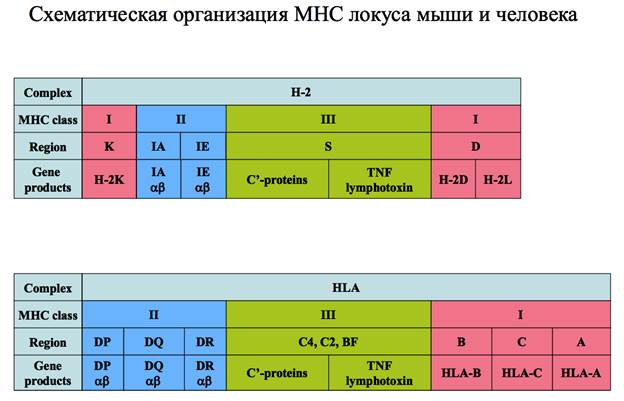
94. Генетическая структура локуса MHC. МНС комплекс находится в 17 хромосоме у мышей, и в коротком плече 6 хромосомы у человека. Дальше будет все про человека, но у мыши похоже. МНС I располагается на 3’ конце области, а МНС II на 5’. между ними располагается МНС III, который не имеет никакого отношения к распознаванию, и кодирует нек. элементы системы комплемента, и был так назван исторически. существует по 3 гена главных аллелей MHCI (A,B,C), соответственно, каждая особь может экспрессировать максимум 6 разных молекул MHCI МНСII тоже разнообразна. есть DR,DP и DQ гены, кодирующие альфа и бета цепи. в целом разнообразие бета цепей выше, чем альфа. Важно, что разнообразие МНС - в популяции, а у человека не больше двух вариантов для каждого гена ( потому что хромосомы всего две). Важно: разнообразие обеспечивает генная конверсия!
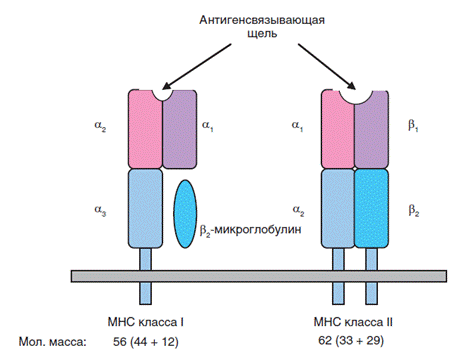
95. Особенности строения молекул MHC I и II классов. МНС I состоит из молекулы, состоящей из альфа цепи ( альфа 1, 2, 3) и бета-2-микроглобулина кодируемого не в МНС локусе. МНСII состоит из двух цепей - альфа (альфа 1 и 2) и бета (бета 1 и 2). Заякорены короткими трансмембранными участками. Альфа 2 и бета 2 участки МНСII родственны иммуноглобулинам, а Альфа 1 и бета1 - альфа 1 и 2 МНСI
96. На молекулах MHC какого класса фрагменты вируса презентируются цитотоксическим Т-лимфоцитам? ● МНС I
97. Биологический смысл аллельного разнообразия MHC. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|