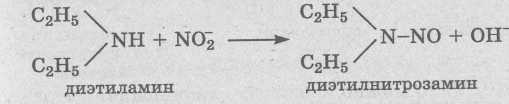|
|
Характеристика ферментов, катализирующих метаболизм ксенобиотиковО термине Метаболизм ксенобиотиков в организме иногда называют детоксикацией. Однако, превращения некоторых ксенобиотиков сопровождаются образованием еще более токсичных веществ. Поэтому более правилен термин «биотрансформация». Реакции биотрансформации ксенобиотиков напоминают процессы, происходящие с эндогенными соединениями, и катализируются соответствующими ферментами. Общее представление о ферментах • Все ферменты имеют белковую макромолекулярную природу. • На поверхности молекул белков-ферментов располагаются активные и регуляторные центры. • Благодоря особенностям структурной и пространственной организации молекул ферменты обладают высокой специфичностью к превращаемым веществам−субстратам. • Реакция начинается после того, как образуется фермент-субстратный комплекс.
Для образования такого комплекса необходимо строгое геометрическое соответствие форм молекул субстрата и фермента (пространственных и зарядовых геометрий). При взаимодействии веществ главный ограничитель скорости химического процесса − энергетический барьер. Действие фермента сводится к снижению энергетического барьера за счет образования фермент-субстратного комплекса При образовании фермент-субстратного комплекса на активных центрах фермента • может растянуться и ослабиться химическая связь между атомами субстрата; • может возникнуть такая пространственная конфигурация субстрата, которая облегчит переход к новому веществу; • может произойти сближения реагирующих молекул субстрата и принятие ими нужной ориентации. В регуляторных центрах ферментов не происходят каталитические превращения. Эти центры замедляют или ускоряют ход процесса. В самом простом случае продукт при избытке присоединяется к активным центрам и предотвращает синтез новых продуктов. Когда продукта мало, регуляторные центры высвобождаются и перестают тормозить работу активных центров Особую группу ксенобиотиков представляют самораспадающиеся соединения (важно для лекарственных препаратов), т.е. спонтанно разрушающиеся в организме с образованием продуктов, не обладающих биологической активностью в данных концентрациях. Распад таких соединений не зависит от наличия ферментов, что важно в тех случаях, когда наблюдаются нарушения функций отдельных органов (печени, почек). Наиболее широко в живых организмах представлены ферменты и ферментативные системы, катализирующие процессы окисления, восстановления, гидролиза ксенобиотиков и синтеза метаболитов, содержащих эндогенные соединения. В клетках высших организмов наиболее активной системой в метаболических превращениях чужеродных соединений являются микросомные фракции. Микросомы − пузырьки−артефакты, образующиеся при разрушении клеток и представляющие собой продукты разрушения мембранной системы ЭПР.
Реакции окисления В катализе окисления ксенобиотиков особое место принадлежит микросомным оксигеназам (монооксигеназам), катализирующим внедрение в молекулу ксенобиотиков активированного кислорода. Основной компонент монооксигеназных систем − терминальная оксидаз — цитохром Р-450, относящийся к гемопротеидам. Различают микросомальную, митохондриальную и бактериальную монооксигеназные системы цитохрома Р-450. К наиболее важным реакциям окисления относятся: 1. Окисление спиртов и альдегидов. Осуществляется алкогольдегидрогеназой, альдегидоксидазами и др. ферментами. 2. Окисление аминов. Например, а) реакция диэтиламина с нитритом в кислой среде желудка, в результате которой образуется канцероген — диэтилнитрозамин:
б) реакция окисления симазина с образованием канцерогенного продукта:
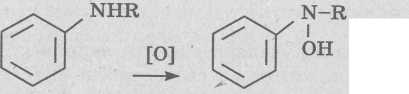
Нитрит натрия ранее широко использовался в качестве консервирующей добавки к пищевым продуктам. 3. Окисление ароматических аминов. Эти вещества подвергаются N-гидроксилированию с участием оксигеназ, что может приводить к появлению канцерогенных продуктов:
4. Окисление ароматических алкилзамещенных соединений. Они обычно расщепляются между атомами C1 и С2 боковой цепи с образованием соответствующей ароматической кислоты.
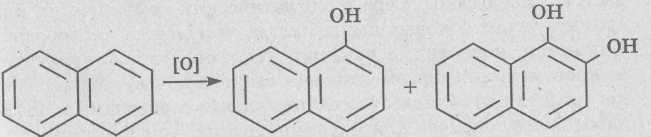
Эти реакции происходят с участием микроорганизмов, а также в растениях. У различных видов микроорганизмов удалось установить многочисленные реакции разрыва бензольного кольца. Такие процессы весьма избирательны. Универсальность почвенной экосистемы в превращениях различных классов соединений определяется разнообразием популяций микроорганизмов в почве. 5. Гидроксилирование кольцевых систем. Алициклические кольцевые структуры гидроксилируются легче, чем ароматические (одна из причин высокой токсичности бензола, поскольку он тяжело окисляется до фенола). При гидроксилировании в орто-положении могут образовываться канцерогенные метаболиты. В реакциях гидроксилирования могут участвовать ферменты микросом. Катализируют реакции оксигеназы. · Алифатическое гидроксилирование: RCH3 → RCH2OH.
· Ароматическое гидроксилирование:
6. Ароматизация алициклических соединений Происходит в случае окисления циклогексанкарбоновых кислот с четным числом СН2-групп в боковой цепи с участием митохондрий. Конечный продукт — бензойная кислота.
7. При реакциях окисления с участием фермента эпоксидазы образуется эпоксидное кольцо (реакция эпоксидации):
Например, в результате окисления (эпоксидации) пестицида альдрина получается токсический эпоксид дильдрин. Эпоксиды высокотоксичны и обладают мутагенными и канцерогенными свойствами. Эпоксидации подвергаются многие ароматические соединения.
8. Окисление или окислительное замещение органической серы Гетероциклическая сера окисляется в сульфоксиды или дисульфоны. Сера в алифатических комбинациях или ароматических боковых цепях иногда замещается кислородом. Например, инсектицид паратион (тиофос) метаболизируется микросомальными ферментами (а также в почве) в параоксон, который также обладает инсектицидными свойствами и почти вдвое более токсичен для млекопитающих, чем паратион:
Превращение связи Р = S в связь Р = О приводит к повышению токсичности продуктов.
9. Окислительное дезалкилирование О- и N-атомов. Наиболее часто дезалкилированию подвергаются ксенобиотики следующих классов: ü динитроанилины (гербициды трифлурамин, динитрамин и др.), ü фенилмочевины (гербициды хлороксурон, диурон, монурон, флуометурон, линурон и др.), ü симметричные триазины, ü фосфорорганические соединения, ü алкиламины и др. Эти реакции осуществляются оксигеназами микроорганизмов, а также клетками печени. Необходимо подчеркнуть, что при окислительной биотрансформации ксенобиотиков нередко образуются более токсичные или канцерогенные соединения. Так, гербицид симазин окисляется в опасный канцероген. Таким образом Широкий круг реакций биологического окисления может быть сведен к одному общему механизму − к гидроксилированию. Для всех этих реакций требуется восстановленный кофермент НАДФ.Н или НАД.Н и кислород.
Реакции восстановления.
1. Восстановление альдегидов и кетонов в спирты под действием алкогольдегидрогеназ. Однако, ацетон может прямо входить в цикл аэробного метаболизма через ацетоацетат и ацетил-КоА.
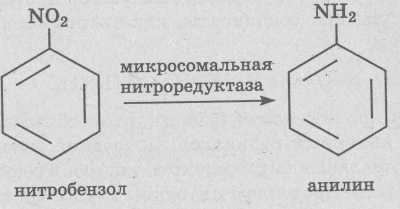
2. Восстановление нитро- и азогрупп. Целый ряд ароматических нитросоединений, например нитробензол, паранитробензойная кислота и хлорамфеникол, восстанавливаются в амины нитроредуктазами, находящимися в микросомальной и растворимой фракциях печени и почек:
Возможно образование продуктов, содержащих гидроксиамино- или нитрозогруппы. Образование нитрозосоединений представляет большую опасность для биосферы, так как при этом может образовываться вещество, обладающее сильным мутагенным и/или канцерогенным действием. Например, при биотрансформации гербицида трифлуралина происходит образование нитрозосоединения, обладающего канцерогенным действием:
Нитроредуктазы малоспецифичны к субстратам и восстанавливают нитрогруппы практически всех ароматических нитросоединений. Ароматические нитросоединения восстанавливаются также ферментами слизистой оболочки кишечника и его микрофлорой. Азосоединения в организме животного подвергаются восстановлению в гидроазосоединения, а затем подвергаются восстановительному расщеплению, образуя две молекулы ароматических аминов.
3. Восстановление N-оксидов. Процесс катализируется N-oксидоредуктазами, которые обнаружены в микросомальной и растворимой фракциях клеток, а также в митохондриях.
4. Восстановление дисульфидов (R - S - S - R1). Они расщепляются с образованием тиолов. 5. Восстановление двойных связей. Двойные связи некоторых алифатических или алициклических соединений могут становиться насыщенными (например, у циклогексана). Простейшие алкены и алкины часто экскретируются без изменений их структуры. 6. Дегидроксилирование. 7. Восстановление ароматических циклов анаэробными микроорганизмами.
Гидролиз
Сложные чужеродные вещества могут гидролизоваться рядом гидролитических ферментов (гидролаз), находящихся в печени и плазме крови. В зависимости от субстратной специфичности ферменты, катализирующие данные процессы, относятся к различным группам. 1. Гидролиз эфиров карбоновых кислот катализируются эстеразами и существляется в организме как животных, так и человека. Гидролиз эфирной связи — начальный этап микробиологической деградации многих пестицидов:
2. Гидролиз амидов, гидразидов и нитрилов происходит в дополнение к другим реакциям биотрансформации. Гидролиз амидной связи описан при изучении микробиологической деградации фениламидных пестицидов и происходит с участием амидаз:
3. Гидролиз фосфорорганических веществ. Участвуют ферменты, атакующие эфирные связи или действующие на ангидриды кислот. Реакция гидролиза эфира фосфорной кислоты проходит по следующей схеме:
Среди гидролитических ферментов особое место занимают Р-глюкуронидаза и сульфатаза. Р-глюкуронидаза катализирует расщепление эфирных и сложноэфирных связей глюкуронидов и эфирных связей серной кислоты. Фермент обнаружен в микросомах и лизосомах печени, почках, селезенке, пищеварительном тракте и половых железах животных. Сульфатаза, гидролизирующая эфирсульфат, находится в микросомах печени человека и животных. Реакции конъюгации
К конъюгационным относятся процессы биосинтеза, в результате которых из ксенобиотиков или их метаболитов и эндогенных продуктов (глюкуроновой кислоты, ацетилсульфата, глицина и др.) образуются сложные вещества. фермент RX + эндогенное соединение −−−−−−−> коньюгат Образование конъюгатов − это энергозависимые процессы, подразделяющиеся на две группы в зависимости от природы активных промежуточных продуктов реакций: 1) процессы, в результате которых образуются активированные конъюгирующие агенты (реакции метилирования, ацетилирования, образования глюкуронидов, гликозидов и сульфатов); 2) процессы, для которых характерно образование активированного субстрата, например, аминокислотная конъюгация.
Реакции конъюгации катализируются ферментами трансферазами, переносящими заместитель в другое соединение. В определенных ситуациях реакции конъюгации считаются высокоэффективными путями снижения токсичности некоторых ксенобиотиков. Наиболее изучены следующие реакции конъюгации: 1. конъюгация ацетата при участии ацетил-КоА с некоторыми ароматическими аминами и сульфонамидами;
2. конъюгация глицина с бензойной кислотой, описанная Келлером в 1842 г., — одна из первых изученных реакций биотрансформации:
3. конъюгация трипептида глутатиона. Глутатион — эффективный конъюгирующий агент для конденсирования кольцевых систем — нафталина, антрацена, фенантрена.
Многие ксенобиотики выделяются в мочу в виде меркаптуровых кислот. Такие конъюгаты образуются в результате взаимодействия ксенобиотиков с глутатионом.
4. Метионин и этионин участвуют в реакциях алкилирования. Таким образом метилируется пиридин, пирогаллол; сульфиты, селениты, теллуриты подвергаются биологическому метилированию и превращаются в летучие диметильные производные.
5. Орнитин используется при детоксикации бензойной кислоты в организме рептилий и птиц, а аргинин — в организме членистоногих.
6. Глутамин у приматов используется для конъюгации фенилуксусной кислоты и некоторых ее гетероциклических аналогов.
7. Рибоза и глюкоза конъюгаты глюкозы особенно широко представлены в растениях, у моллюсков и насекомых. Способность растений гликолизировать ксенобиотики была открыта в 1938 г. Д. Миллером. Гликозирование является основным путем детоксикации растениями чужеродных фенолов. Среди млекопитающих глюкозидная конъюгация встречается в организмах кролика, мышей, крыс и человека.
8. Конъюгация ксенобиотиков с глюкуроновой кислотой (образование глюкуронидов) — наиболее важный механизм детоксикации ксенобиотиков. В реакции участвует активная форма глюкуроновой кислоты — уридиндифосфоглюкуроновая кислота (УДФГ). Катализирует процесс уридиндифосфатглюкуронозилтрансфераза (УДФГТ), локализованная в мембранах ЭР гепатоцитов, легких, кожи, кишечника, почек. Глюкуроновая кислота (6-карбоксильное производное глюкозы) используется для конъюгации с ксенобиотиками у большинства позвоночных и всех млекопитающих. Она имеет преимущество перед глюкозой как детоксицирующий агент, поскольку содержит ионизируемую группу. Конъюгации подвергаются спирты, фенолы, карбокислоты, амины, гидроксиламины, карбамиды, сульфонамиды и тиолы. 9. Лигнин. В растениях удалось обнаружить новый тип конъюгатов — нерастворимое конъюгаты с лигнином. С ним могут ковалентно связываться молекулы пестицидов 2,4-Д (дихлорфеноксиуксусная кислота), пентахлорфенола, 3,4-дихлоранилина. 10. Сульфатная конъюгация (сульфатирование) — один из древних видов биотрансформации. В нее вступаю фенолы, спирты, ароматические амины, гидроксиламины, некоторые стероиды. Происходит с участием сульфатаденилтрансферазы, аденилсульфаткиназы, и др. ферментов. В некоторых случаях сульфатная конъюгация приводит к появлению канцерогенного вещества, взаимодействующего с нуклеиновыми кислотами. Описаны фосфатная конъюгация, реакция ксенобиотиков с глицинтаурином и формилом и др. конъюгации. Необходимо подчеркнуть, что конъюгирование является обезвреживанием вещества лишь для данного организма.
Дегалогенирование
К хлорсодержащим ксенобиотикам относятся многие персистентные поллютанты, в том числе пестициды, а также ряд природных метаболитов низших растений. Выделяют следующие реакции дегалогенирования: 1. Гидролитическое дегалогенирование хлорированных алифатических кислот, при деградации ароматических пестицидов. Например, гербицид 2,4-Д деградируется почвенными бактериями.
2. Восстановительное дегалогенирование − это реакция замещения атома галоида на водород. Например, многие бактерии, грибы, водоросли таким образом трансформируют ДДТ в ДДД. Могут образоваться интермедиаты, токсичные для клеток. 3. Окислительное дегалогенирование. Реакции этого типа подразделяются на: ü дегидрогалогенирование (при метаболизме ДДТ); ü окислительное дегалогенирование с образованием двойной связи; ü дегалогенирование — гидроксилирование с участием молекулярного кислорода.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|