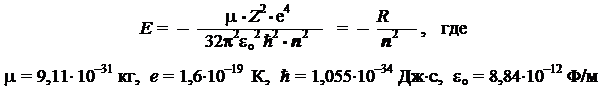|
|
Физические характеристики атома водородаВолновая функция содержит в себе информацию о характере движения электрона в атоме. Поэтому, располагая волновой функцией, с помощью некоторой стандартной процедуры можно извлечь исчерпывающую (с механической точки зрения) информацию о физических свойствах атома, обусловленных движением электрона. Эти характеристики атома целесообразно подразделить на два типа — динамические и пространственные. Наблюдаемые первого типа отличаются тем, что их операторы коммутируют с гамильтонианом. Следовательно, для каждого стационарного состояния атома эти наблюдаемые имеют постоянные во времени и точно определенные значения (т.е. выражаемые одним числом, а не функцией распределения). Динамические наблюдаемые Числовые значения динамических наблюдаемых А можно вычислить по стандартному уравнению: А Y(r, q, j) = А Y(r, q, j) т.е. они представляют собой собственные значения соответствующих квантовомеханических операторов А. Количество независимых наблюдаемых этого типа равно числу механических степеней свободы атома, которое для атома водорода равно трем. Соответственно, фундаментальный набор включает три наблюдаемых: энергия—Е, величина (модуль) вектора орбитального момента — | L|, проекция вектора орбитального момента на ось z — Lz. Можно получить простые соотношения, позволяющие выразить значения наблюдаемых этого типа через величины квантовых чисел. Так, значение энергии (в системе СИ) задается формулой:
Следует обратить внимание на то, что энергия зависит только от квантового числа n. Кроме того, энергия имеет отрицательное значение, так как отсчитывается от уровня, соответствующего электрону, удаленному от ядра на бесконечное расстояние. Константа R = 13,6 эв = 2,18×10–18 Дж называется ридбергом и используется в качестве единицы энергии. Таким образом, стационарные состояния атома водорода распределены по системе дискретных энергетических уровней, сходящихся к некоторому пределу, соответствующему ионизации атома.
Эта сходимость обусловлена гиперболической формой стенок потенциальной ямы, в которой вынужден двигаться электрон. Следует отметить характерную особенность кулоновской потенциальной ямы — отсутствие "дна". Наиболее отрицательное (наименьшее) значение энергии электрона (при n = 1) можно рассматривать как нулевую энергию, характерную для всякой системы, где доступный для движущейся частицы объем пространства ограничен. Энергетические уровни вырождены с кратностью n2. (Подобная независимость энергии от величины числа l имеет место только для одноэлектронных атомов и не наблюдается для многоэлектронных атомов.) Переходы между энергетическими уровнями можно легко наблюдать экспериментально в виде атомных спектров (эмиссионных или абсорбционных). Полосы в таких спектрах составляют систему нескольких серий:
где числа n1 и n2 соответствуют начальному и конечному состояниям. Модуль вектора орбитального момента можно вычислить по формуле:
Поскольку возможные значения числа l ограничены величиной (n – 1), то для каждого энергетического уровня вектор L может иметь только n значений модуля: | L | = 0, 1, 2, …, (n – 1). Модуль вектора L связан с пространственным распределением плотности электронного облака и числом узловых поверхностей, разделяющим облако на отдельные фрагменты. Величина проекции вектора L на ось z, характеризующая пространственную ориентацию этого вектора, задается магнитным квантовым числом: Lz = mh = 0, ± h , ±2h , ±3h ... ±lh Следует подчеркнуть, что ни энергия, ни узловая структура электронного облака не зависят от величины проекции Lz. Поэтому суперпозиционные состояния типа: Yn,l = C1Yn,l,l + C2Yn,l, l–1 + . . . .+ C2l Yn,l, –l+1 + C2l+1Yn,l,–l в которых смешаны состояния с одинаковыми числами n и l, но с разными значениями числа m (от +l до –l), также являются собственными для операторов H и L2. Однако при наложении внешнего магнитного поля такие суперпозиционные состояния разрушаются и переходят в одно из состояний с определенным значением Lz. При этом наблюдается расщепление вырожденного в отсутствие внешнего поля уровня энергии:

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|