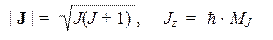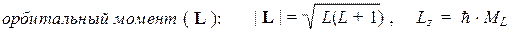|
|
Атом с глобальной точки зренияГлава 1. АТОМЫ Термин "атом" широко используется во всех естественных науках, имеющих дело с исследованием и практическим использованием различных веществ. В широком смысле слова под "атомами" понимаются микроскопические частицы, входящие в состав любых веществ. Однако содержание научного понятия, обозначаемого данным термином, оказывается различным, в зависимости от используемых методов исследования и описания веществ. В рамках данного курса необходимо различать две интерпретации этого термина — "химический атом" и "физический атом". Химический атом — это понятие классической химии, необходимое для описания и объяснения химических свойств веществ. Химические атомы всегда являются составной частью вещества и никогда не встречаются в свободном виде. Поэтому его свойства недоступны для измерения с помощью приборов и имеют конвенциональный характер. В качестве примера можно привести такие характеристики химических атомов как: относительная атомная масса (атомный вес), порядковый номер в периодической таблице, валентность, электроотрицательность, степень окисления, атомные радиусы (ковалентный, ионный) и др. Все химические атомы одного вида считаются тождественными друг другу и, следовательно, любой химический атом данного типа имеет единственное доступное ему состояние. Другими словами, указание типа атома (т.е. его химического символа, например, H, Si, Au) полностью определяет и все его химические свойства. Физический атомпредставляет собой микроскопическую структуру, состоящую из одного атомного ядра и электронной оболочки. Физический атом существует отдельно от окружающей среды и поэтому его всегда можно поместить в прибор, произвести над ним соответствующие измерения и получить числовые значения таких физических характеристик как: энергия, орбитальный и спиновой механические моменты, магнитные моменты, поляризуемость и др. Физический атом, следовательно, допускает построение стандартного механического описания через наблюдаемые, уравнения состояния и уравнения эволюции. При этом малые размеры атома требуют использования квантового варианта механики. Физический атом имеет множество доступных механических состояний и может переходить из одного состояния в другие за счет внешних возмущений. В отличие от химического атома, указание типа физического атома не определяет его свойства однозначно, поскольку эти свойства могут изменяться в широком диапазоне в результате его переходов из одного состояния в другие. Любые механические модели пригодны для описания именно физических атомов. Это, однако, не означает, что такие модели бесполезны для решения химических задач. Существуют способы, позволяющие адаптировать результаты, полученные методами механики для физических атомов, к химической проблематике. Надо только всегда помнить о необходимости такой адаптации и не пытаться переносить полученные механическим способом результаты непосредственно на химические атомы. МЕХАНИЧЕСКАЯ СТРУКТУРНАЯ МОДЕЛЬ АТОМА Для сложных (составных) систем механический способ позволяет построить два типа описания, различающиеся по масштабу: глобальное и локальное. В рамках глобального описания атом рассматривается "снаружи и издалека" и, соответственно, выглядит как материальная точка, обладающая набором глобальных наблюдаемых, характеризующих атом в целом, но не имеющих прямого отношения ни к одной из составляющих его частиц. В рамках локального описания атом рассматривается "изнутри" и, соответственно, выглядит как совокупность взаимодействующих между собой электронов, причем каждый из них требует индивидуального описания с помощью набора локальных (одночастичных) наблюдаемых. Макроскопические структуры, описываемые методами классической механики, допускают оба описания — и глобальное, и локальное, причем оба описания согласованы между собой. Атомы являются микроскопическими структурами и требуют использования методов квантовой механики. В этом случае оказывается, что два вида описания — глобальное и локальное — взаимно исключают друг друга. Причиной служит наличие сильных межэлектронных взаимодействий. Можно сказать, что здесь имеет место своеобразный случай принципа неопределенности. Ввиду этой особенности в рамках ортодоксальной квантовой механики приходится удовлетворяться только глобальным описанием атома как бесструктурной материальной точки. Если все же поставить перед собой цель описать атом локально, то в этом случае вместо строгого механического описания можно построить лишь весьма приближенную модель, требующую использования посторонних для квантовой механики соображений, и поэтому относящуюся уже не к квантовой механике, а к квантовой химии. Атом с глобальной точки зрения С глобальной точки зрения атом характеризуется набором механических наблюдаемых, т.е. таких величин, которые могут быть выражены числами, причем эти числа допускают, хотя бы в принципе, прямое экспериментальное измерение. Все глобальные наблюдаемые атома могут быть измерены с помощью стандартных экспериментальных процедур квантовой механики, основанных на применении спектральных анализаторов. Первой в списке наблюдаемых стоит энергия. (Следует подчеркнуть, что речь здесь идет о внутренней энергии атома, которая не включает в себя ни кинетическую энергию движения атома как целого, ни потенциальную энергию атома во внешних полях, например, гравитационных.) Эту характеристику можно точно определить для любого объекта, находящегося в стационарном состоянии. Рассматривая атом как совокупность электронов, движущихся в потенциальной яме, созданной электрическим зарядом ядра, можно заключить, что атому доступно множество дискретных энергетических уровней. При действии различных возмущающих факторов (например, при электромагнитном облучении) атом может скачкообразно переходить из одного стационарного состояния в другое, поглощая или испуская дискретные порции (кванты) энергии. Дискретные энергетические уровни, соответствующие стационарным состояниям атома, называются атомными термами. Они могут быть обнаружены и исследованы различными экспериментальными средствами: ААС (атомная абсорбционная спектроскопия), АЭС (атомная эмиссионная спектроскопия), Оже-спектроскопия, ФЭС (фотоэлектронная спектроскопия) и т.д. Список глобальных наблюдаемых атомов не исчерпывается одной энергией. Об этом свидетельствует ряд эффектов расщепления атомных термов под влиянием внешних полей — магнитных (эффекты Зеемана и Пашена-Бака) и электрических (эффект Штарка). Следовательно, одной и той же энергии (атомному терму) соответствует несколько состояний, различающихся значениями дополнительных характеристик. В качестве этих характеристик выступают механические моменты, порождаемые вращательным (орбитальным) движением электронов. Следует иметь в виду, что это движение отличается по своему характеру как от классического вращения, так и от элементарных квантовомеханических моделей типа плоского жесткого ротатора. Несмотря на это, многие важные особенности вращательного движения (например, способность тел, обладающих массой и электрическим зарядом, порождать момент импульса и магнитный момент) сохраняются и в этом случае. Необходимо различать несколько разновидностей моментов. Во-первых, это полный механический момент атома (J), для которого можно определить модуль | J | и одну из проекций Jz :
где J — квантовое число полного механического момента, а MJ — соответствующее магнитное число. Допустимые значения этих квантовых чисел для различных атомов задаются формулами: J = 0, 1/2, 1, 3/2, 2, 5/2, … и MJ = –J, (–J + 1), …, (+J – 1), +J. Поскольку электроны обладают электрическими зарядами, то с механическим моментом J всегда связан полный магнитный момент атома mJ, благодаря наличию которого атом может взаимодействовать с внешними магнитными полями. Следует иметь в виду, что, в отличие от элементарных частиц, для большинства атомов направление этого вектора не совпадает с направлением вектора механического момента: mJ ¹ g ×J. Несовпадение ориентаций двух векторов можно объяснить тем, что полный механический момента складывается из двух компонент: J = L +S,которые характеризуются аналогичными парами квантовых чисел:
где: L = 0, 1, 2, 3, … и ML = –L, (–L + 1), …, (+L – 1), +L ;
где: S = 0, 1/2, 1, 3/2, 2, … и MS = –S, (–S + 1), …, (+S – 1), +S . Каждый из этих моментов характеризуется своим магнитно-механическим отношением: mL = gL ×Lи mS = gS ×S. Поэтому в формуле, связывающей величины двух полных моментов — магнитного и механического, — имеется дополнительный множитель g, который называется "g-фактором" или "фактором Ланде" (в общем случае он представляет собой тензор 2 ранга): mJ = g × g ×J Полная энергия атома зависит от длин векторов J, L и S, но не от величин их проекций. Поэтому все состояния атома, которые характеризуются определенными значениями квантовых чисел J, L и S, имеют одну и ту же энергию. Совокупность таких вырожденных по энергии состояний атома также обозначается термином "атомный терм". Существует специальная номенклатура, в которой для обозначения атомных термов используют специальные символы, состоящие из буквы и двух числовых индексов:
Например, символ 3Р2 означает совокупность состояний атома, для которых квантовые числа имеют значения: J = 2, L = 1, S = 1. Между собой эти состояния различаются значениями магнитных чисел МJ, МL и МS. Глобальные наблюдаемые атома не только доступны прямому экспериментальному измерению, но также могут быть вычислены как собственные значения соответствующих квантовомеханических операторов: AY = A × Y Для использования этих уравнений необходимо знать явный вид волновых функций Y, установление которых представляет собой центральную задачу теории физического атома. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|