
|
|
Взаимные превращения жидкостей и газов.Испарение и конденсация. Любое вещество при определенных условиях может находиться в различных агрегатных состояниях - твердом, жидком и газообразном. Переход из одного состояния в другое называется фазовым переходом. Испарение и конденсация являются примерами фазовых переходов. Однако превращение газа в жидкость может происходить только при температурах ниже определенной, так называемой критической температуры Ткр. Например, для воды критическая температура равна 647.3 К, для азота 126 К, для кислорода 154.3 К. При комнатной температуре ( Испарением называется фазовый переход из жидкого состояния в газообразное. С точки зрения молекулярно-кинетической теории испарение - это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, т.е. к охлаждению жидкости (если нет подвода энергии от окружающих тел). Конденсация - это процесс, обратный процессу испарения. При конденсации молекулы пара возвращаются в жидкость.
Влажность.
Абсолютной влажностью называется плотность водяных паров в атмосфере -
Охлаждение пара при постоянном давлении рано или поздно превратит его в насыщенный пар. Температура при которой водяной пар становится насыщенным, называют точкой росы. При охлаждении воздуха до точки росы начинается конденсация паров: появляется туман. Выпадает роса.
Гигрометры и психрометры.
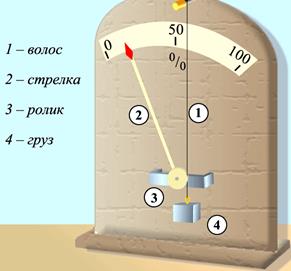
Для измерения влажности воздуха используют гигрометры в котором используют свойство волоса изменять свою длину при увеличении или уменьшении влажности воздуха.
Психрометр Августа состоит из двух термометров сухого и важного. По показанию сухого термометра и по разнице температур по психрометрической таблице определяют влажность воздуха. Для показаний указанных на рисунке влажность составляет 59%.
Кипение. Давление p0 насыщенного пара очень быстро возрастает с ростом температуры T. Зависимость p0(T) нельзя получить из законов идеального газа. Давление газа при постоянной концентрации молекул растет прямо пропорционально температуре. В насыщенном паре при повышении температуры возрастает не только средняя кинетическая энергия движения молекул, но и их концентрация. Поэтому давление насыщенного пара при повышении температуры возрастает быстрее, чем давление идеального газа при постоянной концентрации молекул. Испарение может происходить не только с поверхности, но и в объеме жидкости. В жидкости всегда имеются мельчайшие пузырьки газа. Если давление насыщенного пара жидкости равно внешнему давлению (т.е. давлению газа в пузырьках) или превышает его, жидкость будет испаряться внутрь пузырьков. Пузырьки, наполненные паром, расширяются и всплывают на поверхность. Этот процесс называется кипением. Таким образом, кипение жидкости начинается при такойтемпературе, при которой давление ее насыщенных паров становится равным внешнему давлению. В частности, при нормальном атмосферном давлении вода кипит при температуре 1000 С. Это значит, что при этой температуре давление насыщенных паров воды равно 1 атм. При подъеме в горы атмосферное давление уменьшается, и поэтому температура кипения воды понижается (приблизительно на 10 С на каждые 300 метров высоты). На высоте 7·103 м давление составляет примерно 0.4 атм, и температура кипения понижается до 700 С. В герметически закрытом сосуде жидкость кипеть не может, т.к. при каждом значении температуры устанавливается равновесие между жидкостью и ее насыщенным паром. По кривой равновесия p0(T) можно определять температуры кипения жидкости при различных давлениях.
Примером может служить кривая равновесия p0(T) насыщенного пара и жидкости. Если кривые равновесия между различными фазами данного вещества построить на плоскости (p,T), то они разбивают эту плоскость на отдельные области, в которых вещество существует в однородном агрегатном состоянии - твердом, жидком или газообразном (рис.). Изображенные в координатной системе (p, T) кривые равновесия называются фазовой диаграммой. Кривая OT, соответствующая равновесию между твердой и газообразной фазами, называется кривой сублимации. Кривая TK равновесия между жидкостью и паром называется кривой испарения; она обрывается в критической точке K. Кривая TM равновесия между твердым телом и жидкостью называется кривой плавления. Кривые равновесия сходятся в точке T, в которой могут сосуществовать в равновесии все три фазы. Эта точка называется тройной точкой.
Контрольные вопросы и задания: Пример: Относительная влажность воздуха в закрытом сосуде при температуре 50 С равна 84%, а при температуре 220 С равна 30%. Во сколько раз давление насыщенного паров воды при температуре t2 больше, чем при температуре t1? Решение: Давление водяного пара в сосуде при Т1= 278К равно: р1= Отсюда Вопрос 1. Как изменяется температура жидкости при ее испарении?
Вопрос 3. На каком из графиков правильно изображена зависимость давления насыщенного пара от абсолютной температуры?
Вопрос 3. Как изменится точка кипения жидкости при повышении давления? Вопрос 4. Как можно перевести ненасыщенный пар в насыщенный?
Задача 1. При относительной влажности воздуха Задача 2. Кубический метр влажного воздуха при относительной влажности Задача 3. Определите абсолютную влажность воздуха, если парциальное давление пара в нем 14кПа, температура 333К. Задача 4. Относительная влажность в комнате при температуре 160 С составляет 65%. Как изменится она при понижении температуры воздуха на 4к, если давление водяного пара остается прежним. Задача 5. В сосуде вместимостью 100л при температуре 30 С находится воздух с относительной влажностью 30%. Какой будет относительная влажность воздуха в сосуде, если в него ввести воду массой 1г?

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 К) вода может находиться и в жидком и в газообразном состояниях, а азот и кислород существуют только в виде газов.
К) вода может находиться и в жидком и в газообразном состояниях, а азот и кислород существуют только в виде газов. Насыщенные и ненасыщенные пары.В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, т.е. когда скорости процессов испарения и конденсации одинаковы. Такую систему называют двухфазной. Пар, находящийся в равновесии со своей жидкостью, называют насыщенным. Установление динамического равновесия между процессами испарения и конденсации при повышении температуры происходит при более высоких концентрациях молекул пара. Так как давление газа (пара) определяется его концентрацией и температурой, то можно сделать вывод: давление насыщенного пара p0 данного вещества зависит только от его температуры и не зависит от объема. Поэтому изотермы реальных газов на плоскости (p, V) содержат горизонтальные участки, соответствующие двухфазной системе (рис.). При повышении температуры давление насыщенного пара и его плотность возрастают, а плотность жидкости уменьшается из-за теплового расширения. При температуре, равной критической температуре Tкр для данного вещества, плотности пара и жидкости становятся одинаковыми. При T>Tкр исчезают физические различия между жидкостью и ее насыщенным паром. Из газообразного состояния в жидкое можно перейти, минуя двухфазную область. Для этого нужно совершить процесс в обход критической точки K. Один из возможных процессов такого рода показан на рисунке ломаной линией ABC.
Насыщенные и ненасыщенные пары.В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, т.е. когда скорости процессов испарения и конденсации одинаковы. Такую систему называют двухфазной. Пар, находящийся в равновесии со своей жидкостью, называют насыщенным. Установление динамического равновесия между процессами испарения и конденсации при повышении температуры происходит при более высоких концентрациях молекул пара. Так как давление газа (пара) определяется его концентрацией и температурой, то можно сделать вывод: давление насыщенного пара p0 данного вещества зависит только от его температуры и не зависит от объема. Поэтому изотермы реальных газов на плоскости (p, V) содержат горизонтальные участки, соответствующие двухфазной системе (рис.). При повышении температуры давление насыщенного пара и его плотность возрастают, а плотность жидкости уменьшается из-за теплового расширения. При температуре, равной критической температуре Tкр для данного вещества, плотности пара и жидкости становятся одинаковыми. При T>Tкр исчезают физические различия между жидкостью и ее насыщенным паром. Из газообразного состояния в жидкое можно перейти, минуя двухфазную область. Для этого нужно совершить процесс в обход критической точки K. Один из возможных процессов такого рода показан на рисунке ломаной линией ABC. В атмосферном воздухе всегда присутствуют пары воды при некотором парциальном давлении ( давление водяного пара при отсутствии других газов) p, которое как правило, меньше давления насыщенного пара p0. Отношение
В атмосферном воздухе всегда присутствуют пары воды при некотором парциальном давлении ( давление водяного пара при отсутствии других газов) p, которое как правило, меньше давления насыщенного пара p0. Отношение  , выраженное в процентах, называется относительной влажностью воздуха.
, выраженное в процентах, называется относительной влажностью воздуха. .
.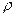 ;
;  , плотность насыщенного пара
, плотность насыщенного пара 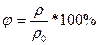


 Фазовые переходы. Изображенная на рисунке картина изотерм реального газа описывает процессы испарения и конденсации, т.е. фазовый переход между газообразной и жидкой фазами вещества. Зависимость равновесного давления от температуры называется кривой фазового равновесия.
Фазовые переходы. Изображенная на рисунке картина изотерм реального газа описывает процессы испарения и конденсации, т.е. фазовый переход между газообразной и жидкой фазами вещества. Зависимость равновесного давления от температуры называется кривой фазового равновесия. *ро, где ро- давление насыщенного пара при температуре Т1. При температуре Т2=295К р2=
*ро, где ро- давление насыщенного пара при температуре Т1. При температуре Т2=295К р2=  .
. .
. Вопрос 2. Как изменяется давление насыщенного пара при уменьшении его объема?
Вопрос 2. Как изменяется давление насыщенного пара при уменьшении его объема? Вопрос 5. Какой участок изотермы реального газа соответствует процессу превращения газа в жидкость.
Вопрос 5. Какой участок изотермы реального газа соответствует процессу превращения газа в жидкость. вода, налитая в блюдце, испарилась на открытом воздухе за время
вода, налитая в блюдце, испарилась на открытом воздухе за время  мин. За какое время
мин. За какое время  испарилась бы вода при относительной влажности
испарилась бы вода при относительной влажности  ?
? , температуре t=200C и давлении p=105 Па имеет массу m=1.19 кг. Определите давление Pн насыщенного водяного пара при температуре 200C.
, температуре t=200C и давлении p=105 Па имеет массу m=1.19 кг. Определите давление Pн насыщенного водяного пара при температуре 200C. Задача 6.Относительная влажность воздуха вечером при t =160 С равна 55%. Выпадет ли роса, если ночью температура понизится до 8 0С?
Задача 6.Относительная влажность воздуха вечером при t =160 С равна 55%. Выпадет ли роса, если ночью температура понизится до 8 0С?