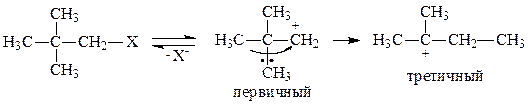|
|
Пероксидное окисление липидов
Тема: Основные закономерности протекания органических реакций Реакционная способность – способность вещества вступать в ту или иную химическую реакцию и реагировать с большей или меньшей скоростью.
Реакционный центр – атом или группа атомов в молекуле, непосредственно участвующих в химической реакции.
Субстрат – вещество, подвергающееся изменениям в результате химической реакции.
Реагент– его партнер. субстрат реагент продукт реакции субстрат реагент продукт реакции
реакционный центр основный, реагент кислотный реакционный центр кислотный, реагент основный
В биохимии:
Типы реагентов:
Основание – отрывает протон от кислотного центра (НО-, СН3О-).
Нуклеофил – имеет повышенную электронную плотность, взаимодействует с любым атомом, кроме водорода, несущим частичный или полный положительный заряд (заряжен отрицательно или имеет неподеленную пару электронов или π–связь) (Cl-, OH-, NH3, CH3O-, R-).
Электрофил – имеет недостаток электронов, взаимодействует с реакционным центром с повышенной электронной плотностью (заряжен положительно, или имеет атом с частичным положительным зарядом или имеет вакантную орбиталь) (H+, Cl+, H2CO, AlCl3, R+).
Свободный радикал – частица, имеющая неспаренный электрон (H۰, HO۰,۰O-O۰ , R۰) .
Окислитель – отбирает электроны или атомы водорода от органического субстрата (O2, Fe3+, органические окислители).
Восстановитель – отдает электроны или атомы водорода субстрату (Fe2+, органические восстановители).
Классификация органических реакций:
1. По типу разрыва связи: - гомолитические - гетеролитические
2. По типу реагента - радикальные (R) - электрофильные (E) - нуклеофильные (N) - окислительные - восстановительные
3. По конечному результату - замещения (S) - присоединения (A) - отщепления или элиминирования (Е) - изомеризации - циклизации
4. По числу частиц, участвующих в стадии, определяющей скорость реакции - мономолекулярные (диссоциативные) - бимолекулярные (ассоциативные)
Механизм реакции – детальное описание всех ее стадий: 1. Элементарные стадии 2. Способ разрыва и образования связи на каждой стадии 3. Стереохимия процесса – пространственное строение исходных продуктов, переходных состояний, промежуточно образующихся частиц и продуктов реакции 4. Кинетика процесса
Факторы, определяющие реакционную способность Органического вещества Пространственный фактор – пространственная доступность реакционного центра молекулы.
Электронный фактор – распределение электронной плотности в молекуле (электроотрицательность атомов, входящих в молекулу, электронные эффекты заместителей, наличие сопряженных и ароматических фрагментов).
Статический фактор –
Динамический фактор –
Тема: Механизмы органических реакций Свободно-радикальные процессы Пути образования свободных радикалов: 1. Фотохимический 2. Термический 3. Химический Механизм галогенирования алканов. Реакции SR.
Региоселективность реакций радикального замещения
Статический фактор - энергия разрыва связи (кДж/моль):
Динамический фактор - устойчивость свободного радикала:
Региоселективность галогенирования
Электрофильные реакции. π-доноры:
Реакции электрофильного присоединения(AE)
1. Галогенирование алкенов:
2. Гидрогалогенирование алкенов:
3. Гидратация алкенов (АЕ):
Региоселективность реакций АЕ Н3С-С=СН2 + HCl ® H3C-CH(Cl)-CH3 F3С-С=СН2 + HCl ® F3C-CH2-CH2Cl
Исключения из правила В.В Марковникова:
а) К несимметричным алкенам, имеющим в сопряжении электроноакцепторный заместитель, водород присоединяется к наименее гидрированному атому углерода.
б) В присутствии перекисей, инициирующих радикальную реакцию (АR), водород присоединяется к наименее гидрированному атому углерода.
4. Алкилирование алкенов карбокатионами:
(АЕ)-реакции в сопряженных системах
Механизм SЕ-реакций в ароматическом кольце
электрофил продукт субстрат π-комплекс σ-комплекс замещения
Резонансные структуры σ–комплекса: Примеры реакций электрофильного замещения: Галогенирование: Роль катализатора – формирование электрофильной частицы:
Нитрование:
Сульфирование:
Алкилирование по Фриделю-Крафтсу:
Ацилирование по Фриделю-Крафтсу:
Алкилирование ароматических соединений карбкатионами в биохимических реакциях:
Региоселективность реакций электрофильного замещения:
орто мета пара X – донор X – акцептор X - донор
Тема: Реакции нуклеофильного замещения у sp3-гибридного атома углерода Классы органических соединений, содержащих связь С-Х (углерод-гетероатом) 1. С-Hal (в организме – иодсодержащие гормоны щитовидной железы) 2. С-O (спирты, фенолы, простые эфиры, пероксиды, гидропероксиды) 3. C-S (тиолы, сульфиды, дисульфиды) 4. C-N (амины, четвертичные аммониевые основания) Общее – полярная связь углерод-гетероатом:
Нуклеофильность – способность взаимодействовать с атомом (кроме водорода), несущем целый или частичный положительный заряд.
Общая схема: нуклеофил субстрат продукт уходящая реакции группа
Факторы, влияющие на скорость реакции:
Структура субстрата
Нуклеофильная сила
3. Уходящая группа - должна быть хорошей
Стереохимия реакции

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|







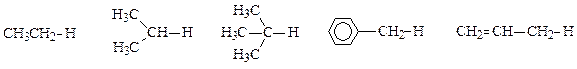
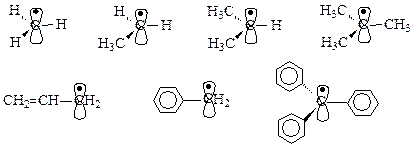















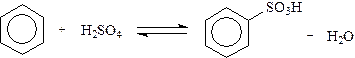

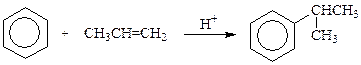

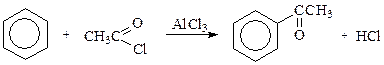





 переходное состояние
переходное состояние