
|
|
Распределение Максвелла-Больцмана. Распределение Больцмана.
5.1. Распределение Максвелла-Больцмана В начале настоящей главы мы установили, что для классической подсистемы её энергия может быть представлена в виде суммы двух независимых слагаемых:
поскольку кинетическая энергия есть функция импульсов (скоростей) частиц, а потенциальная энергия - функция координат. Поэтому вероятность для подсистемы находится в состоянии с энергией
Используя распределение Гиббса, мы можем записать, что вероятность молекуле находиться в состоянии с энергией
Выраженное таким образом распределение вероятностей для одной частицы называется распределением Максвелла-Больцмана.
Средняя энергия, приходящаяся на колебательную степень свободы. Закон Дюлонга и Пти.
Распределение Максвелла-Больцмана позволяет получить теплоемкость твердых тел при высоких температурах Равновесное состояние кристалла – периодическое расположение атомов в пространстве. Однако, атомы не находятся в покое, они совершают малые тепловые колебания относительно положений равновесия. Рассмотрим колебания, совершаемые атомом вдоль оси
где
Здесь
Сосчитаем среднюю энергию осциллятора, совершающего колебания вдоль оси
Выше, используя интеграл Пуассона, мы получили
аналогично
Т.о.,
Итак, на одну колебательную степень свободы приходится энергия Здесь мы окончательно доказали теорему о равномерном распределении энергии по степеням свободы, согласно которой на каждую колебательную степень свободы приходится энергия Если представить колебательное движение атомов в кристалле в виде совокупности независимых движений вдоль трех ортогональных осей
а для тела, состоящего из
Если рассматривать 1 моль вещества, то
где температура Эта энергия играет роль внутренней энергии в термодинамике, поэтому молярная теплоемкость
Т.о., мы пришли к правилу, которое было установлено опытным путем и получило название закона Дюлонга и Пти: Молярная теплоемкость всех твердых тел при высоких температурах (
5.2. Распределение Больцмана.
Пусть интересующая нас подсистема (газ) находится во внешнем поле, в котором потенциальная энергия молекулы Основываясь на соотношении (5.1), т.е. в силу независимости событий иметь определенные значения как кинетической, так и потенциальной энергий, можно рассмотреть отдельно распределение частиц во внешнем поле
что дает вероятность нахождения частицы в объеме Пусть
то число молекул в элементе пространственного объема
Смысл множителя
Тогда, очевидно, что произведение
Полученная формула носит название распределения Больцмана. Примечание: если отсчет идет от точки, где
Примеры применения распределения Больцмана.
1). Распределение частиц в сосуде по высоте в однородном поле тяжести ( Для Земли поле тяжести может считаться однородным для небольших высот
Тогда получаем известную барометрическую формулу Больцмана:
Здесь
Концентрация частиц убывает с высотой, причем концентрация более тяжелых частиц убывает с высотой быстрее. Это создает подъемную силу (для более легких объектов - воздушные шары). Для более высоких температур распределение высотой становится более равномерным (см. рисунок). При этом полное число частиц сосуде N постоянно:
Здесь
Сила инерции
Таким образом, концентрация молекул растет с радиусом.
3). О распределении молекул в атмосфере планет. Потенциальная энергия молекул равна:
Однако, если бы это распределение было справедливо на всех расстояниях от планеты, то при
Т.е. получаем конечное число для концентрации на бесконечности, что невозможно, т.к. объем вокруг планеты бесконечен, а общее число молекул в атмосфере конечно. Получаем, что равновесие возможно лишь при Отсюда вывод: невозможность существования равновесного состояния планетной атмосферы. Это связано с тем, что разность потенциальной энергии молекулы в поле тяготения планеты на поверхности и на бесконечности остается конечной.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 ,
, определяется как
определяется как . (5.1)
. (5.1) . (5.2)
. (5.2) , при которых применимо классическое описание.
, при которых применимо классическое описание. . Энергия такого осциллятора равна
. Энергия такого осциллятора равна
 масса атома,
масса атома,  упругая постоянная. Статистическое описание атомов с энергией
упругая постоянная. Статистическое описание атомов с энергией 
 - нормировочная постоянная, выражаемая через произведение 2-х постоянных:
- нормировочная постоянная, выражаемая через произведение 2-х постоянных:  , которые равны, соответственно:
, которые равны, соответственно: .
.
 .
. ,
, .
. .
. . Из расчета видно, что первое слагаемое
. Из расчета видно, что первое слагаемое  возникает при усреднении кинетической энергии колебательного движения, а второе слагаемое
возникает при усреднении кинетической энергии колебательного движения, а второе слагаемое  ).
). , то средняя энергия колебаний атома равна
, то средняя энергия колебаний атома равна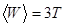 ,
, атомов:
атомов: .
. и
и ,
, измеряется в Кельвинах.
измеряется в Кельвинах. твердого тела при постоянном объеме оказывается равной
твердого тела при постоянном объеме оказывается равной .
. ) не зависит от температуры и равна
) не зависит от температуры и равна 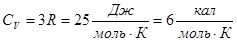 .
. есть функция только её координат (например, гравитационное поле).
есть функция только её координат (например, гравитационное поле). :
: , (5.3)
, (5.3) вблизи точки с координатами
вблизи точки с координатами  .
. полное число молекул в подсистеме. Так как
полное число молекул в подсистеме. Так как ,
, определяется формулой:
определяется формулой: (5.4)
(5.4) легко установить, если ввести число частиц в единице объема, т.е. концентрацию частиц (плотность числа частиц):
легко установить, если ввести число частиц в единице объема, т.е. концентрацию частиц (плотность числа частиц): (5.5)
(5.5) , т.е.
, т.е.  . Тогда выражение (5.5) принимает вид
. Тогда выражение (5.5) принимает вид (5.6)
(5.6) , тогда распределение Больцмана имеет вид:
, тогда распределение Больцмана имеет вид: (5.7)
(5.7) ).
). (
(  ), где
), где 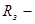 радиус Земли.:
радиус Земли.:
 ,
,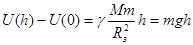
 (5.8)
(5.8) - молярная масса газа,
- молярная масса газа,  - универсальная газовая постоянная. Воспользовавшись связью между концентрацией газа и давлением, получаем барометрическую формулу Больцмана в виде:
- универсальная газовая постоянная. Воспользовавшись связью между концентрацией газа и давлением, получаем барометрическую формулу Больцмана в виде: (5.9)
(5.9)
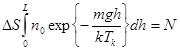 .
. площадь сечения сосуда, а
площадь сечения сосуда, а 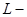 его полная высота.
его полная высота. 2). Распределение частиц во вращающемся сосуде.
2). Распределение частиц во вращающемся сосуде. и потенциальная энергия
и потенциальная энергия  , тогда распределение частиц имеет вид:
, тогда распределение частиц имеет вид: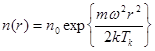 (5.10)
(5.10) и в равновесном состоянии получаем следующее распределение:
и в равновесном состоянии получаем следующее распределение: .
. мы бы получили
мы бы получили .
. , т.е. атмосфера не должна быть в равновесии.
, т.е. атмосфера не должна быть в равновесии.