|
Карапетьянц М.Х., Дракин С.И. Общая и неорганическая химия. – М.: Химия, 1993. – 558 с.
11. Карапетьянц М.Х., Дракин С.И. Строение вещества. – М.: Высшая школа, 1976.– 304 с.
12. Кемпбел Д. Современная общая химия. Т. 1-3. – М: Мир, 1989.
13. Коровин В.Н. Общая химия. –М.: Высшая школа, 2000.– 558 с.
14. Коровин Н.В., Масленникова Г.Н. и др. Курс общей химии. – М.: Высшая школа, 1998. – 445 с.
15. Краткий справочник физико-химических величин / Под ред. А.А. Равделя и А.М. Пономаревой. – СПб.: Специальная литература, 1998. – 232 с.
16. Литвинова Т.Н. Сборник задач по общей химии. – М.: Мир и образование, 2007.– 224 с.
17. Некрасов Б.В. Основы общей химии, т. 1-2. – М.: Химия, 1973. – 518 с., – 415 с.
18. Николаев Л.А. Современная химия. –М.: Просвещение, 1970.– 208 с.
19. Пузаков С.А., Попков В.А., Филиппова А. Л. Сборник задач и упражнений по общей химии: Учеб. пособие. – М.: Высшая школа, 2004. – 255 с.
20. Полинг А. Общая химия.– М.: Мир, 1974. – 848 с.
21. Практикум по общей химии / Е.М.Соколовская, О.С.Зайцев. – М.: Изд-во Моск. ун-та, 1981. – 400 с.
22. Сборник задач и упражнений по общей химии: Учеб. пособие для нехим. спец. Вузов /Л. М. Романцева, 3.Л. Лещинская, В.А. Суханова. – М.: Высшая школа, 1991.– 288 с.
23. Семенов И.Н., Перфилова И.Л. Химия: Учеб. для вузов. – СПб: Химиздат, 2000. – 656 с.
24. Слета Л.А., Черный А.В., Холин Ю.В. 1001 задача по химии с ответами, указаниями, решениями. – М: Илекса, 2004. –368 с.
25. Суворов А.В., Никольский А.Б. Общая химия. – СПб: Химиздат, 2001. –512 с.
26. Угай Я.А. Общая и неорганическая химия. – М.: Высшая школа, 1997. – 527 с.
27. Хомченко И.Г. Сборник задач и упражнений по химии. – М.: Высшая школа, 1989. – 253 с.
Приложение 1
Некоторые константы и величины
Число Авогадро А= 6,022·1023 частиц / моль
Постоянная Планка  h =6,62·10-34 Дж·К-1 h =6,62·10-34 Дж·К-1
Постоянная Больцмана 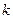 б =1,3805·10-23 Дж·К-1 б =1,3805·10-23 Дж·К-1
Универсальная газовая постоянная R=8,3143 Дж·К-1·моль-1
Масса электрона mе =9,110·10-31 кг =5,48580·10-4 а.е.м.
Масса протона mр =1,673·10-27кг=1,007276 а.е.м.
Боровский радиус а0 =5,292·10-11 м.
Атомная единица массы (а.е.м.)=1,66-27 кг
Скорость света с =2,998·108 м·с-1
Давление (стандартные условия) Р =1,013·105 Н·м-2 (1,013·10-5 Па)=760 мм рт. ст.
Абсолютный нуль Т0 =-273,15 0С
Элементарный электрический заряд е =1,602189·10-19 Кл
Число Фарадея F =9,64846·104 Кл·моль-1
Соотношение между некоторыми единицами
В различных системах.
| Величина
| Единица измерения
| Эквивалент в СИ
| |
Энергия, работа
| Электроновольт (эВ)
| 1,60219·10-19Дж
| | Калория (кал)
| 4,1868 Дж
| | Эгр
| 10-7 Дж
| |
Длина
| Микрон или микрометр (мкм)
| 1·10-6м
| | Нанометр
| 1·10-9м
| | Ангстрем
| 1·10-10м
| | Давление
| Миллиметр ртутного столба (мм рт. ст.)
| 133,322 Па
|
Значения газовой постоянной в
Различных единицах измерения
| Единица
| Дж/моль ·К
| эрг/моль·К
| л·атм/моль·К
| кал/моль·К
| кгс·м/моль·К
| | R
| 8,3143
| 8,3143·107
| 0,082057
| 1,98725
| 0,8478
|
Приложение 2
Стандартные энтальпии образования∆Н0298, энтропии
∆ S0298 и энергии Гиббса∆G0298 К (25 0С)
| Вещество
| ∆Н0298 кДж/моль
| ∆S0298, Дж/(моль·К)
| ∆G0298, кДж/моль
| | Al (к)
AlCl3 (к)
AlCl3·6H2O(к)
Al2O3(к)
BaCO3(к)
ВаО (к)
Вr2(ж)
С (графит)
3СаО·Аl2O3 (к)
3СаО·Аl2O3·6H2O (к)
СН4 (г)
С2Н4 (г)
C2H4 (г)
С3Н8
н-С4Н10 (г)
изо-С4Н10 (г)
С5Н12 (г)
С6Н14
С6Н14 (ж)
С7Н16 (г)
С7Н16(ж)
С8Н18 (г)
С6Н12О6 (к)
СН3ОН (ж)
С2Н5ОН (ж)
н-С3Н7ОН (ж)
изо-С3Н7ОН (ж)
н-С5Н13ОН (ж)
СаВr2 (к)
СаВr2·6Н2О (к)
СаСl2 (к)
СаСl2·6Н2О (к)
СаСО3 (к)
СаНРО4 (к)
СаНРО4·2Н2О (к)
СаО
Са(ОН)2 (к)
СаSO4·0,5Н2О (к)
СаSO4·2Н2О (к)
Сl2 (г)
Сl2O (г)
СlО2 (г)
СО (г)
СО2 (г)
СS2 (г)
2СаО·SiO2 (к)
2CaO·SiO2·2H2O (к)
3CaO·SiO2 (к)
Cu (к)
СuCl2 (к)
СuCl2·2H2O (к)
СuSO4 (к)
СuSO4·5H2O (к)
СuO (к)
F2 (г)
Fe (к)
FeO (к)
Fe2O3 (к)
Fe3O4 (к)
FeSO4 (к)
FeSO4·7H2O (к)
Н2 (г)
HBr (г)
HCl (г)
HF (г)
HI (г)
H2O (г)
Н2О (ж)
Н3РО4 (р)
Н2S (г)
I2 (г)
MgCO3 (к)
MgO (к)
MnCl2м (к)
MnCl2·4H2O (к)
N2 (к)
Na2CO3
Na2CO3·7H2O (к)
Na2SO4 (к)
Na2SO4·10H2O (к)
NH3 (ж)
Ni (к)
NiO (к)
NiSO4 (к)
NiSO4·7H2O (к)
N2O (г)
NO (г)
N2O3 (г)
NO2 (г)
N2O4 (г)
O2 (г)
OF2 (г)
Pb (к)
Р (к)
PBr3 (г)
PBr5 (ж)
PCl3 (г)
PCl5 (г)
PF3 (г)
PF5 (г)
PbO (к)
PbO2 (к)
S (к)
Sn (к)
SnO (к)
SnO2 (к)
SO2 (г)
SO3 (г)
SnCO3 (к)
SnO (к)
Zn (к)
ZnO (к)
|
-704,2
-2693
-1676,0
-1219,0
-558,1
-3556,4
-5550,6
-74,9
52,3
-89,7
-103,8
-126,2
-131,6
-146,4
-167,2
-189,8
-187,8
-224,4
-208,5
-1273,0
-238,6
-277,6
-307,0
-302,3
-306,1
-674,9
-2507,9
-795,0
-2599,6
-1207,0
-1815,6
-2405,2
-635,5
-986,6
-1577,8
-2024,0
76,6
105,0
-110,5
-393,5
115,3
-2308,5
-3140,8
-2968,3
-215,6
-818,6
-770,9
-2279,4
-162,0
-264,8
-822,2
-1117,1
-929,5
-3016,0
-34,1
-91,8
-270,9
26,6
-241,8
-285,8
-1288,3
-21,0
62,4
-1113,0
-601,8
-481,2
-1687,4
-1131,0
-4083,5
-1384,6
-4324,2
294,0
-239,7
-873,5
-2977,4
82,0
90,3
83,3
33,5
9,6
25,1
-132,0
-184,0
-287,0
-366,0
-956,5
-1593,0
-219,3
-276,6
-286,0
-580,8
-296,9
-395,8
-1216,4
-590,4
-350,6
| 28,3
109,3
318,2
50,9
112,0
70,3
152,3
5,74
205,5
404,8
186,2
219,4
229,5
269,9
310,1
-
348,9
388,4
295,9
427,8
328,5
466,7
-
126,8
160,7
192,9
179,9
254,8
304,7
113,6
285,1
88,7
111,5
189,6
39,7
76,1
130,6
194,3
222,9
266,2
257,0
197,5
213,7
237,8
167,4
171,2
168,7
33,2
108,1
190,6
109,0
300,0
42,6
27,2
60,8
87,4
146,2
121,0
409,1
130,5
198,6
186,8
173,7
206,5
188,7
70,1
-158,1
205,7
260,6
65,7
26,9
118,2
311,5
191,5
136,4
564,7
149,5
591,9
328,0
29,9
38,0
103,6
378,9
219,9
210,6
307,0
240,2
303,8
205,0
247,0
64,8
41,1
438,0
240,2
311,7
364,5
272,6
296,0
66,2
74,9
31,9
51,6
56,5
52,3
248,1
256,7
97,1
54,4
41,6
43,6
|
-628,6
-2262,8
-1582,0
-1139,0
-528,4
-3376,5
-5015,6
-50,8
68,1
-32,9
-23,5
-17,2
-
-8,4
-0,3
-4,3
8,1
1,1
16,5
-919,5
-166,2
-174,8
-173,1
182,5
-
-656,1
-2118,9
-750,2
-2198,9
-1127,7
-1682,4
-2156,2
-604,2
-896,8
-1437,8
-1798,7
94,2
122,3
-137,1
-394,4
65,1
-2193,2
-3335,9
2784,3
-171,4
-660,1
-661,8
-1879,9
-129,9
-244,3
-704,3
-1014,2
-825,6
-2512,0
-51,2
-94,8
272,8
1,8
-228,6
-237,3
-1142,6
-33,8
19,4
-1029,3
-569,6
-440,4
-1426,0
-1047,5
-3424,3
-1266,8
-3642,9
238,8
-211,6
-763,8
-2463,3
104,1
86,6
140,5
51,5
98,4
42,5
-155,7
-175,7
-260,5
-305,4
-935,7
-1517,2
-189,1
-218,3
-256,9
-519,3
-300,2
-371,2
-1137,6
-559,8
-320,7
|
Приложение 3
Электродные потенциалы
| Уравнение электродного процесса
| Стандартный потенциал при 250 С, В
| Уравнение электродного процесса
| Стандартны потенциал при 250 С, В
| | Li++е-=Li
| -3,045
| Co2++2e-=Co
| -0.277
| | Rb++e-=Rb
| -2,925
| Ni2++2e-=Ni
| -0,250
| | K++e-=K
| -2,924
| Sn2++2e-=Sn
| -0,136
| | Cs++e-=Cs
| -2,923
| Pb2++2e-=Pb
| -0,126
| | Ca2++2e-=Ca
| -2,866
| Fe3++3e-=Fe
| -0,037
| | Na++e-=Na
| -2,714
| 2H++2e-=H2
| -0
| | Mg2++2e-=Mg
| -2.363
| Bi3++3e-=Bi
| 0,215
| | Al3++3e-=Al
| -1,663
| Cu2++2e-=Cu
| 0,337
| | Ti2++2e-=Ti
| -1,630
| Cu++e-=Cu
| 0,520
| | Mn2++2e-=Mn
| -1,179
| Hg22++2e-=2Hg
| 0,788
| | Cr2++2e-=Cr
| -0,913
| Ag++e-=Ag
| 0,799
| | Zn2++2e-=Zn
| -0,763
| Hg2++2e-=Hg
| 0,850
| | Cr3++3e-=Cr
| -0,744
| Pt2++2e-=Pt
| 1,188
| | Fe2++2e-= Fe
| -0,440
| Au3++3e-= Au
| 1,498
| | Cd2++2e-Cd
| -0,403
| Au++e-= Au
| 1,692
| | 2H2O+2e-=H2+2OH-
| -0,828
| O2+2H2O+4e-=4OH-
| 0,401
| | NO3-+10H++8e-= NH4++3H2O
| 0,870
| O2+4H++4e-=2H2O
| 1,228
| | NO3-+2H++e-= NO2++H2O
| 0,780
| SO42-+8H++6e-=S+4H2O
| 0,357
| | NO3-+4H++3e-= NO++2H2O
| 0,957
| SO42-+10H++8e-=H2S+4H2O
| 0,300
|
СОДЕРЖАНИЕ
| Предисловие
|
| | Глава 1. Основные понятия химии. Современная номенклатура неорганических веществ. Химические свойства и способы получения неорганических соединений. Химические реакции
|
| | Основные понятия общей химии
|
| | Важнейшие химические свойства и способы получения оксидов, оснований, кислот, амфотерных гидроксидов и солей
|
| | Химические реакции. Классификация химических реакций
|
| | Примеры решения типовых задач
|
| | Задачи и упражнения для самостоятельной работы
|
| | Контрольная работа № 1
|
| | Глава 2. Строение атома. Периодическая система и Периодический закон Д.И. Менделеева в свете современных представлений о строении атома. Химическая связь. Комплексные соединения
|
| | Строение атома
|
| | Периодический закон и периодическая система Д. И. Менделеева в свете современных представлений о строении атома
|
| | Химическая связь
|
| | Комплексные соединения
|
| | Примеры решения типовых задач
|
| | Задачи и упражнения для самостоятельной работы
|
| | Контрольная работа № 2
|
| | Глава 3. Термодинамика химических процессов
|
| | Основные понятия термодинамики
|
| | Первый закон термодинамики
|
| | Второй закон термодинамики
|
| | Третий закон термодинамики
|
| | Примеры решения типовых задач
|
| | Задачи и упражнения для самостоятельной работы
|
| | Глава 4. Химическая кинетика. Обратимость химических реакций. Химическое равновесие
|
| | Основные понятия химической кинетики
|
| | Факторы, влияющие на скорость химических реакций
|
| | Обратимость химических реакций. Химическое равновесие
|
| | Смещение химического равновесия
|
| | Примеры решения типовых задач
|
| | Задачи и упражнения для самостоятельной работы
|
| | Контрольная работа № 3 по разделам «Термодинамика» и «Химическая кинетика»
|
| | Итоговый тест
|
| | Литература
|
| | Приложение
|
|
Для заметок
Не нашли, что искали? Воспользуйтесь поиском по сайту:
©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|


 h =6,62·10-34 Дж·К-1
h =6,62·10-34 Дж·К-1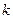 б =1,3805·10-23 Дж·К-1
б =1,3805·10-23 Дж·К-1