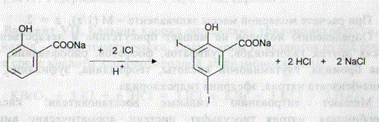
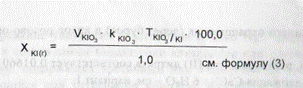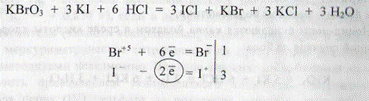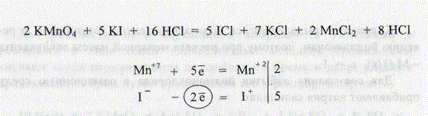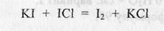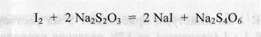|
|
Мл 0,1 н. раствора ртути (II) нитрата соответствует 0,01660 г KIРасчет содержания СаС12 • 6 Н20 - см. вариант I. Расчет содержания KI см. - вариант IV. Помимо приведенных методик определения калия йодида методами осадительного титрования в экспресс-анализе широко применяются окислительно-восстановительные способы титрования. Вариант VI.Кальция хлорид определяют трилонометрически, а калия йодид - методом йодатометрии.
Йодид-ионы окисляются калия йодатом в среде кислоты хлороводородной сначала до йода:
При расчете молярной массы эквивалента - ! Методика. К 1 мл смеси добавляют 5 мл раствора кислоты хлороводородной 1 : 1 (готовится из 37% раствора кислоты хлороводородной), 1 мл раствора крахмала растворимого и быстро" титруют 0,1 н. раствором калия йодата до появления светло бурой окраски. Затем титрование проводят медленно, по каплям, до перехода окраски в лимонно-желтую. 1 мл 0,1 н. раствора калия йодата соответствует 0,005533 г KI.
Расчет содержания СаС12 • 6 Н20 - см. вариант I. Вариант VII.Кальция хлорид определяют трилонометрически, капая йодид - броматометрически. Йодид-ионы окисляются калия брома-гоМ в сРеДе кислоты хлороводородной до йодмонохлорида:
При расчете молярной массы эквивалента-М (1/z), z = 2. Методика.К 1 мл микстуры прибавляют 5 мл раствора кислоты лороводородной 1 : 1 (готовится из 37% раствора кислоты хлороводородной), 1 мл раствора крахмала и титруют 0,1 н. раствором калия 5г)о^ата Д° перехода бурой окраски раствора в лимонно-желтую. 1 мл 0,1 н. раствора калия бромата соответствует 0,0083005 г KI.
Расчет содержания СаС12 • 6 Н20 - см. вариант I. Вариант VIII.Кальция хлорид определяют трилонометрически, каЛйЯ йодид - методом перманганатометрии. Йодид-ионы окисляются калия перманганатом в среде кислоты хлороводородной разведенной:
При расчете молярной массы эквивалента - M (1/z), z = 2. Определению йодидов не мешает присутствие в лекарственных смесях других галогенидов, сульфатов, фосфатов, рибофлавина, тиамина бромида, глутаминовой кислоты, теофиллина, эуфиллина, ко-феина-бензоата натрия, эфедрина гидрохлорида. Мешают титрованию сильные восстановители: кислота аскорбиновая, натрия тиосульфат, цистеин, ароматические амины, фенолы и их производные и другие лекарственные вещества, которые могут реагировать с калия перманганатом или образующимся при титровании йодмонохлоридом. Методика.К 1 мл микстуры прибавляют 5 мл раствора кислоты хлороводородной 1 : 1 (готовится из 37% раствора хлороводолрода) и титруют 0,1 н. раствором калия перманганата до появления светло-бурой окраски раствора. Затем прибавляют 1 мл раствора крахмала растворимого и снова титруют по каплям до перехода окраски в лимонно-желтую. 1 мл 0,1 н. раствора калия перманганата соответствует 0,0083005 г KI.
Расчет содержания СаС12 • 6 Н20 см. вариант I. Вариант IX.Кальция хлорид определяют трилонометрически, калия йодид - методом йодхлорметрии. Сущность метода заключается в следующем: к аликвотной части микстуры, содержащей калия йодид, прибавляют избыток 0,1 н. раствора йодмонохлорида. При этом протекает реакция:
Количество выделившегося йода эквивалентно вступившим в реакцию йодид-ионам, поэтому при расчете молярной массы эквивалента -M(l/z), z = 1. Для связывания избытка йодмонохлорида в реакционную среду прибавляют натрия салицилат:
Через несколько минут выделившийся йод оттитровывают 0,1 н. стандартным раствором натрия тиосульфата:
Йодхлорметрическому определению йодидов не мешают хлориды, но мешают бромиды. Методика.К 1 мл смеси прибавляют избыток (10 - 20 мл) 0,1 н. раствора йодмонохлорида и взбалтывают. Затем прибавляют 100 мл воды и 5 - 10 мл 1% раствора натрия салицилата. Через 3-5 минут выделившийся йод титруют 0,1 н. раствором натрия тиосульфата.
см. формулу (9) Расчет содержания СаСЬ • 6 Н20 - см. вариант I. Вариант X.Анализ можно осуществить с использованием метода рефрактометрии. Вначале проводят трилонометрическое определение кальция хлорида шестиводного, а затем определяют показатель преломления лекарственной смеси относительно воды. Расчет содержания СаСЬ ■ 6 НгО - см. вариант I. Расчет содержания KI см. формулу 97. Для количественного определения хлоридов в сочетании с бромидамив виде солей одновалентных металлов бромид-ионы окисляют калия перманганатом до свободного брома и далее удаляют образовавшийся бром путем превращения его в пентабромацетон:
После этого в растворе остаются только хлорид-ионы, которые определяют по методу Фольгарда. Для определения бромидов сумму галогенидов титруют по методу Мора или определяют меркуриметрическим методом. Примером служит анализ прописи 22. ПРОПИСЬ 22 Натрия бромида 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
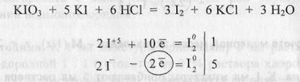
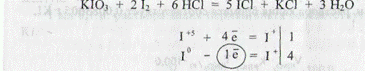
 = 3.
= 3.