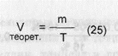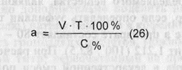|
|
Предварительный расчет расхода титрованного раствора.КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ В СМЕСЯХ В экспресс-анализе для количественного определения ингредиентов смесей применяются титриметрические и физико-химические методы. Из титриметрических методов для указанных целей применяется большинство известных способов титрования (см. таблицу 1). Из физико-химических методов наиболее часто используется рефрактометрия, спектрофотометрия в УФ- и видимой областях. Несмотря на большое разнообразие в химическом строении лекарственных веществ, многие соединения, имеющие одинаковые функциональные группы или элементы структуры, можно определить одними и теми же методами. При количественном анализе нужно не только выбрать наиболее точный и удобный метод, исходя из индивидуальных свойств анализируемого вещества, но и учесть вид лекарственной формы, установить, позволят ли сопутствующие ингредиенты обеспечить необходимую точность, учесть реакцию среды, наличие электролитов, веществ, анализируемых аналогично, и т.д. Поэтому знание альтернативных вариантов определения различными титриметрическими методами, особенностей взаимодействия индикаторов, титрованных растворов при анализе смесей приобретает особое значение. 5.1 Расчеты при анализе титриметрическими методами При анализе многокомпонентных лекарственных форм используют различные варианты титрования: прямое, обратное, заместительное, с контрольным опытом и др. (см. табл. 1). Способы расчета концентраций определяемого ингредиента зависят от вида лекарственной формы, величин эквивалентов (особенно при определении по разности) и т.д. Для самостоятельного составления схемы количественного анализа, а также в целях обеспечения точности определения и экономного расходования реактивов провизору-аналитику необходимо уметь производить предварительные расчеты массы (объема) лекарственной формы, необходимой для анализа, величины разведения, среднего ориентировочного титра, коэффициентов пересчета, теоретического объема титранта, оценивать результаты анализа и делать выводы. Таблица 1. Титриметрические методы, наиболее часто используемые при анализе ингредиентов в лекарственных смесях
Расчеты при титровании Концентрацию ингредиента в смеси в процентах или его содержание рассчитывают в тех единицах, в каких данный ингредиент выписан в прописи. При прямомтитровании концентрацию ингредиентов в процентах (в жидких лекарственных формах, мазях, порошках) рассчитывают по формуле:
где С - концентрация определяемого вещества, в %; V - объем титрованного раствора,в мл; к - коэффициент поправки на титрованный раствор; Т - титр по определяемому веществу (титриметрический фактор пересчета); а - масса (в г) или объем (в мл) анализируемой смеси Титр по определяемому веществу (или титриметрический фактор пересчета) - это масса анализируемого вещества (в г), взаимодействующая с 1 мл титрованного раствора. Титриметрический фактор пересчета рассчитывают по формуле:
где С - молярная концентрация титранта в моль/л;
Титриметрический фактор пересчета - величина постоянная для данного лекарственного вещества, определяемого конкретным титриметрическим методом с известной концентрацией титранта. Поэтому провизоры-аналитики в своей работе пользуются таблицами с указаниями величин титра по определяемому веществу. Содержание ингредиентов в граммах (в жидких лекарственных формах, порошках, мазях) рассчитывают по формулам:
где X - масса определяемого лекарственного вещества, в г; V - объем титрованного раствора, в мл; Vi - объем жидкой лекарственной формы по прописи, в мл; Р - общая масса порошка, мази по прописн, в г; а - объем, в мл, или масса, в г, лекарственной формы, отобранные для анализа; к - поправочный коэффициент. Если при анализе жидкой лекарственной формы предварительно делали разведение и для титрования использовали часть полученного разведения (А), то концентрацию определяемого 'вещества рассчитывают по формуле:
где В - объем мерной колбы, в мл; А - объем разведенного раствора, отобранный для титрования (аликвотная доля), в мл. При необходимости выразить содержание анализируемого вещества в граммах, в числитель вместо цифры 100 подставляют величину общей массы (Р, в г) или объема (Vi, в мл) лекарственной формы:
При обратном титровании(или титровании по избытку) используют два титрованных раствора. Тогда концентрацию ингредиентов в % (в жидких лекарственных формах, мазях, Порошках) рассчитывают по формуле:
где Vi - объем первого титранта, взятого в избытке, в мл; ki - коэффициент поправки на первый титрованный раствор; V2 - объем второго титранта, затраченного на титрование избытка первого титрованного раствора, в мл; кг - коэффициент поправки на второй титрованный раствор; остальные обозначения см. в формуле (1). Содержание ингредиентов в граммах (в жидких лекарственных формах, порошках, мазях) рассчитывают по формулам:
где V3 - объем жидкой лекарственной формы по прописи, в мл; Р - общая масса порошка, мази по прописи, в г; остальные обозначения см. в формуле (1). В экспресс-анализе иногда проводят контрольный (холостой) опыт при прямом и обратном способах титрования. Контрольный опыт в случае прямого титрования проводят при: алкалиметрическом титровании веществ в мазях (контрольный опыт проводится с мазевой основой, обладающей собственной кислот - алкалиметрическом титровании с использованием растворителей,обладающих кислотными свойствами (спирт, ацетон); комплексонометрическом титровании в малых количествах солей В приведенных примерах концентрацию определяемого вещества в процентах и в граммах вычисляют с учетом контрольного опыта по формулам:
где Vo.o - объем титрованного раствора, израсходованный на титрование определяемого вещества, в мл; Ук.о - объем титрованного раствора, израсходованный на титрование контрольного опыта, в мл; Р - масса порошка или мази, в г; остальные обозначения см. в формуле (1). При прямом ацидиметрическом титровании некоторых лекарственных веществ (гексаметилентетрамин, калия ацетат, натрия бензоат и др.) контрольный опыт проводится с целью сравнения перехода окраски индикатора в точке эквивалентности в анализируемом и контрольном растворах. В этом случае количество титрованного раствора, израсходованное на титрование в контрольном опыте, при расчетах не учитывается. В экспресс-анализе проведение контрольного опыта в случае обратного титрованиянеобходимо при: - йодометрическом определении некоторых лекарственных ве - броматометрическом определении препаратов группы фенолов; - при йодхлорметрическом определении метилурацила, этакриди- - перманганатометрическом определении натрия нитрита. вычисляют с учетом контрольного опыта по формулам
где VK о. — объем второго титранта, пошедший на титрование контрольного оптыта, в мл; V0.o. - объем второго титранта, пошедший на титрование основного опыта, в мл; Р -т масса порошка или мази, в г; остальные обозначения см. в формуле (1). Кроме того, контрольный опытставят, если необходимо отфильтровать осадок и титровать избыток раствора в аликвотной части фильтрата. В этом случае расчет ведут по формулам:
где В - объем мерной колбы (в мл); А - объем фильтрата, взятого на титрование (в мл); Р - масса порошка или мази (в г); остальные обозначения см. в формуле (1). При заместительном титровании,т.е. титровании вещества, образующегося в результате реакции в количестве, эквивалентом определяемому компоненту, расчет ведут, как при прямом титровании, но титриметрический фактор пересчета определяют не по титруемому заместителю, а по определяемому веществу. Например, при пропускании через катионитную колонку натрия цитрата образуется эквивалентное количество лимонной кислоты, которую титруют стандартным раствором натрия гидроксида. При расчете титр определяют по натрия цитрату, а не по лимонной кислоте. При определении по разностилекарственные вещества титруют суммарно общим для них методом, а затем один из компонентов анализируют другим методом, при котором второй компонент не мешает определению. Вычисление по разности включает несколько вариантов в зависимости от типа протекающих реакций. Если при титровании разными методами молярные массы эквивалентов - М (1/z) - анализируемых веществ не меняются, то объем тированного раствора (\Л), пошедший на титрование вещества, определяемого по разности, рассчитывают по алгебраической разности между объемом, затраченным на титрование суммы веществ (Vc), и объемом другого титрованного раствора (V2), израсходованного на титрование второго вещества:
I акой расчет справедлив, если при титровании использовали одинаковые массы (объемы) лекарственной смеси и одинаковые концентрации титрованных растворов. Разберем это на примере прописи 16. ПРОПИСЬ 16 Эфедрина гидрохлорида 0,6 Новокаина 0,9 Воды очищеннойдо 120 мл Для количественного определения новокаина и эфедрина гидрохлорида вначале в аликвотной доле титруют сумму двух лекарственных веществ 0,1 н. раствором серебра нитрата:
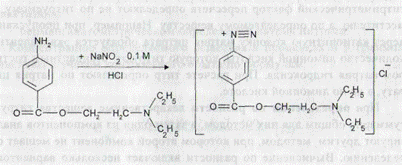
Согласно уравнению реакции, значение "z" при расчете М (1/z) для каждого лекарственного вещества равно 1. Затем проводят второе титрование в аликвотной доле 0,1 М раствором натрия нитрита для определения новокаина:
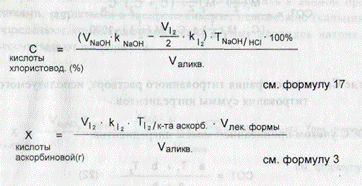
Величина "z" для новокаина и в этой реакции равна 1. Эфедрин в этом случае не мешает определению новокаина и объем 0,1 М раствора натрия нитрита эквивалентен только количеству новокаина. Расчет содержания новокаина проводят по формуле:
Количество эфедрина гидрохлорида рассчитывают по разности между объемом 0,1 н. раствора серебра нитрата (пошедшего на титрование суммы новокаина и эфедрина гидрохлорида) и объемом 0,1 М раствора натрия нитрита, пошедшего на титрование новокаина:
В случае если для количественного определения используют разные массы (объемы)лекарственной смеси, то в расчетной формуле это учитывают следующим образом: предположим, что для определения суммы новокаина и эфедрина гидрохлорида взяли аликвотную долю объемом 2 мл (титрант -.0,1 н. раствор серебра нитрата), а для титрования новокаина - 1 мл (титрант - 0,1 М раствор натрия нитрита), тогда при расчете содержания эфедрина гидрохлорида объем раствора натрия нитрита, пошедший на титрование новокаина, умножают на два и расчетная формула приобретает вид:
см. формулу (17) И наоборот, когда для титрования суммы новокаина и эфедрина гидрохлорида берут 1,0 мл раствора лекарственной формы, а для определения новокаина - 2 мл, то объем натрия нитрита, пошедший на титрование, следует разделить на два:
см. формулу (17) Данные формулы расчета справедливы при использовании титрованных растворов одинаковых концентраций, т.е. в данном случае необходимо только приведение к одному объему аликвотной части или к одной массе. Использование различных концентраций титрованных растворовв процессе количественного определения ингредиентов смеси отражаются в формуле следующим образом: предположим, что для определения суммы новокаина и эфедрина гидрохлорида использовали 0,1 н. раствор серебра нитрата, а для титрования новокаина — 0,02 М раствор натрия нитрита. При этом аликвотные доли в первом и во втором случаях были равны. В данном примере на титрование навески новокаина пойдет в пять раз больше 0,02 М раствора натрия нитрита, чем 0,1 н. раствора серебра нитрата. Поэтому при расчете содержания эфедрина гидрохлорида по разности для приведения объемов титрантов к одной концентрации объем раствора натрия нитрита делят на пять:
см. формулу (17) Более сложным случаем расчета является схема анализа, когда для определения содержания ингредиентов берут разные аликвотные долии титрование проводят стандартными растворами различной концентрации.
Например, для анализа новокаина берут аликвотную долю 2,0 мл и титрование проводят 0,02 М раствором натрия нитрита; сумму новокаина и эфедрина гидрохлорида определяют в аликвотной доле 0,5 мл и титрование проводят 0,1 н. раствором серебра нитрата. Для пересчета объема 0,02 М раствора натрия нитрита, эквивалентного 0,1 н. раствору серебра нитрата, объем натрия нитрита делят на пять. Объем раствора натрия нитрита при определении новокаина в 2,0 мл смеси будет в четыре раза превышать объем этого же титранта, пошедший на титрование новокаина в навеске, равной 0,5 мл смеси. Расчет по разности приобретает следующий вид: Т.е. в данном случае необходимо сделать приведение к одному объему аликвотной доли и одной концентрации титрантов. При использовании расчетов по разностинеобходимо максимально устранить неточности при определении сопутствующих ингредиентов (особенно если их три и более в составе одной смеси), так как допущенные ошибки существенно сказываются на результате количественного определения вещества, рассчитываемого по разности. Примером может служить пропись 2 ( жидкость Полосухина; состав см. выше). При разработке схемы количественного анализа необходимо учесть, как определить по разности вещество, содержащееся в прописи в значительно большем количестве. Так, определение натрия тиосульфата проводят методом йодометрии, кальция хлорид титруют раствором трилона Б, а натрия хлорид определяют по методу Фольгарда. Количества натрия тиосульфата и кальция хлорида рассчитывают раздельно по объемам йода (Vl2) и трилона Б (VTp.B)- Количество натрия хлорида рассчитывают по разности: (VAgN03 - VNH4cns) - (Vj, - VTp.e)
см. формулу 17 где V-i — объем 0,1 н. раствора серебра нитрата, взятого в избытке, в мл; . V2 — объем 0,1 н. раствора аммония роданида, пошедшего на титрование избытка серебра нитрата, в мл; V3 — объем 0,1 н. раствора йода, пошедшего на титрование натрия тиосульфата, в мл; V4 - объем 0,01 М раствора трилона Б, пошедшего на титрование кальция хлорида, в мл. Концентрация трилона Б выражена в молярных единицах, а остальных растворов - в виде нормальной концентрации. Поскольку при титровании кальция хлорида раствором трилона Б значение «z» равно 2, необходимо молярную концентрацию трилона Б (См) перевести в нормальную (CN) и только после этого объем трилона Б использовать при вычислении по разности:
Если при титровании разными методами эквиваленты анализируемых веществ меняются,важно правильно рассчитать количества титрантов. Примером служит пропись 17. ПРОПИСЬ 17 Раствора кислоты хлористоводородной 1% - 200,0 мл Кислоты аскорбиновой 1,0 Вначале определяют сумму кислот титрованием 0,1 н. раствором натрия гидроксида. При этом значение величины «z» при расчете молярной массы эквивалента М (1/z) для каждого вещества равно 1.
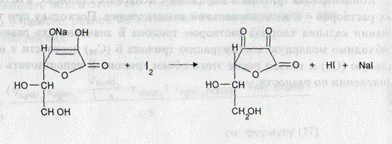
Количество натрия гидроксида эквивалентно сумме кислоты хлористоводородной и кислоты аскорбиновой. Далее для определения кислоты аскорбиновой полученный аскорбинат натрия титруют 0,1 н. раствором йода.
При титровании кислоты аскорбиновой 0,1 н. раствором йода значение величины «z» при расчете М (1/z) равно 2, а это означает, что на одну и ту же аликвотную долю смеси будет расходоваться 0,1 н. раствора йода в два раза больше, чем 0,1 н. раствора натрия гидроксида. Поэтому при расчете количества раствора, пошедшего на титрование кислоты хлористоводородной, из общего объема 0,1 н. раствора гидроксида натрия следует вычесть Уг объема 0,1 н. раствора йода, израсходованного на титрование кислоты аскорбиновой:
Содержание в лекарственных смесях веществ близких по химическому строению и свойствам (соли галогеноводородных кислот, сульфаниламиды и др.) затрудняет их раздельное определение общепринятыми титриметрическими методами. Как исключение в подобных случаях допускается применять средний ориентировочный титр(СОТ) для определения суммы веществ. СОТ - это масса смеси определяемых веществ в граммах, соответствующая 1 мл титранта. Его величина зависит от значений титриметрических факторов пересчета ингредиентов смеси и соотношения этих веществ в лекарственной смеси. Существует несколько способов расчета СОТ: > Упрощенный вариант:
где Ci, Сг ...С„ - концентрации веществ, входящих в лекарственную смесь; T-i, Т2 ... Тп - титриметрические факторы пересчета (титры по определяемому веществу) веществ.
где См - концентрация титрованного раствора, используемого для титрования суммы ингредиентов. > С учетом прописанной массы ингредиентов:
где Ti — титр по определяемому веществу первого ингредиента; Тг - титр по определяемому веществу второго ингредиента; а - прописанная масса первого ингредиента, в г; Ь - прописанная масса второго ингредиента, в г. > С учетом различных количеств ингредиентов:
обозначения - см. формулу (22) Использование в расчетах среднего ориентировочного титра рассматривается на примере раствора Рингера (пропись 18). ПРОПИСЬ 18 Раствор Рингера Состав: Натрия хлорида 0,9 Калия хлорида 0,02 Кальция хлорида 0,02 Натрия гидрокарбоната 0,02 Воды для инъекций до 100,0 мл Натрия и калия хлориды раздельно определить в данной прописи методиками, принятыми в экспресс-анализе, невозможно (кальция хлорид определяют комплексиметрически). Сумму хлоридов натрия и калия рассчитывают по формуле:
где \/Адмоз- объем 0,1 н. раствора серебра нитрата, пошедший на титрование суммы хлоридов натрия, калия и кальция; Vjp.B - объем трилона Б, пошедший на титрование кальция хлорида; Тддыоз/ыаСкка - средний ориентировочный титр (СОТ) при титровании натрия и калия хлоридов 0,1 н. раствором серебра нитрата. Значение СОТ 0,1 н. раствора серебра нитрата для суммы натрия и калия хлоридов рассчитывают следующим образом:
Например, кофеин-бензоат натрия в экспресс-анализе чаще анализируют по бензоату натрия, которого в препарате должно быть 58 -62%. Если пользоваться титром 0,01441 г/мл, исходя из М.м. натрия бензоата (144,1 г/моль) и титрантом - 0,1 н. раствором кислоты хлороводородной, то в результате получим содержание натрия бензоата в лекарственной форме. Для пересчета на кофеин-бензоат натрия полученный результат нужно дополнительно поделить на фактическое содержание (массовую долю) натрия бензоата в кофеине-бензоате натрия. Чтобы не делать громоздких расчетов, можно использовать так называемый условный титр,пересчитанный на препарат. Для кофеина-бензоата натрия его определяют по формуле:
Величина Тусловн. может значительно колебаться. При содержании в кофеине-бензоате натрия 58% натрия бензоата Тусловн = 0,02484,а при 62% Тусловн= 0,02324.Поэтому для определения Тусловн. необходимо знать содержание натрия бензоата в препарате. Если таких данных нет, расчеты следует вести по среднему пределусодержания данного компонента в препарате. Так, при титровании 0,1 н. раствором кислоты хлороводородной эуфиллина по этилендиа-мину (содержание которого в комплексе находится в пределах 14 — 18%) I усповн. равен:
где 0,003005 - масса этилендиамина (в г), соответствующая 1 мл 0,1 н. раствора кислоты хлороводородной. Коэффициент пересчета.При анализе комплексных соединений, состоящих из двух веществ, чаще пользуются коэффициентом пересчета на определяемое вещество. Коэффициент пересчета - частное от деления массы (или 100%) всего комплексного соединения на массу (или массовую долю) определяемого вещества, являющегося компонентом комплекса. Например, если определять эуфиллин титрованием по тео-филлину (содержание в препарате составляет 80 - 85%), то коэффициент пересчета составит 1,212 (100 : 82,5). При расчете количественного содержания эуфиллина в лекарственной смеси полученный результат нужно умножить на данный коэффициент, а при количественном определении препарата по этилендиамину коэффициент пересчета на эуфиллин (при содержании этилендиамина 16%) составит 6,25 (100 : 16). Предварительный расчет расхода титрованного раствора. Предварительный расчет объема титрованного раствора (\/те0рет.), который должен быть затрачен на титрование массы (объема) лекарственной смеси, в экспересс-анализе имеет важное значение. Так, при составлении схемы анализа химик-аналитик должен четко представлять теоретические объем титранта, и если VTe0peT. составляет менее 0,5 мл, а массу (объем) аликвотной доли увеличить нельзя, следует сделать разведение исходного титрованного раствора. Условия выполнения количественного определения ингредиентов лекарственной смеси необходимо подбирать сучетом того, чтобы VTeopeT. составлял не менее 1 мл (чтобы не увеличивать ошибку определения). Значение Утеорет. можно рассчитать по формуле:
где m - содержание лекарственного вещества (в г) в 1 мл смеси. Предварительный расчет массы (объема) лекарственной смеси, необходимый для анализа. Вцелях экономии титрованного раствора и для повышения точности анализа перед титрованием целесообразно рассчитывать предварительную массу (объем) лекарственной смеси (а), чтобы при титровании был израсходован определенный объем стандартного раствора (V):
В порошках (мазях, суппозиториях) вместо 100% подставляют величину общей массы порошка (мази, суппозиториев), а вместо С% - X в граммах (формула 4). 5.2. АНАЛИЗ СМЕСЕЙ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ БЕЗ РАЗДЕЛЕНИЯ КОМПОНЕНТОВ Составление схемы количественного определения ингредиентов смеси. При разработке схемы анализа смеси целесообразно привести все существующие методики количественного определения (фармакопейные и нефармакопейные) каждого ингредиента смеси в отдельности. В качестве примера составим схему количественного определения ингредиентов прописи 19. ПРОПИСЬ 19 Калия йодида 4,0 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|

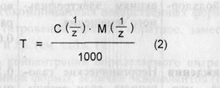
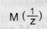 - молярная масса эквивалента определяемого вещества в г/моль.
- молярная масса эквивалента определяемого вещества в г/моль.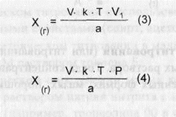
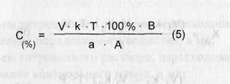

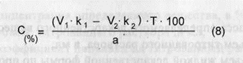
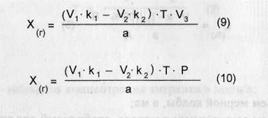
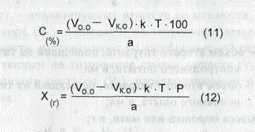
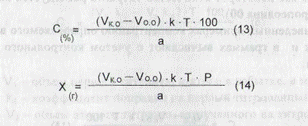

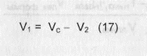







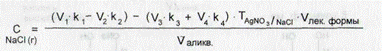



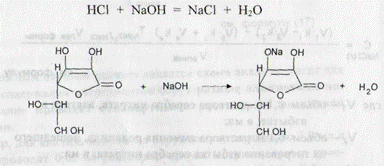
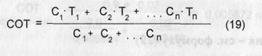

 Р При более точных определениях, а также при расчете СОТ для лекарственных смесей по авторским прописям:
Р При более точных определениях, а также при расчете СОТ для лекарственных смесей по авторским прописям: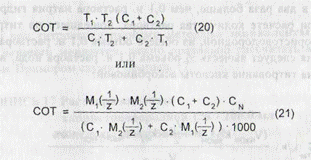
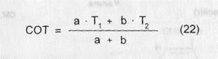
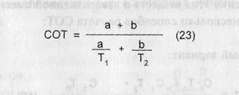



 Условный титр.Некоторые лекарственные вещества представляют собой комплексные соединения, состоящие из двух веществ (кофе-ин-бензоат натрия, эуфиллин, темисал и др.). Такие соединения в лекарственных смесях можно определять по входящим в них компонентам, содержание которых согласно требованиям ГФ и др. НД должно быть в строго определенных пределах.
Условный титр.Некоторые лекарственные вещества представляют собой комплексные соединения, состоящие из двух веществ (кофе-ин-бензоат натрия, эуфиллин, темисал и др.). Такие соединения в лекарственных смесях можно определять по входящим в них компонентам, содержание которых согласно требованиям ГФ и др. НД должно быть в строго определенных пределах. где а - содержание натрия бензота в данном образце кофеина-бензоата натрия (в %); 0,01441 - масса натрия бензоата (в г), соответствующая 1 мл 0,1 н. раствора кислоты хлороводородной.
где а - содержание натрия бензота в данном образце кофеина-бензоата натрия (в %); 0,01441 - масса натрия бензоата (в г), соответствующая 1 мл 0,1 н. раствора кислоты хлороводородной.