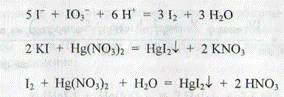|
|
Способы определения хлоридов и бромидов при совместном присутствии
Расчет содержания лекарственных веществ проводят по разности (в случае суммарного титрования йодидов и хлоридов), или по формуле прямого титрования (если йодиды и хлориды определяют отдельно). В экспресс-анализе для количественного определения йодидов и хлоридов часто используют сочетание приведенных титриметрических методов с рефрактометрией. Рассмотрим приведенную схему титрования на примере прописи 21. ПРОПИСЬ 21 Кальция хлорида 3,0 Калия йодида 2,0 Воды очищенной 100,0 мл Вариант I.Кальция хлорид определяют трилонометрически, а калия йодид - по методу Фаянса с индикатором эозинатом натрия (хлорид-ионы не мешают титрованию с индикатором эозинатом натрия). Методика.Кальция хлорид. К 2 мл микстуры прибавляют 4 - 5 мл аммиачного буферного раствора, 0,1 г индикаторной смеси или 5-7 капель раствора кислотного хром темно-синего и титруют 0,05 М раствором трилона Б до сине-фиолетового окрашивания. 1 мл 0,05М раствора трилона Б соответствует 0,01095 г СаС12-6Н20
Калия йодид. К 2 мл микстуры прибавляют 1 мл разведенной кислоты уксусной, 3-5 капель раствора натрия эозината и титруют 0,1 н. раствором серебра нитрата до ярко-розового окрашивания осадка.
1 мл 0,1 н. раствора серебра нитрата соответствует 0,01660 г KI Вариант II.Кальция хлорид определяют трилонометрически, а ка лия йодид - методом аргетометрии с применением внешнего индика тора. Определение конечной точки титрования основано на реакци: йодидов с нитритом натрия в кислой среде:
Титрование стандартным 0,1 н. раствором серебра нитрата прово дят до тех пор, пока капля реакционной среды, нанесенная на нитрозе крахмальную бумагу, не будет вызывать ее посинения вследствие вы деления йода. ,Д,ля получения более точных результатов необходимо предвари тельно рассчитать объем 0,1 н. титрованного раствора серебра нитрата который должен пойти на титрование взятой навески. Можно такж провести вначале ориентировочное титрование. В данном случае \Леорет. 0,1 н. раствора серебра нитрата, необходи мый для титрования 1 мл микстуры с содержанием 0,02 г калия йодид; рассчитывают по формуле:
Следует отметить, что определению йодидов по реакции с натри нитритом не мешают хлориды и бромиды. Кроме приведенных вариантов аргентометрического титрованиз возможно определять сумму калия йодида и кальция хлорида по м« тоду Фольгарда или Фаянса (с индикатором бромфеноловым синим), затем содержание калия йодида рассчитывать по разности между объе мом титрованного раствора, израсходованным на титрование сумм: галогенидов, и объемом трилона Б, пошедшим на титрование кальци хлорида:
Определение СаС12 • 6 Н20 проводят трилонометрически (расчет -см. вариант I). Вариант III.Йодкрахмальный метод Кольтгофа используют для определения йодидов в присутствии хлоридов и бромидов. В реакционную смесь, содержащую йодиды, прибавляют 1 каплю 0,1 н. раствора калия йодата, раствор крахмала и раствор серной кислоты разведенной. В результате реакции образуется йод, окрашивающий крахмал в синий цвет:
Окрашивание йодкрахмального комплекса устойчиво лишь в присутствии йодид-ионов. Если их связать серебра нитратом, синяя окраска раствора исчезает. На резкость изменения окраски влияет количество прибавленной воды. В экспресс-анализе объем раствора должен быть около 15 мл. Метод дает хорошие результаты при титровании йодидов в присутствии хлоридов, если концентрация последних не превышает концентрацию йодидов более чем в три раза. Метод также удобен при определении йодидов в присутствии алкалоидов пуринового ряда и других оснований, барбитуратов, оснований. Однако его нельзя применять для анализа, содержащих лекарственные вещества, с которыми может взаимодействовать йод (кислота аскорбиновая, натрия салицилат и др.). В присутствии бромидов титрование затруднено, а переход окраски от синей через серую до желтой наступает не резко. Поэтому до прибавления раствора кислоты серной к реакционной смеси приливают 5 мл 10% раствора аммония карбоната. Методика.Калия йодид. К 2 мл микстуры прибавляют 10 - 15 мл воды, 1 каплю 0,1 н. раствора калия йодата, 2 мл свежеприготовленного раствора крахмала и по каплям серную кислоту разведенную до появения синего окрашивания жидкости. Далее титруют 0,1 н. раствором серебра нитрата до перехода синего окрашивания в желтое. 1 мл 0,1 н. раствора серебра нитрата соответствует 0,0166 г KI. Расчеты содержания калия йодида и кальция хлорида шестивод-ного - см. вариант I. Вариант IV.Количественное определение обоих компонентов можно провести методом меркуриметрии в одной навеске. Калия йодид определяют безындикаторным методом Кольтгофа, основанным на растворении оранжевого осадка ртути дийодида в избытке калия йодида с образованием бесцветного комплекса.
После того как все свободные йодиды перейдут в комплекс тет-райодмеркурата калия, избыточная капля титрованного раствора ртути (II) нитрата, вступая во взаимодействие с частью комплексного иона, вновь образует нерастворимый оранжевый осадок ртути дийодида, свидетельствующий о конце титрования.
При определении без индикатора йодид-ионы взаимодействуют фактически до комплексного соединения K2[Hgl4], поэтому в данном случае z = 2. Для определения кальция хлорида к оттитрованной жидкости прибавляют в качестве индикатора раствор дифенилкарбазона и титруют стандартным раствором ртути(П) нитрата до фиолетового окрашивания. При этом ртути (II) нитрат сначала разрушает полученное ранее комплексное соединение:
Затем взаимодействует с кальция хлоридом: „
Избыточная капля ртути (II) нитрата реагирует с дифенилкарбазоном, образуя комплекс фиолетового цвета:
Методика. Калия йодид. 2 мл микстуры титруют 0,1 н. раствором ртути (II) нитрата до появления не исчезающей красно-оранжевой мути. 1 мл 0,1 н. раствора ртути (И) нитрата соответствует 0,03320 г KI
Где \/нд(ыоз)2 - объем 0,1 н. раствора ртути (И) нитрата, пошедший на титрование калия йодида (в мл). Кальция хлорид. К оттитрованной жидкости прибавляют 5-7 ка- .... раствора дифенилкарбазона, 1 - 2 капли раствора кислоты азотной |М ин-денной и титруют 0,1 н. раствором ртути (II) нитрата до фиолето-101 о окрашивания. I мл 0,1 н. раствора ртути (И) нитрата соответствует 0,01095 г i ,i( I.-6 П,0
Vbig(N03)2 - объем 0,1 н. раствора ртути (II) нитрата, пошедший на титрование калия йодида, в мл; ViHg(N03)2- объем 0,1 н. раствора ртути (II) нитрата, пошедший на титрование суммы калия йодида и кальция хлорида, в мл
Барбитураты и сульфаниламиды также образуют осадки с солями jlg2+, но при подкислении раствором кислоты азотной (по бромфеполо-рому синему) титрование возможно в их присутствии (лучше с добавлением эфира). Соли Hg2+ способны восстанавливаться до металлической ртути f восстановители (кислота аскорбиновая, натрия тиосульфат и др.), поэтому меркуриметрическое титрование в их присутствии общепринят ?ьшИ методиками невозможно. Влияние кислоты аскорбиновой МОЖНО исключить прибавлением эквивалентного количества титрованного раствора церия (IV) сульфата до появления неисчезающего желтого окрашивания. Вариант V. Кальция хлорид определяют тригонометрически, а (еялия йодид - йодкрахмальным методом (с применением в качес IH нитрованного раствора ртути (И) нитрата). Механизм реакции аналогичен титрованию йодидов по MOTOflj) ]{ольтгофа с применением в качестве титранта раствора серебра нитрата. Точку эквивалентности устанавливают по исчезновению окраски |одкрахмального комплекса, синяя окраска которого изменяется через буроватую до чистой розовато-оранжевой:
Титрованию калия йодида не мешают кислота борная, рибофлавин, эуфиллин, натрия бензоат, натрия гидрокарбонат, прозерин. Методика. Калия йодид. К 2 мл микстуры прибавляют 2 мл воды, ) каплю 0,1 н. раствора калия йодата, 0,5 мл раствора крахмала растворимого, по каплям серную кислоту разведенную до появления устойчивого синего окрашивания и титруют 0,1 н. раствором ртути"(II) нитрат до перехода синего окрашивания (через бурое) в яркое розово-оранжевое. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|

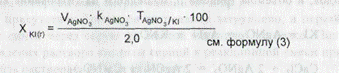
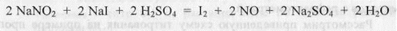



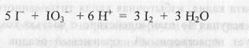
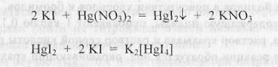

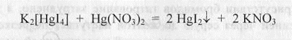
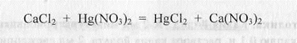


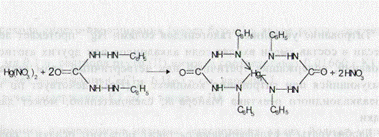



 Титрование указанных галогенидов солями Hg протекает легко, jio если в состав смеси входят соли алкалоидов или других азотистых оснований, содержащих третичный или четвертичный атом азота, то образующийся при титровании комплекс K2[HgI4] действует по типу общеалкалоидного реактива Майера и, следовательно, может давать осадки.
Титрование указанных галогенидов солями Hg протекает легко, jio если в состав смеси входят соли алкалоидов или других азотистых оснований, содержащих третичный или четвертичный атом азота, то образующийся при титровании комплекс K2[HgI4] действует по типу общеалкалоидного реактива Майера и, следовательно, может давать осадки.
 + 0,854 v), если в лекарственную смесь входят сильные
+ 0,854 v), если в лекарственную смесь входят сильные