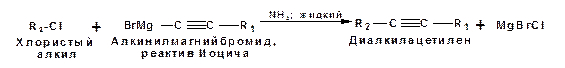|
|
Гидратация (или реакция Кучерова)Алкины присоединяют воду в присутствии сульфата ртути (II). При этом из ацетилена получается уксусный альдегид:
Ненасыщенный радикал СН2=СН- называется винил. Реакция гидратации ацетилена протекает через стадию ненасыщенного винилового спирта или енола, в котором гидроксигруппа связана с атомом углерода в состоянии sp2-гибридизации. По правилу Эльтекова подобная структура является неустойчивой и изомеризуется карбонильное соединение. Енол и карбонильное соединение находятся в равновесии. Взаимопревращение енола и карбонильного соединения является примером так называемой кето-енольной таутомерии или кето-енольного таутомерного равновесия. Участники этого равновесия различаются положением атома водорода и кратной связи. К гомологам ацетилена вода присоединяется по правилу Марковникова. Продуктами гидратации гомологов ацетилена являются кетоны:
Нуклеофильное присоединение.
В силу более высокой электроотрицательности атома углерода, в состоянии sp-гибридизации, по сравнению с атомом углерода в состоянии sp2гибридизации, алкины, в отличии от алкенов могут вступать в реакции нуклеофильного присоединения. Реакциями нуклеофильного присоединения (реакции тип АdN) называют реакции присоединения, в скоростьлимитирующей стадии которых атакующей частицей является нуклеофил. Примером нуклеофильного присоединения является присоединение спиртов к алкинам в присуствии щелочи (реакция Фаворского, 1887г.):
Механизм реакции нуклеофильного присоединения к тройной связи включает следующие стадии: 1. На первой стадии по кислотно-основной реакции образуется алкоголят-анион или алкоксид-ион, являющийся сильным основанием:
2. На второй стадии алкоксид-ион присоединяется к алкину. Эта стадия является скоростьлимитирующей. Причем, если алкин несимметричный, то присоединение протекает в соответствии с правилом Марковникова, а именно: анион, будучи нуклеофильной частицей, присоединяется к наименее гидрогенизированному атому углерода:
3. На третьей стадии образовавшийся карбанион отщепляет протон от другой молекулы спирта, что приводит к образованию эфира и регенерации алкоголят-аниона:
Образовавшийся виниловый эфир может присоединить еще одну молекулу спирта. При этом образуется соединение называемое ацеталем:
Винилирование.
Реакция образование виниловых эфиров из ацетилена и спиртов является примером так называемых реакций вининилирования. К числу этих реакций относятся: 1. Присоединение к ацетилену хлористого водорода:
2. Присоединение к ацетилену синильной кислоты в присутствии солей меди:
3. Присоединение к ацетилену уксусной кислоты в присутствии фосфорной кислоты:
Гидрирование
В условиях гетерогенного катализа алкины присоединяют водород аналогично алкенам:
Первая стадия гидрирования более экзотермична (протекает с большим выделением тепла), чем вторая, что обусловлено большим запасом энергии в ацетилене, чем в этилене:
Окисление. Алкины подобно алкенам окисляются по месту тройной связи. Окисление идет в жестких условиях с полным разрывом тройной связи и образованием карбоновых кислот. Аналогично исчерпывающему окислению олефинов. В качестве окислителей применяют перманганат калия при нагревании или озон:
Следует отметить, что при окислении терминальных алкенов и алкинов одним из продуктов окисления является углекислый газ. Его выделение можно наблюдать визуально и тем самым можно отличить терминальные от внутренних ненасыщенных соединений. При окислении последних выделение углекислого газа не будет наблюдаться.
Полимеризация.
Ацетиленовые углеводороды способны к полимеризации в нескольких направлениях: 1. Циклотримеризация ацетиленовых углеводородов, с использованием активированного угля (по Зелинскому) или комплексного катализатора из дикарбонила никеля и фосфорорганического соединения (по Реппе). В частности из ацетилена получается бензол:
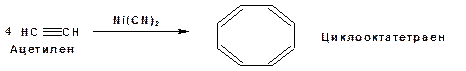
В присутствии цианида никеля ацетилен претерпевает циклотетрамеризацию:
В присутствии солей меди происходит линейная олигомеризация ацетилена с образованием винилацетилена и дивинилацетилена:
Кроме всего того, алкины способны к полимеризации с образованием сопряженных полиенов:
Реакции замещения. Металлирование При действии очень сильных оснований алкины, имеющие концевую тройную связь, полностью ионизируются и образуют соли, которые называются ацетиленидами. Ацетилен реагирует как более сильная кислота и вытесняет более слабую кислоту из ее соли:
Ацетилениды тяжелых металлов, в частности меди серебра, ртути, являются взрывчатыми веществами. Алкинид-анионы (или ионы), входящие в состав ацетиленидов являются сильными нуклеофилами. Это свойство нашло применение в органическом синтезе для получения гомологов ацетилена с использованием галогеналкилов:
Кроме ацетилена подобное превращение можно провести для других алкинов, имеющих концевую тройную связь. Гомологи ацетилена или терминальных алкинов можно получить другим путем. С использованием так называемого реактива Иоцича. Реактив Иоцича получают из реактива Гриньяра:
Далее проводят реакцию реактива Гриньяра с алкином, имеющим концевую двойную связь.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|

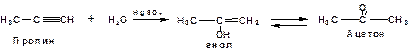
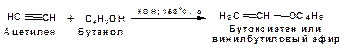
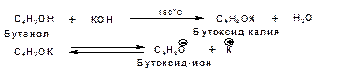

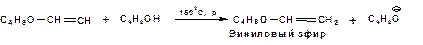
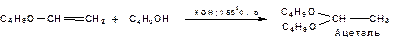
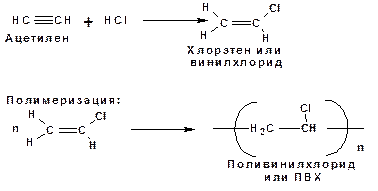
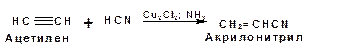
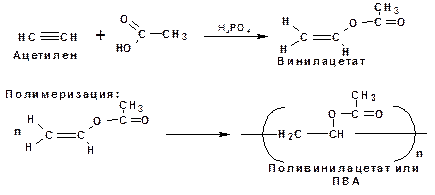
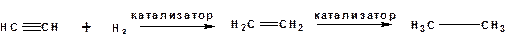
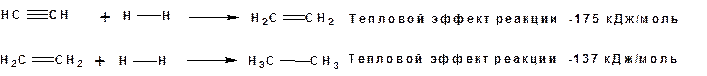 В качестве гетерогенных катализаторов, как и при гидрировании алкенов, используют платину, палладий, никель. Причем гидрирование алкена протекает значительно быстрее, чем гидрирование алкина. Чтобы замедлить процесс гидрирования алкена применяют так назывваемые «отравленные» катализаторы. Замедление скорости гидрирования алкена достигается за счет добавки оксида или ацетата свинца к палладию. Гидрирование на палладие с добавкой солей свинца приводит к образованию цис-олефина. Гидрирование действием металлического натрия в жидком аммиаке приводит к образованию транс-олефина.
В качестве гетерогенных катализаторов, как и при гидрировании алкенов, используют платину, палладий, никель. Причем гидрирование алкена протекает значительно быстрее, чем гидрирование алкина. Чтобы замедлить процесс гидрирования алкена применяют так назывваемые «отравленные» катализаторы. Замедление скорости гидрирования алкена достигается за счет добавки оксида или ацетата свинца к палладию. Гидрирование на палладие с добавкой солей свинца приводит к образованию цис-олефина. Гидрирование действием металлического натрия в жидком аммиаке приводит к образованию транс-олефина.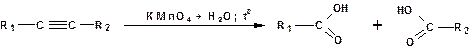
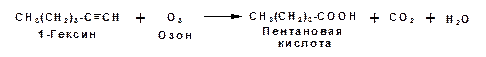


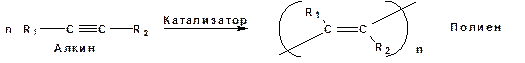
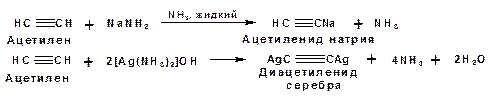
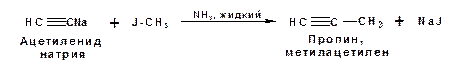

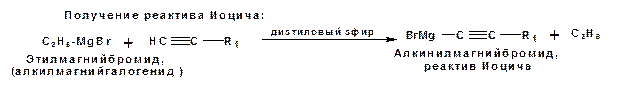 Полученный реактив Иоцича в среде высокополярных апротонных растворителей или в жидком аммиаке взаимодействует с другим галоидным алкилом:
Полученный реактив Иоцича в среде высокополярных апротонных растворителей или в жидком аммиаке взаимодействует с другим галоидным алкилом: