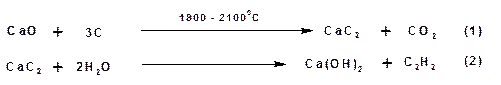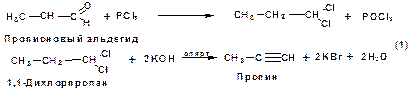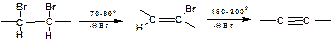|
|
Алкилирование рассмотрим далее.Номенклатура Алкинами, ацетиленовыми углеводородами называют углеводороды, в состав молекул которых входят как минимум два углеродных атома, находящиеся в состоянии sp-гибридизации и соединенные друг с другом тремя связями. Алкины образуют гомологический ряд с общей формулой СnН2n-2. Первым членом гомологического ряда является ацетилен имеющий молекулярную формулу С2Н2 и структурную формулу СНºСН. В силу особенности sp-гибридизации молекула ацетилен имеет линейное строение. Наличие двух π-связей расположенных в двух взаимно перпендикулярных плоскостях предполагает расположение α-атомов замещающих групп на линии пересечения плоскостей, в которых расположены π-связи. Поэтому связи атомов углерода, затраченные на соединение с другими атомами или группами жестко расположены на линии под углом 1800 друг к другу. Строение системы тройной связи в молекулах алкинов определят их линейное строение. Особенность строения молекул алкинов предполагает существование изомерии положения тройной связи. Структурная изомерия, обусловленная строением углеродного скелета, начинается с пятого члена гомологического ряда. 1. Изомерия положения тройной связи. Например:
2. Структурные изомеры. Например:
Первый член гомологического ряда носит тривиальное название «ацетилен». По рациональной номенклатуре ацетиленовые углеводороды рассматриваются как производные ацетилена, Например:
Тройная связь может быть концевой (терминальной, например, в пропине) или «внутренней», например в 4-метил-2-пентине. При составлении названий радикал -СºСН называют «этинил».
Способы получения. 2.1 Промышленные способы. В промышленных условиях получают главным образом ацетилен. Существуют два способа получения ацетилена. Карбидный способ получения ацетилена Ацетилен впервые карбидным способом был получен Фридрихом Велером в 1862г. Появление карбидного способа положило начало широкому применению ацетилена, в том числе и в качестве сырья в органическом синтезе. До настоящего времени карбидный способ является одним из основных промышленных источников ацетилена. Способ включает две реакции:
Пиролиз этилена и метана Пиролиз этилена и метана при очень высокой температуре ведет к получению ацетилена. В этих условиях ацетилен термодинамически нестабилен, поэтому пиролиз проводят за очень короткие интервалы времени (сотые секунды):
Термодинамическая нестабильность ацетилена (взрывается даже при сжатии) следует из высокого положительного значения теплоты его образования из элементов:
Это свойство создает определенные трудности при хранении ацетилена и работе с ним. Для обеспечения безопасности и упрощения работы с ацетиленом используют его свойство легко сжижаться. Сжиженный ацетилен растворяют в ацетоне. Раствор ацетилена в ацетоне хранят в баллонах, наполненных пемзой или активированным углем. Такие условия хранения предотвращают возможности произвольного взрыва.
Лабораторные методы В лабораторных условиях ацетиленовые углеводороды получают также двумя путями: 1. Алкилирование ацетилена. 2. отщепление галогенводородов от поли (много)галогенпроизводных алканов. Алкилирование рассмотрим далее.
Дегидрогалогенирование дигалогенидов и галогеналкенов. Обычно используют геминальные из карбонильных соединений (1) и вицинальные дигалогениды, которые получаются из алкенов (2). Например:
В присутствии спиртовой щелочи реакция дегидрогалогенирования идет в две стадии:
При умеренных температурах (70-800С) реакция останавливается на стадии получения винилгалогенида. Если реакция протекает в жестких условиях (150-2000С), то конечным продуктом является алкин. Физические свойства. Физические свойства алкинов соответствуют физическим свойствам алкенов. Следует отметить, что алкины обладают более высокими температурами плавления и кипения. Терминальные алкины имеют более низкие температуры плавления и кипения, чем внутренние.
Химические свойства. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|

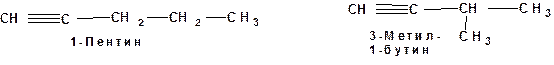
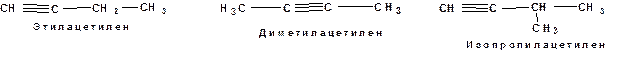 По номенклатуре ИЮПАК названия алкинов образуются заменой суффикса «ан» на «ин». Главную цепь выбирают таким образом, чтобы в нее попала тройная связь. Нумерацию углеродных атомов начинают с того конца цепи, к которому ближе тройная связь. При наличии в молекуле двойной и тройной связей двойная связь имеет меньший номер. Например:
По номенклатуре ИЮПАК названия алкинов образуются заменой суффикса «ан» на «ин». Главную цепь выбирают таким образом, чтобы в нее попала тройная связь. Нумерацию углеродных атомов начинают с того конца цепи, к которому ближе тройная связь. При наличии в молекуле двойной и тройной связей двойная связь имеет меньший номер. Например: