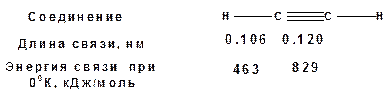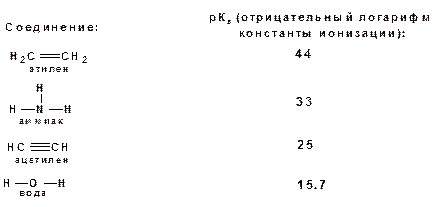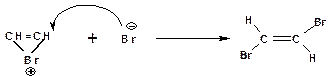|
|
Пространственное и электронное строение.В соответствии с состоянием sp-гибридизации молекула ацетилена линейна.
Энергия тройной связи 829 кДж/моль, что больше энергии двойной связи 607.1 кДж/моль, ординарной связи Сsp3–Сsp3 - 349.6 кДж/моль и ординарной связи Сsp3–Сsp2 - 360 кДж/моль. Однако две ординарные связи и одна двойная, а также четыре ординарные связи по энергии превосходят одну тройную связь. Поэтому тройная связь легко переходит в две ординарные и одну двойную связь путем присоединения по месту тройной связи двух атомов или атомных групп. Из этого следует, что для алкинов, также как и для алкенов, наиболее характерны реакции присоединения. Однако то, что атомы углерода, связанные тройной связью, находятся в состоянии sp-гибридизации, придает алкинам определенные особенности в химических свойствах. В первой лекции отмечалось, что с понижением степени гибридизации растет электроотрицательность атома углерода. Наибольшая электроотрицательность атома углерода в состоянии sp-гибридизации приводит к тому, что алкины обладают способностью не только выступать в роли нуклеофила в реакциях электрофильного присоединения (подвергаться атаке электрофильных частиц), но и выступать в роли электрофила (подвергаться атаке нуклеофильных частиц). Т.е. участвовать в реакциях нуклеофильного присоединения. Повышенная электроотрицательность атома углерода в состоянии sp-гибридизации также приводит к тому, что терминальные алкины являются так называемыми С-Н – кислотами (способны к электролитической диссоциации по связи С-Н). В результате ионизации образуется устойчивый карбанион:
Причем алкины являются кислотами более сильными, чем этилен и аммиак, и более слабыми, чем вода:
Причина более высокой кислотности алкинов по сравнению с алкенами заключается в большей устойчивости соответствующего карбаниона. Следствием возможности образования стабильного карбаниона - является способность терминальных алкинов участвовать в реакциях замещения.
Электрофильное присоединение.
Галогенирование Электрофильное присоединение (AdE) галогенов: хлора, брома йода к ацетиленам идет с меньшей скоростью, чем к олефинам. При этом образуются транс-дигалогеналкены. Дальнейшее присоединение галогенов идет с еще более низкой скоростью: Например, присоединение брома к этилену с образованием 1,1,2,2-тетрабромэтана в среде уксусной кислоты:
Механизм реакции присоединения брома к ацетилену: 1. Образование π-комплекса:
2. Скоростьлимитирующая стадия образования циклического бромирениевого катиона:
3. Присоединение бромид-иона к циклическому бромирениевому катиону:
Гидрогалогенирование Алкины реагируют с хлористым водородом и бромистым водородом подобно алкенам. Галогенводороды присоединяются к ацетиленовым углеводородам в две стадии по правилу Марковникова:
В таких реакциях скорость 100-1000 раз ниже, чем в реакциях с участием алкенов. Соответственно процесс может быть остановлен на стадии монобромида. Введение атома галоида снижает реакционную способность двойной связи. Механизм реакции гидрогалогенирования можно представить схемой: 1. На первой стадии образуется π-комплекс:
2. Образование промежуточного карбкатиона. Эта стадия является медленной (скоростьлимитирующей):
На этой стадии один из атомов углерода двойной связи переходит в состояние sp2-гибридизации. Другой остается в состоянии sp-гибридизации и приобретает вакантную р-орбиталь. 3. На третьей стадии бромид-ион, образовавшийся на второй стадии, быстро присоединяется к карбкатиону:
Взаимодействие образовавшегося бромалкена со второй молекулой бромистого водорода идет по обычному для алкенов механизму. В присутствии пероксидов наблюдается перекисный эффект Караша. Реакция идет по радикальному механизму. Вследствие чего бромоводород присоединяется к алкину против правила Марковникова:

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|