
|
|
Порядок выполнения работы1. Взвесить внутренний калориметр и определить его массу mк (масса мешалки mм написана на ней самой). 2. Наполнить внутренний калориметр примерно на 2/3 водой, температура которой примерно на 10°С выше комнатной. Взвесить сосуд еще раз, определив, тем самым, массу воды m2. 3. Собрать калориметрическую установку, вставив внутренний калориметр во внешний и поместив термометр в воду для измерения температуры во время опыта. Перемешать воду в калориметре. 4. Подготовить кусок льда, масса которого m1 примерно равна 1/3 массы воды, и t = 0°C. 5. Включить секундомер, зафиксировав температуру в начальный момент времени. Тщательно перемешивая воду, записывать в таблицу показания термометра через 1–2 минуты до тех пор, пока температура воды в калориметре за счет теплообмена с внешней средой понизится примерно на 0,8 – 1,5°С (4–10 значений). Это начальная стадия опыта. 6. зафиксировав температуру t0, опустить в калориметр, заранее приготовленный и высушенный фильтровальной бумагой, кусок льда. 7. Продолжая перемешивать воду в калориметре, измерять температуру в нем как можно чаще (через 15–20 секунд) до тех пор, пока не кончится процесс плавления льда, что соответствует минимальной температуреt1 в калориметре. Это главная стадия опыта. 8. В заключительной стадии опыта необходимо, продолжая перемешивать воду, отмечать через 1–2 минуты повышение температуры воды в калориметре в результате теплообмена с внешней средой до тех пор, пока она не повысится на 1–2°С выше температуры t1. 9. Взвесить внутренний калориметр в третий раз, чтобы определить массу льда m1. Обработка результатов измерений 1. Построить на миллиметровой бумаге график зависимости температуры системы от времени по полученным экспериментальным данным. 2. Определить по графику исправленные значения температур t0' и t1', проведя вертикальный отрезок СD (см. рис 12.2) так, чтобы площади BOC и DOE были равны. 3. Рассчитать значение величины λ по формуле (12.7) и величину изменения энтропии льда при плавлении (S2–S1) по формуле (12.6). 4. Вычислить погрешности полученных значений ∆λ и ∆(S2 – S1).
Формулы для расчета погрешности результата эксперимента
Погрешность величиныλ можно вычислить по следующей формуле
Эта формула получена на основании общей формулы вычисления погрешности функции многих переменных. При этом были отброшены слагаемые, которые в условиях данного опыта на порядок меньше остальных. Кроме того, погрешности измерения температур считаются равными: ∆t1= ∆t0= ∆t и определяются точностью термометра. Погрешности измерения масс также принимаются равными: ∆m1= ∆m2= ∆m3= ∆m0. Но так как все используемые в уравнении массы m1, m2, m3 определяются из двух взвешиваний, то Примечание. Рекомендуется подумать: каким образом можно упростить формулу (12.10). Погрешность изменения энтропии определяется по формуле
где λ и ∆λ – найденные значения удельной теплоты плавления льда и её погрешность. Содержание отчета
Контрольные вопросы s Что такое агрегатное и фазовое состояние вещества? Чем характеризуется каждое из них? s Что такое фазовые переходы? Какие фазовые переходы существуют и чем они отличаются? s Что такое удельная теплота фазового перехода? s Каким образом учитывается в данной работе теплообмен калориметра с окружающей средой?
Лабораторная работа 13
Изучение зависимости температуры кипения воды от давления Прежде чем приступить к работе, необходимо ознакомится с введением по теме «Агрегатные и фазовые состояния вещества». Цель работы: изучить зависимость температуры кипения воды T от давления p внутри сосуда и на основании этих данных определить удельную теплоту испарения воды λ. Физическое обоснование эксперимента. Уравнение Клапейрона–Клаузиуса для случая испарения имеет вид:
где Vп и Vж – объем пара и жидкости для некоторой массы m, λ – удельная теплота испарения, р – давление, T – температура кипения. Из уравнения (13.1), следует, что понижение давления ведет к понижению температуры кипения, так как всегда Vп – Vж > 0. Сделаем упрощающие приближения: 1. Считаем, что величина λ не зависит от температуры в исследуемом интервале температур. Строго говоря, это не так. Делая такое допущение, мы определяем среднее значение λ для данного интервала температур. 2. Пренебрежем объемом Vж по сравнению с Vп. Это приближение вполне допустимо, так как для воды при 100°С и 760 ммрт.ст. Vп = 1650 Vж, что, как можно потом проверить, значительно меньше погрешности результата. 3. Объем водяного пара будем определять из уравнения Менделеева–Клапейрона Учтя сделанные допущения в уравнении (13.1) и подставив в него значение Vп, получим
Интегрируя его
получим
где
Уравнение (13.3) – это уравнение прямой y = ax+b, где y = lnp, x = 1/T и a = μλ/R – есть тангенс угла наклона этой прямой. Определив значение a (методом наименьших квадратов и из графика lnp = f(1/T)), можно вычислить значение λ:
Потенцируя это уравнение, получаем выражение, связывающее давление р насыщенных паров жидкости с её температурой Т:
Описание экспериментальной установки. Экспериментальная установка изображена на рис. 13.1. Электронагреватель и насос обеспечивают само явление – кипение воды в колбе А при определенных давлении Воздух из системы откачивается форвакуумным насосом с электромотором. Поскольку насос предназначен для откачки воздуха, а не водяного пара и тем более не воды, колба подключена к нему через холодильник, в котором водяной пар, образующийся при нагревании и кипении воды, охлаждается, конденсируется и стекает обратно в колбу. Холодильник Д представляет собой трубку, окруженную водяной рубашкой для охлаждения паров воды. Как и в любой подобный холодильник, холодная вода из водопроводного крана подается снизу (через отверстие а), а нагревшаяся отводится сверху (через отверстие б). Для поглощения оставшихся паров воды служит сосуд В с концентрированной серной кислотой.
Температура кипения воды измеряется с помощью термометра Т, опущенного в колбу так, чтобы шарик ртути находился непосредственно над поверхностью воды. По ртутному манометру М с точностью до 1 мм определяется разность Атмосферное давление Трехходовой кран Кпозволяет соединять систему колба, холодильник, сосуд В и манометр либо с атмосферой (I положение крана К), либо с насосом (II положение крана К), либо изолировать систему и от атмосферы, и от насоса (III положение крана К). Отверстие в пробке крана всегда находится со стороны ручки. Понижение давления в системе, т.е. откачка воздуха из системы осуществляется с помощью форвакуумного насоса с мотором. Система должна быть хорошо изолирована от внешней среды для того, чтобы в процессе эксперимента давление внутри системы оставалось контролируемым. Порядок выполнения работы 1. Произвести подготовку установки для измерений: соединить систему с атмосферой, для чего поставить кран К в положение I. Вращая пробку крана одной рукой, другой рукой обязательно придерживать сам кран, во избежание его поломки. 2. Открыть кран водопровода и установить медленное протекание воды через холодильник. 3. Включить электроплитку и начать нагревание. Примечание: если в нижней части трубки холодильника образуется "пробка" из сконденсированной воды, то нагревание прекратить до тех пор, пока эта вода не стечет обратно в колбу. 4. Убедиться, что уровни ртути в обоих коленах манометра совпадают, измерить по барометру и записать атмосферное давление p0. 5. Нагреть воду до кипения при атмосферном давлении и приступить к измерениям, предварительно заготовив таблицу.
6. Выключить плитку и записать температуру кипения воды при атмосферном давлении. 7. Как только кипение воды прекратится, поставить кран К в положение II, т.е. соединить колбу с насосом и начать откачивать воздух из колбы до повторного закипания воды в колбе. Затем перекрыть кран К, поставив его в положение III, и произвести отсчеты hлев, hпр и температуру окончания кипения tºC. 8. Многократно повторять операции пункта 7, при понижении температуры воды в колбе до 70ºС. (Следить, чтобы интервалы между температурами кипения не превышали 2–3ºС) 9. Закончив измерения, кран К медленно соединить с атмосферой и закрыть кран водопровода. Работу можно делать и в обратном порядке. При этом экономится время, так как не нужно ждать, пока вода закипит при атмосферном давлении. В этом случае порядок работы следующий. 1. Включив плитку и нагрев воду в колбе примерно до 75ºС, начать откачивать воздух из системы до закипания воды в колбе. 2. Поставить кран К в положение III и произвести отсчет tºC, hлев, hпр. Затем, не выключая плитку, медленно соединить кран К с атмосферой и повышать температуру воды в колбе примерно на 2°С. 3. Поставить кран К в положение II, откачать систему до закипания воды в колбе, повернуть кран К в положение III и произвести отсчеты tºC, hлев, hпр. Все эти операции повторять до тех пор, пока вода не закипит при атмосферном давлении.
Обработка результатов измерений 1. Построить графики Т = f(p) и lnp = f(1/T) 2. Определить тангенс угла наклона a и его погрешность Δa из графика линейной зависимости lnp = f(1/T), и рассчитав его по методу наименьших квадратов. Искомая величина удельной теплоты испарения выражается через величину a формулой λ = aR/μ, следовательно, погрешность Δλ можно выразить через погрешность величины a: Δλ = Δa(R/μ). Погрешностью величин R иμ пренебрегаем, так как табличные значения постоянных можно взять с достаточной точностью. Содержание отчета 1. Таблица измерений: p0, hлев, hпр, p, T. 2. График зависимости Т = f(p). 3. График зависимости lnp = f(1/T). 4. Величина a – тангенс угла наклона этого графика, определенная из графика и расcчитанная по методу наименьших квадратов. 5. Вычисленное значение λ и погрешность Δλ. 6. Окончательный результат в системе СИ. Контрольные вопросы s Что такое фазовый переход? s Какие существуют фазовые переходы, и чем они отличаются? s Что такое удельная теплота испарения? s Какой метод определения удельной теплоты испарения использован в данной работе? s Как и почему температура кипения жидкости зависит от давления? 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|


 , где ∆m – погрешность при непосредственном взвешивании, определяемая точностью весов и разновесов. Погрешностью величин c1 и с2 пренебрегаем.
, где ∆m – погрешность при непосредственном взвешивании, определяемая точностью весов и разновесов. Погрешностью величин c1 и с2 пренебрегаем.
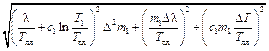 ,
,
 ,
,
 , где R – универсальная газовая постоянная, μ – молекулярная масса воды (R ≈ 8,31·103 Дж·кмоль–1·К–1, μ ≈ 18 кг/кмоль).
, где R – универсальная газовая постоянная, μ – молекулярная масса воды (R ≈ 8,31·103 Дж·кмоль–1·К–1, μ ≈ 18 кг/кмоль). , а после разделения переменных получаем дифференциальное уравнение:
, а после разделения переменных получаем дифференциальное уравнение:  .
. ,
,
 ,
,
 и
и  – это атмосферное давление и температура кипения при атмосферном давлении. Учитывая, что вторые слагаемые в обеих частях этого уравнения постоянные величины, его можно переписать:
– это атмосферное давление и температура кипения при атмосферном давлении. Учитывая, что вторые слагаемые в обеих частях этого уравнения постоянные величины, его можно переписать: .
.


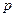 и температуре
и температуре 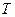 . Электронагреватель включается в сеть с напряжением 220 В.
. Электронагреватель включается в сеть с напряжением 220 В.
 между атмосферным давлением
между атмосферным давлением  и
и  – расстояния в миллиметрах в левом и в правом коленах манометра от нулевой отметки шкалы до верхней точки мениска, то
– расстояния в миллиметрах в левом и в правом коленах манометра от нулевой отметки шкалы до верхней точки мениска, то  и
и 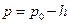 (hлев и hпрмогут быть не равны из-за непостоянства диаметра трубки манометра по её длине)
(hлев и hпрмогут быть не равны из-за непостоянства диаметра трубки манометра по её длине)