|
|
Стимуляция в режиме двойной вспышки(СРДВ):серия из трех коротких (0,2 mc) импульсов с интервалом 20 mc (частота 50 Гц), затем пауза длиной 750 mc, после чего повторяется два (СРДВ3,2) или три (СРДВ3,3) импульса, аналогичных начальным (рис. 6-35). Затухание,т. е. постепенное снижение вызванного мышечного ответа при длительной или повторяющейся стимуляции нерва, характерно для действия недеполяризующих миорелаксантов (табл. 9-2). Затухание объясняется тем, что недеполяризующие миорелаксанты уменьшают количество доступного ацетилхолина, способного высвободиться при стимуляции нерва (блокада мобилизации ацетилхолина). Полноценное восстановление нервно-мышечной проводимости четко коррелирует с отсутствием затухания. Так как затухание лучше выявляется при тетанической стимуляции и при стимуляции в режиме двойной вспышки, чем при TOF-режиме и повторных одиночных стимулах, то именно первые два режима предпочтительно использовать для оценки полноценности восстановления нервно-мышечной проводимости в конце анестезии. Способность тетанической стимуляции усиливать ответ на одиночный импульс получила название посттетанического облегчения. Посттетани-ческое облегчение может быть обусловлено компенсаторным увеличением мобилизации ацетилхолина после тетанической стимуляции. В отличие от недеполяризующего блока для I фазы деполяризующего блока нехарактерно затухание при тетанической стимуляции и в TOF-режиме, не возникает и посттетанического облегчения. Однако, если доза деполяризующего миорелаксанта чрезмерно высока, качество блока изменяется — он начинает напоминать недеполяризующий. Этот феномен получил название II фазы деполяризующего блока и может быть объяснен ионными и конформационными изменениями, возникающими при длительной деполяризации мышечной клетки. ТАБЛИЦА 9-2. Вызванные мышечные ответы при электрической стимуляции периферического нерва: характеристика деполяризующего (I и Il фаза) и недеполяризующего блоков
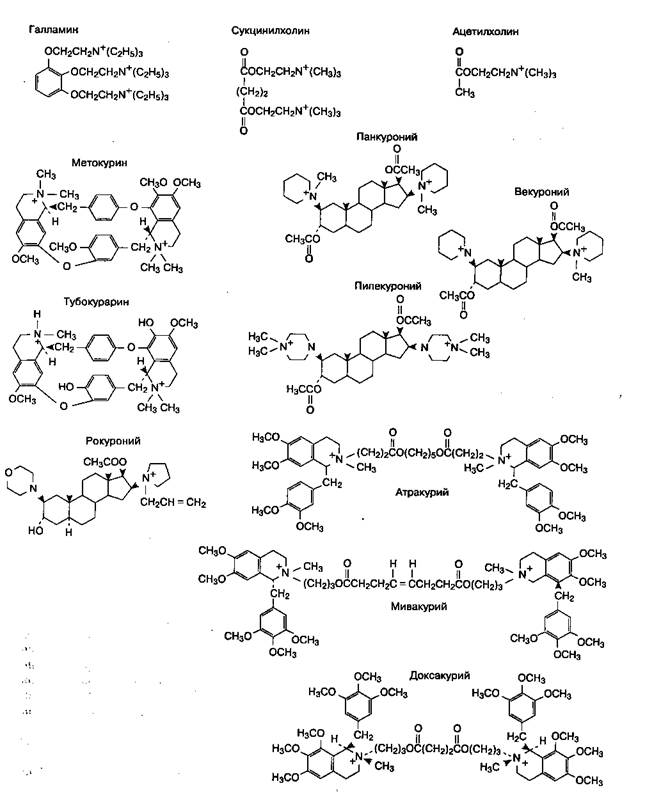
Восстановление нервно-мышечной проводимости Деполяризующие миорелаксанты не взаимодействуют с ацетилхолинэстеразой. Из области нервно-мышечного синапса они поступают в кровоток, после чего подвергаются гидролизу в плазме и печени под действием другого фермента — псевдохолин-эстеразы (синонимы — неспецифическая холинэс-тераза, холинэстераза плазмы). Этот процесс протекает очень быстро, что имеет благоприятный характер: специфические антидоты деполяризующего блока отсутствуют. За исключением мивакуриума недеполяризующие миорелаксанты не гидролизуются ни ацетилхолинэстеразой, ни псевдохолинэстеразой. При недеполяризующем блоке восстановление нервно-мышечной проводимости обусловлено перераспределением, частичной метаболической деградацией и экскрецией недеполяризующих миорелаксантов или же может быть вызвано воздействием специфических антидотов — ингибиторов ацетилхолинэстеразы (гл. 10). Так как в нервно-мышечных синапсах ингибиторы ацетилхолинэстеразы увеличивают количество доступного аце-тилхолина, конкурирующего с деполяризующими релаксантами, то они не способны устранять деполяризующий блок. В действительности, повышая концентрацию доступного ацетилхолина в нервно-мышечном синапсе и снижая активность псевдохолинэстеразы плазмы, ингибиторы ацетилхолинэстеразы увеличивают продолжительность деполяризующего блока. Деполяризующие миорелаксанты Сукцинилхолин (Дитилин) Сукцинилхолин — единственный недеполяризующий миорелаксант, применяемый в клинике в настоящее время. Структура Миорелаксанты подавляют нервно-мышечную проводимость благодаря сходству с ацетилхоли-ном. Так, все миорелаксанты являются четвертичными аммониевыми соединениями. Сукцинилхолин (синонимы — суксаметониум и диацетилхолин) состоит из двух соединенных между собой молекул ацетилхолина (рис. 9-3). Структурное сходство с ацетилхолином объясняет механизм действия, побочные эффекты и метаболизм сукцинилхолина. Из-за структурного сходства аллергия к одному миорелаксанту свидетельствует о высоком риске перекрестной аллергии к другим миорелаксантам. Метаболизм и экскреция Непреходящая популярность сукцинилхолина обусловлена быстрым началом действия (30-60 с) и кратковременностью эффекта (как правило, < 10 мин). Быстрое начало действия обусловлено низкой жирорастворимостью (все миорелаксанты представляют собой высокоионизированные и водорастворимые соединения) и относительной передозировкой при применении (обычно перед интубацией вводят препарат в избыточно высоких дозах). После поступления в кровоток подавляющая часть сукцинилхолина под воздействием псевдохолинэстеразы быстро гидролизуется до сукци-нилмонохолина. Эта реакция настолько эффективна, что только часть сукцинилхолина достигает нервно-мышечного синапса. После того как концентрация препарата в сыворотке крови снижается, молекулы сукцинилхолина начинают диффундировать из комплекса с холинорецепторами в кровоток и нервно-мышечная проводимость восстанавливается. Действие препарата удлиняется при увеличении дозы и нарушении метаболизма. Метаболизм сукцинилхолина нарушается при гипотермии, а также при низкой концентрации или наследственном дефекте псевдохолинэстеразы. Гипотермия замедляет гидролиз. Концентрация псевдохолинэстеразы в сыворотке (ее измеряют в ед/л) может снижаться при беременности, заболеваниях печени и под воздействием некоторых лекарственных средств (табл. 9-3). У 2 % больных одна аллель гена псевдохолинэстеразы нормальная, вторая — патологическая (гетерозиготный дефект гена псевдохолинэстеразы), что несколько удлиняет действие препарата (до 20-30 мин). У 1 больного из 3000 обе аллели гена псевдохолинэстеразы патологические (гомозигот-ный дефект гена псевдохолинэстеразы), в результате чего активность псевдохолинэстеразы снижается в 100 раз по сравнению с нормой. В отличие от сниженной концентрации и гетерозиготного дефекта псевдохолинэстеразы, когда продолжительность нервно-мышечного блока увеличивается лишь в 2-3 раза, при гомозиготном дефекте нервно-мышечный блок после инъекции сукцинилхолина длится очень долго (до 6-8 ч). Из патологических генов псевдохолинэстеразы наиболее распространен дибукаиновый вариант. Дибукаин — это местный анестетик, который ингибирует активность нормальной псевдохолинэстеразы на 80 %, активность псевдохолинэстеразы при гетерозиготном дефекте на 60 %, при гомозиготном дефекте — на 20 %. Процент угнетения активности псевдохолинэстеразы называют дибу-каиновым числом. Дибукаиновое число прямо пропорционально функциональной активности псевдохолинэстеразы и не зависит от ее концентрации. Следовательно, для определения активности псевдохолинэстеразы при лабораторном исследовании измеряют концентрацию фермента в ед/л (второстепенный фактор, определяющий активность) и определяют его качественную полноценность — дибукаиновое число (главный фактор, определяющий активность). При длительном параличе скелетных мышц, который возникает после введения сукцинилхолина больным с патологической псевдохолинэстеразой (синоним — атипичная псевдохолинэстераза), следует осуществлять ИВЛ до тех пор, пока нервно-мышечная проводимость не восстановится. В некоторых странах (но не в США) применяют термически обработанные препараты холинэстеразы человеческой плазмы. Хотя можно использовать свежезамороженную плазму, риск инфекции обычно превышает пользу от трансфузии.
Рис. 9-3.Химическая структура миорелаксантов 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|