|
Нефть. Состав, свойства нефти. Продукты перегонки нефти, их применение. Детонационная стойкость бензина.

Нефть - маслянистая жидкость темно-бурого или почти черного цвета с характерным запахом. Она легче воды (густ. 0,73-0,97 г/см3), в воде практически не растворима. По составу нефть - сложная смесь углеводородов различной молекулярной массы. Главным образом жидких (в них растворены твердые и газообразные углеводороды). Обычно это углеводороды парафиновые, циклоалканы, ароматические, соотношение которых в нефти разных месторождений колеблется в широких пределах. Бакинская и эмбинская нефти содержат больше циклоалканов (с пяти - и шестичленными кольцами), грозненская и западно-украинская - парафиновых, уральская-ароматических. Кроме углеводородов нефть содержит кислородные, сернистые и азотистые органические соединения. Сырую нефть обычно не используют. Чтобы добыть технически ценные продукты нефти, ее подвергают переработке. Первичная переработка нефти заключается в ее перегонке. Перегонку проводят на нефтеперерабатывающих заводах после отделения газов. При перегонке нефти получают светлые нефтепродукты: бензин (т. кип. от' 40 до 150-200 °С), лигроин (т. кип. 120-240 °С), керосин (т. кип. 150-300 °С), газойль - солярное масло (т. кип. выше 300 °С), а в остатке - вязкую черную жидкость - мазут. Мазут подвергают дальнейшей переработке. Его перегоняют под пониженным давлением (чтобы предотвратить разложение) и выделяют масла: веретенное, машинное, цилиндрический и т.д. С мазута некоторых сортов нефти добывают вазелин и парафин. Остаток мазута после отгонки называется нефтяным пеком, или гудроном.
| Фракция
| Размеры молекул
| Температура кипения, °С
| Применение
| | Бензин
| С5 – С11
| от 40 до 200
| Моторное, авиационное и автомобильное топливо; растворитель масел
| | Лигроин
| С8 – С14
| от 120 до 240
| топливо для тракторов, растворитель в лакокрасочной промышленности
| | Газ
| С12 – С18
| от 180 до 300
| Топливо для реактивных и тракторных двигателей
| | Газойль
| С18 – С25
| от 270 до 350
| Топливо для дизелей
| | Мазут
| от С20 и выше
| От 300 и выше
| Мастика, парафин, вазелин
|
Солярное масло используется как моторное топливо, а масла - для смазывания механизмов.
Вазелин используют в медицине. Он состоит из смеси жидких и твердых углеводородов.
Парафин применяется для получения высших карбоновых кислот, пропитки древесины в производстве спичек и карандашей, для изготовления свечей, гуталина и т.д. Он состоит из смеси твердых углеводородов.
Гудрон – нелетучая темная масса; после частичного окисления применяется для изготовления асфальта.
Мазут кроме переработки на смазочные масла и бензин используют как жидкое котельное топливо.
При вторичных методах переработки нефти происходят изменения в структуре углеводородов, входящих в ее состав. Среди этих методов большое значение имеет крекинг (расщепление) углеводородов нефти, который осуществляют для повышения выхода бензина.
Термический крекинг проводят при нагревании исходного сырья (мазута и др.) до температуры 450 - 550°С при давлении 2-7МПа. При этом молекулы углеводородов с большим числом атомов углерода расщепляются на
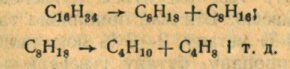
более мелкие молекулы насыщенных и ненасыщенных углеводородов.
Каталитический крекинг проводят при наличии катализаторов (преимущественно алюмосиликатов) при 450 °С га атмосферном давлении. Этим способом добывают авиационный бензин с выходом до 80 %. Такому виду крекинга подвергаются преимущественно керосиновая и газойлевая фракции нефти. Пол время каталитического крекинга вместе с реакциями расщепления происходят реакции изомеризации. В результате последних образуются насыщенные углеводороды с разветвленным углеродным скелетом молекул, что улучшает качество бензина.
Важным каталитическим процессом есть ароматизация углеводородов, то есть превращение парафинов и циклопарафинов на ароматические углеводороды. В результате нагрев тяжелых фракций нефтепродуктов при наличии катализатора! (платины или молибдена) углеводороды, содержащие 6-8 атомов углерода в молекуле, превращаются в ароматические углеводороды. Эти процессы происходят вовремя риформинга (облагородь жевания бензинов).
При крекинг-процессах образуется большое количество газов (газы крекинга), которые содержат в основном насыщенные и ненасыщенные углеводороды. Эти газы используют как сырье для химической промышленности.
В последнее время (наряду с увеличением выработки топлива и масел) углеводороды нефти широко используются как источник химического сырья. Различными способами из них получают вещества, необходимые для производства пластмасс, синтетического текстильного волокна, синтетического каучука, спиртов, кислот, синтетических моющих средств, взрывчатых веществ, ядохимикатов, синтетических жиров и т.д.. Основную часть бензина получают прямой перегонкой и каталитическим крекингом. Свойства автомобильных бензинов характеризуются теплотой сгорания, детонационной стойкостью, фракционным составом, химической стабильностью, содержанием серы и других вредных примесей. Способность топлива противостоять детонационному сгоранию называется детонационной устойчивостью и характеризуется октановым числом. Чем выше октановое число, тем больше может быть сжатая в цилиндре горючая смесь. Как эталонное топливо принята смесь двух углеводородов: изооктана (С8Н12), обладает высокими антидетонационными свойствами, и нормального гептана (С7НІ6), что легко детонирует. Октановым числом называется условная единица, численно равная проценту (по объему) озооктана в смеси, состоящей из изооктана и нормального гептана и равноценна по своим антидетонационными свойствами данном топливу. Октановое число изооктана принимается за 100, а нормального гептана-за 0. Так, если бензин детонирует при работе смеси, состоящей из 76% изооктана и 24 % нормального гептана, то октановое число такого бензина равно 76.
Бензин - (рус. бензин; англ. petrol;) - естественная или искусственно полученная смесь
 углеводородов различного строения, температура кипения которых от 40 °C до 205 °C. Бензин - горючая, подвижная, в основном бесцветная жидкость с характерным запахом; удельный вес 0,700-0,780; легко испаряется, образует с воздухом в определенных концентрациях взрывоопасные смеси, температура вспышки преимущественно ниже 0°. Большинство бензинов замерзает ниже -60 °C. Около 90 % добывают из нефти. углеводородов различного строения, температура кипения которых от 40 °C до 205 °C. Бензин - горючая, подвижная, в основном бесцветная жидкость с характерным запахом; удельный вес 0,700-0,780; легко испаряется, образует с воздухом в определенных концентрациях взрывоопасные смеси, температура вспышки преимущественно ниже 0°. Большинство бензинов замерзает ниже -60 °C. Около 90 % добывают из нефти.
3. Каменный уголь, продукты его переработки.
Уголь - это соединение от бурого до черного цвета, плотность 0,92-1,7 г/см3, тускло-блестящая, матовая вещество, характеризуется различными оттенками цвета и блеска, разной структурой.
В состав угля входят органические вещества, минеральные примеси и влага. Содержание органических веществ составляет 50-97 % от общей массы сухого угля. Химический состав органической части угля включает C, H, O, S, N и др. химические элементы периодической системы Д.И. Менделеева. Массовая доля углерода составляет 60-98 % всей массы угольной веществ. В незначительных количествах содержатся сульфиды цветных металлов, фосфаты, сульфаты, соли щелочных металлов. Относительное содержание минеральных примесей в сухом веществе угля колеблется в широких пределах (зольность 50-60 %). Влажность - один из основных параметров классификации бурого угля.
Уголь образуется в условиях, когда гниющий растительный материал накапливается быстрее, чем происходит его бактериальное разложение. Идеальные условия для этого есть в болотах, где стоячая вода обеднена кислородом, препятствует жизнедеятельности бактерий и тем самым предохраняет растительную массу от полного разрушения. На определенной стадии процесса, кислоты, которые выделяются в его ходе, предотвращают дальнейшей деятельности бактерий. Так возникает торф - исходный продукт для образования угля. Если затем происходит его захоронение под другими наносами, то торф под действием сжатия теряя воду и газы, преобразуется в уголь.
Торф → бурый уголь → каменный уголь → антрацит
Различают следующие виды угля:
- уголь каменный;
- уголь бурый;
- антрациты.
Антрацит - это ископаемый уголь, характеризуется большой плотностью и блеском. Содержание углерода в антраците составляет примерно 95 %. Применяется как твердое высококалорийное топливо. Имеет наибольшую теплоту сгорания, но плохо загорается. Образуется из каменного угля при повышении давления и температуры на глубинах порядка 6 километров.
Каменный уголь - осадочная порода, является продуктом глубокого разложения остатков растений (древесно-кустарниковых папоротников, хвощей). Большинство залежей каменного угля было образовано в палеозое, главным образом в каменноугольный период, примерно 300-350 миллионов лет назад. Каменный уголь - смесь высокомолекулярных полициклических ароматических соединений с высокой массовой долей углерода (75 % до 95 %), влаги (12 %) и летучих веществ с небольшим количеством минеральных примесей (32 %). Образуется из бурого угля на глубинах порядка 3 километров.
Бурый уголь - твердое ископаемое уголь, образовавшийся из торфа, содержит 65-70 % углерода бурого цвета, низкую теплоту сгорания (т.е. много воды 43 %), количество летучих веществ (до 50 %).
Используется как местное топливо, а также как химическое сырье. Образуется из отмерших органических остатков под давлением нагрузки и действием повышенной температуры на глубинах порядка 1 км.
| Название угля
| Обозна
чение марки
| Классификационные показатели
| | Содержание С, %
| Теплотворная способность, кДж/кг
| | Бурый
| Б
| 65-80
| 8500 - 30000
| | Каменный
| К
| 80-93
| 30000-35000
| | Антрацит
| А
| 93-98
| 35000-38000
|
Уголь широко используют как твердое высококалорийное топливо, оно служит также исходным сырьем для получения различных химических продуктов.
Основной метод переработки каменного угля - коксование (сухая перегонка). При коксовании (нагревании до 1000-1200 °С без доступа воздуха) получают различные продукты: кокс, каменноугольную смолу, аммиака воду и коксовый газ. Примерный состав коксового газа, %: водорода - 60, метана - 25, оксида углерода (II) - 5, азота - 4, оксида азота (IV) - 2, этилена - 2 и других газов - 2.
Сухая перегонка угля заключается в его химическом раскладе при нагревании без доступа воздуха. Различают два варианта сухой перегонки угля – полукоксования и коксования, первый процесс осуществляется при 500-550 0С, второй – при 900-1050 0С.
Главная задача полукоксования каменного угля - получение жидких углеводородов (бензина); попутно образуются полукокс и смесь газов (СО, СО2, Н2, СН4, N2 и др.). Полукокс нельзя применять в металлургии, его применяют в производстве кальций карбида и для газификации угля. Температура, при которой проводится полукоксование, не должна превышать 550 0С, так как при более высокой температуре выход жидких углеводородов уменьшается. Из 1 т каменного угля получают 110 м3 газа, 750-800 кг полукокс, 8 кг смолы и дегтя. Процесс коксования осуществляется на коксохимических заводах. Основные продукты коксования каменного угля: 
- коксовый газ, из которого путем контакта с каменноугольной смолой получают технический бензол - жидкую смесь легко кипящих аренов;
- каменноугольная смола, ее разделяют перегонкой на арены, фенолы, которые являются ценным сырьем для производства красителей, растворителей, взрывчатых веществ, лекарственных препаратов, пестицидов;
- надсмольная вода, из нее путем обработки известковым молоком (кальций гидроксид) изымают аммиак;
- кокс, используют в металлургии.
Полукоксование бурого угля проводят с целью получения дегтя.
Основные продукты полукоксование бурого угля:
• полукоксовый газ используется для нагрева печей в процессе полу коксования;
•буроугольный деготь используется в производстве алканов;
• легкое масло, которое содержит бензин низкого качества, используется как
растворитель масел или как моторное масло;
• среднее масло, которое содержит фенол, пригодное как дизельное топливо;
тяжелое масло - из него выделяют смесь высших гомологов ряда алканов;
подсмольная вода - из нее выделяют фенолы, кетоны и аммиак.
Газификация - это превращение органической части ископаемого угля в горючие газы при высокотемпературной (1000-2000 0С) взаимодействия его с окислителями (О2, воздух, водяной пар, СО2). Для газификации используют бурый уголь и продукт переработки каменного угля - кокс. Газификацию проводят в газогенераторах.
Основные виды топлива.
Проблема обеспечения украинской экономики энергоносителями - одна из самых болезненных. Газ, нефть, уголь и даже электроэнергию приходится импортировать. Ежегодно на это тратится около 8 млрд. долл. На что идет 2/3 всего товарного экспорта. Дефицит энергоносителей влечет за собой шлейф тяжких последствий: недобор урожая, систематическое отключение населенных пунктов от электроснабжения и т. д. Поэтому проблема требует кардинального решения.
На современном этапе экономического развития важнейшее - топливно - энергетическая проблема. Успешное ее решение определяет возможности, темпы и направление экономического и социального развития. Значение топлива для экономики любой страны большое: без него невозможен производственный процесс, работа промышленности, сельского хозяйства и транспорта. Основными первичными источниками энергии на современном этапе является нефть, уголь, природный газ, гидроэнергия, а также быстро растет значение атомной энергии. Доля остальных источников (дрова, торф, энергия солнца, ветра, геотермальная энергия) в общем энергопотреблении составляет лишь несколько процентов.
Среди добываемых органических топливных ресурсов на уголь приходится (в зависимости от оценки) 65-90%. Исторически оно сыграло большую роль в мировом промышленном развитии. Уголь обеспечил энергетическую основу первой промышленной революции.
Угольная промышленность по объему добычи топлива в натуральном выражении занимает первое место среди других отраслей. Здесь сосредоточено большинство работников и основных фондов топливной промышленности.
Уголь оценивают по нескольким параметрам:
1. По глубине залегания. Уголь добывают открытым или закрытым
(шахтного) способами, - от этого зависит его себестоимость.
2. По марочному составу и качеству.
Основным районом добычи каменного угля является Донецкий бассейн.
Здесь есть все марки угля: коксующийся (половина запасов), антрацит, газовый. Донецкий уголь имеет высокую теплотворную способность и незначительную зольность. Зато себестоимость его сравнительно большая из-за большой глубины залегания пластов. Это снижает его конкурентоспособность. Основными звеньями угледобычи шахтным способом являются: шахта с комплексом наземных и подземных сооружений и энергосиловых хозяйств, углеобогатительная фабрика, транспортные коммуникации и водохозяйственные сооружения, районные энергетические центры, складские хозяйства, предприятия и организации непроизводственной сферы. Из угольной промышленности прямо или непосредственно связана деятельность почти 40% городского населения Донецкой и Луганской областей. Угольные шахты сосредоточены преимущественно в центральной и северной частях Донецкой и южной части Луганской области.
Коксовый уголь добывают главным образом в центральной части Донецкой области в районе Енакиево, Макеевки, Горловки, Донецка, Красноармейска, Константиновки и других городов, а также в Краснодарском и Кудеевском районах Луганской области. В Антрацитовском, Лутугинском и Алчевском районах Луганской области добывают больше энергетического угля.
Использование газа в 2 раза дешевле по сравнению с нефтью. Кроме того, она обеспечивает производство азотных удобрений и синтетических материалов. Промышленность природного газа включает в себя разведку, добычу, транспортировку, хранение и переработку природного газа сопутствующего нефтяного газа, который добывается вместе с нефтью. Эта отрасль энергетики развивается быстрее всего, потому что ее роль в энергоснабжении постоянно растет. Природный газ применяется во многих отраслях, но большая его часть используется в энергетике, потому что это топливо меньше загрязняет атмосферу. Газовая промышленность как отрасль сформировалась в послевоенные годы на базе разведанных в стране месторождений природного газа. Очень интенсивное развитие газовая промышленность приобрела в первой половине 70-х годов.
Контроль знаний:
1. Напишите про перегонку нефти.
2. Перелечите соединения, которые можно получить из нефти.
3. Что такое крекинг? Какие виды крекинга вас известны?
4. Склад имеет нефть?
5. Перелечите основные природные источники уллеводородов.
6. Что означает детонационная стойкость бензина?
7. Какой состав имеет природный газ?
8. Оцените влияние продуктов переработки углеводородного сырья на окружающую среду.
Литература:
1.Габриелян О.С. Химия. 11 класс. Базовый уровень: учеб. для общеобразоват. учреждений. – М., 2010,
2. Габриелян О.С. Химия: учеб. для студ. сред. проф. учеб. заведений.- 2-е издание / О.С. Габриелян, И.Г. Остроумов. – М., 2013.
3. http://ru.wikipedia.org- энциклопедия
4. .Рудзитис Г.Е., Фельдман Ф.Г, химия. 10 класс: учебник для общеобразовательных учреждений (базовый уровень). – М.: Просвещение, 2016.

Самостоятельная работа № 7
Тема: Фенолы, их свойства.Характерные реакции. Поликонденсация фенола с формальдегидом. Применение фенола на основе свойств.
Основные понятия и термины по теме:фенол, формальдегид, поликонденсация фенола.
План изучения темы
(перечень вопросов, обязательных к изучению):
Применение.
1.Фенолы, их свойства на примере фенола.
2.Характерные реакции. Химические свойства.
3. Поликонденсация фенола с формальдегидом.
4. Получение и применение фенола на основе их свойств.
Содержание:
1.Фенолы, их свойства на примере фенола.
Фенолы. R–OH или R(OH)n.
Фенолы — органические соединения ароматического ряда, в молекулах которых гидроксильные группы связаны с атомами углерода ароматического кольца. По числу ОН-групп различают:
- одноатомные фенолы (аренолы): фенол (C6H5OH) и его гомологи;
- двухатомные фенолы (арендиолы): гидрохинон, пирокатехин, резорцин;
- трёхатомные фенолы (арентриолы): пирогаллол, флороглюцин, гидроксигидрохинон и т. д. Важнейшим представителем фенолов является фенол (гидроксобензол, старые названия - гидроксибензол, оксибензол) C6H5—OH.
Физические свойства фенола: твердое бесцветное вещество с резким запахом; ядовит; при комнатной температуре заметно растворим в воде, водный раствор фенола называют карболовой кислотой. 2.Характерные реакции. Химические свойства:
Химические свойства фенола обусловлены сочетанием двух фрагментов в составе его молекулы: ароматического углеводородного радикала фенила и гидроксильной группы. Свойства фенола являются яркой иллюстрацией положения теории строения органических соединений о взаимном влиянии атомов в молекулах.
Влияние фенила на гидроксил заключается в том, что он еще более поляризует ковалентную связь между атомами кислорода и водорода в гидроксиле. Атом водорода при этом становится более подвижным по сравнению со спиртами, что обусловливает кислотные свойства фенола (отсюда и название — карболовая кислота):
1.Кислотные свойства.
-взаимодействуют с щелочными металлами.
2C6H5OH + 2Na 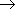
| 2C6H5ONa
| + H2
| | | фенолят натрия
| | - в отличие от спиртов, фенол вступает в реакцию нейтрализации со щелочами:
C6H5OH + NaOH 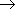 C6H5ONa + H2O C6H5ONa + H2O
Однако кислотные свойства фенола выражены слабее, чем у карбоновых кислот и, тем более, у сильных неорганических.
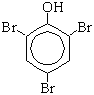
2.Замещение в бензольном кольце. Наличие гидроксильной группы в качестве заместителя в молекуле бензола приводит к перераспределению электронной плотности в сопряженной  -системе бензольного кольца, при этом увеличивается электронная плотность у 2-го, 4-го и 6-го атомов углерода (орто- и пара-положения) и уменьшается у 3-го и 5-го атомов углерода (мета-положение). -системе бензольного кольца, при этом увеличивается электронная плотность у 2-го, 4-го и 6-го атомов углерода (орто- и пара-положения) и уменьшается у 3-го и 5-го атомов углерода (мета-положение).
а) Реакция с бромной водой (качественная реакция):
Образуется 2,4,6-трибромфенол - осадок белого цвета.
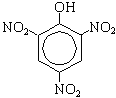
б) Нитрование (при комнатной температуре):
1. C6H5—OH + HNO3(разб.) 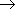 H2O + O2N—C6H4—OH (смесь орто- и пара-изомеров) H2O + O2N—C6H4—OH (смесь орто- и пара-изомеров)
По второй реакции образуется 2,4,6-тринитрофенол (пикриновая кислота).
Поликонденсация фенола с формальдегидом (по этой реакции происходит образование фенолформальдегидной смолы:
 Качественная реакция с хлоридом железа(III). Образуется комплексное соединение фиолетового цвета. Качественная реакция с хлоридом железа(III). Образуется комплексное соединение фиолетового цвета.
Реакция поликонденсации– это процесс образования полимера, который сопровождается выделением побочного низкомолекулярного продукта (чаще всего воды).
Не нашли, что искали? Воспользуйтесь поиском по сайту:
©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|



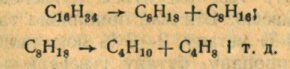
 углеводородов различного строения, температура кипения которых от 40 °C до 205 °C. Бензин - горючая, подвижная, в основном бесцветная жидкость с характерным запахом; удельный вес 0,700-0,780; легко испаряется, образует с воздухом в определенных концентрациях взрывоопасные смеси, температура вспышки преимущественно ниже 0°. Большинство бензинов замерзает ниже -60 °C. Около 90 % добывают из нефти.
углеводородов различного строения, температура кипения которых от 40 °C до 205 °C. Бензин - горючая, подвижная, в основном бесцветная жидкость с характерным запахом; удельный вес 0,700-0,780; легко испаряется, образует с воздухом в определенных концентрациях взрывоопасные смеси, температура вспышки преимущественно ниже 0°. Большинство бензинов замерзает ниже -60 °C. Около 90 % добывают из нефти.

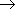
 -системе бензольного кольца, при этом увеличивается электронная плотность у 2-го, 4-го и 6-го атомов углерода (орто- и пара-положения) и уменьшается у 3-го и 5-го атомов углерода (мета-положение).
-системе бензольного кольца, при этом увеличивается электронная плотность у 2-го, 4-го и 6-го атомов углерода (орто- и пара-положения) и уменьшается у 3-го и 5-го атомов углерода (мета-положение).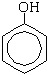
 Качественная реакция с хлоридом железа(III). Образуется комплексное соединение фиолетового цвета.
Качественная реакция с хлоридом железа(III). Образуется комплексное соединение фиолетового цвета.