|
|
Клинические синдромы при патологии тимусаДля выяснения роли тимуса большое значение имели данные, полученные в экспериментах на животных. Так, его удаление у новорожденных животных приводило к формированию синдрома "истощения", включающего отставание в росте, недоразвитие лимфоидной ткани, дистрофические изменения кожи и подкожной жировой клетчатки, снижение содержания гаммаглобулина в крови и, наконец, раннюю гибель животных.
· Врожденная аплазия тимуса у человека. Характеризуется лимфопенией, гипотрофией лимфоидной ткани, и агаммаглобулинемией; проявляется не поддающейся лечению диареей и кахексией, имеет неблагоприятный прогноз.
· Гипофункция тимуса Проявляется в развитии иммунодефицитных заболеваний. Гипоплазия тимуса (синдром Ди-Джорджи) развивается в результате дефекта эмбрионального развития: отсутствуют тимус, наблюдаются дефекты лица, щитовидной и паращитовидной желез и другие пороки развития. Отсутствуют иммунные реакции клеточного типа. Недоразвитие тимуса наблюдается также при швейцарском типе иммунодефицита, при синдроме Луи-Бара и др.
· Гиперфункция вилочковой железы Приводит к развитию аутоиммунных заболеваний. В частности, предполагается ее вовлечение в патогенез злокачественной миастении. Выделен фактор – тимин, под влиянием которого снижается скорость проведения возбуждения в нервно-мышечных синапсах, осуществляемого с участием ацетилхолина как нейротрансмиттера. Основным механизмом этого нарушения считают активацию под влиянием избытка тимина "запрещенного" клона лимфоцитов с последующей продукцией антител против холинорецепторов и, возможно, других антигенов мышечных волокон. Гипертрофия и гиперфункция тимуса проявляется также гемолитической анемией аутоиммунной природы и другими аутоиммунными заболеваниями, в частности, диссеминированной красной волчанкой. Предполагают вовлечение нарушений функций тимуса в генез лимфолейкозов.
· Опухоли вилочковой железы – тимомы Болезни, ассоциированные с тимомами, подобны аутоиммунному полиэндокринному синдрому II типа, хотя частота специфических расстройств различна. У больных с тимомами встречаются: миастения (44% больных), аплазия красных клеток крови, гипоглобулинемия, аутоиммунное поражение щитовидной железы, недостаточность надпочечников, а также кандидозы.
ГЛАВА 9 ПАТОФИЗИОЛОГИЯ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
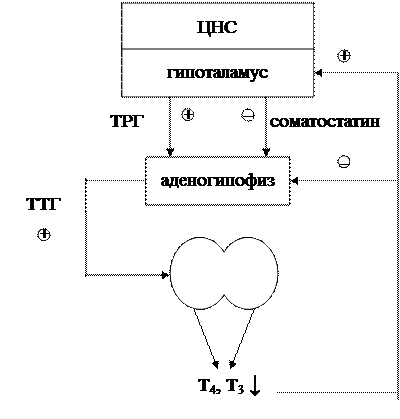
Щитовидная железа секретирует тиреоидные гормоны (Т4 – тироксин или тетрайодтиронин, Т3 – трийодтиронин) и кальцитонин. Около 90% тиреоидных гормонов секретируется в виде тироксина и 10% – в виде трийодтиронина. Большая часть тироксина в тканях превращается в трийодтиронин, который более активен (в 4 раза), чем тироксин, но содержится в крови более короткий промежуток времени. В щитовидной железе тиреоидные гормоны образуются в результате йодирования тирозина и находятся в фолликулярном коллоиде в связи с молекулой тиреоглобулина. Базальная мембрана тиреоидных клеток имеет специфическую способность перекачивать йод внутрь клеток. При выходе в кровь Т3 и Т4 соединяются с тироксин-связывающим глобулином (около 80 %) и альбумином. Вследствие высокой аффинности связывающих (транспортных) белков к тиреоидным гормонам, особенно к тироксину, гормоны освобождаются в тканях очень медленно. При поступлении в клетки оба гормона вновь связываются с внутриклеточными протеинами и образуют резерв. Они используются медленно в течение нескольких дней или недель. Эффекты Т3 развиваются в 4 раза быстрее эффектов тироксина с латентным периодом 6-12 часов и максимумом клеточной активности на 2-3 день. Почти весь тироксин дейодируется, превращаясь в трийодтиронин, который имеет более высокую аффинность к внутриклеточным рецепторам. При связывании с тиреоидным гормоном рецепторы становятся активными и инициируют процесс транскрипции с последующей трансляцией РНК на цитоплазматические рибосомы и синтезом сотен новых типов протеинов, обладающих энзиматическими и другими функциями (структурные, транспортные протеины). Активными метаболитами тиреоидных гормонов в тканях являются тетрайодпропионовая, тетрайодуксусная и трийодтироуксусная кислоты. Схема взаимодействий в гипоталамо-гипофизарно-тиреоидной системе иллюстрируется рис. 13. Как видно из рис., секреция ТТГ стимулируется ТРГ из гипоталамуса и тормозится соматостатином (в меньшей степени допамином). Гипоталамические факторы, таким образом, взаимодействуют на уровне гипофиза и определяют скорость секреции. Тиреоидные гормоны действуют на гипоталамус, чтобы стимулировать секрецию соматостатина (этот стимулирующий эффект действует как негативный сигнал на гипофиз). Эффект тиреоидных гормонов на секрецию ТРГ не определен точно. В конечном итоге в гипоталамусе T4 также превращается в T3 и это превращение может играть роль в механизме обратной связи.
Рис. 13. Схема взаимодействий в гипоталамо-гипофизарно-тиреоидной оси. Условные обозначения как на рис. 5. Основные эффекты тиреоидных гормонов Метаболическое действие Влияние тиреоидных гормонов на образование энергии – калоригенное действие. Тиреоидные гормоны усиливают метаболизм почти во всех тканях тела. Механизмы данного действия следующие. 1. Один из главных механизмов – увеличение числа и активности митохондрий → увеличение скорости образования АТФ. 2. Влияние на активный транспорт ионов через клеточные мембраны: повышение активности Na+–K+–АТФ-азы → повышение скорости транспорта ионов натрия и калия через мембраны клеток некоторых тканей → усиленный метаболизм и продукция тепла. В случае высоких концентраций тиреоидных гормонов наблюдается набухание митохондрий и разобщение окисления и фосфорилирования с уменьшением синтеза АТФ и потерей больших количеств тепла. Набухание митохондрий – следствие повышения проницаемости их мембраны, что считается ведущим механизмом токсического действия тиреоидных гормонов.
Влияние на обмен белков. В физиологических концентрациях тиреоидные гормоны стимулируют синтез белков, но в больших количествах вследствие увеличения скорости метаболизма, тиреоидные гормоны усиливают распад белка, и больные имеют отрицательный азотистый баланс. Катаболизм белков ведет к потере массы мышц и протеинов костной ткани с развитием гиперкальциемии, гиперкальциурии и остепороза.
Влияние на обмен углеводов. По влиянию на обмен углеводов тиреоидные гормоны являются диабетогенными – вызывающими гипергликемию. Механизмы развития гипергликемии: · увеличение всасывания глюкозы в кишечнике; · стимуляция гликогенолиза и глюконеогенеза; · усиление инактивации инсулина (активация инсулиназы в печени); · потенциирование гликогенолитического действия адреналина.
Влияние на жировой обмен. Тиреоидные гормоны снижают уровни холестерина в сыворотке крови. Механизмы: · увеличенное образование рецепторов к липопротеидам низкой плотности, поэтому при гипертиреозе уровень холестерина низкий или нормальный, при гипотиреозе – высокий; · мобилизация жирных кислот из жировой ткани, усиление липолитического действия гормона роста и адреналина. · Влияние на обмен витаминов. Тиреоидные гормоны необходимы для синтеза витамина А из каротина, поэтому при гипотиреозе – желтое окрашивание кожи из-за избытка каротина.
Влияние на минеральный обмен: усиливают выведение через почки натрия и калия и способствуют мобилизации внутриклеточной и внеклеточной воды. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|