|
|
Стадийность морфогенеза опухолейНа первые два вопроса о развитии опухолей de novo или стадийно отвечают две теории — скачкообразной и стадийной трансформации. Теория скачкообразной трансформации.В соответствии с этой теорией H.Ribbert, M.Borst, B.Fischer (1914) опухоль может развиться без предшествующих изменений тканей, о чем свидетельствуют данные экспериментального вирусного канцерогенеза, а также разнообразные клинические наблюдения. Теоретически возможность скачкообразного развития опухоли подтверждается существованием одноступенчатой модели вирусного канцерогенеза. В подавляющем же большинстве экспериментальных моделей опухолей речь идет о многоступенчатом развитии опухолей (см. лекцию 20 "Опухолевый рост"). Теория стадийной трансформациипри опухолевом росте была разработана отечественным онкологом-экспериментатором Л.М.Шабадом (1968), который одним из первых высказывался о решающем значении мутации соматических клеток в происхождении злокачественных опухолей. В 60-х годах, изучая экспериментальный канцерогенез в различных органах, он предложил выделять четыре стадии в морфогенезе злокачественных опухолей, три из которых относятся к предопухолевым процессам: 1) очаговая гиперплазия; 2) диффузная гиперплазия; 3) доброкачественная опухоль; 4) злокачественная опухоль. В настоящее время расшифрованы и уточнены следующие стадии морфогенеза злокачественных опухолей: ▲ стадия предопухоли — гиперплазии и предопухолевой дисплазии; ▲ стадия неинвазивной опухоли (рак на месте); а стадия инвазивного роста опухоли; ▲ стадия метастазирования. Вопрос о взаимоотношении доброкачественных и злокачественных опухолей решается неоднозначно. Бесспорно, существуют доброкачественные опухоли, которые могут трансформироваться в злокачественные. Примером могут служить аденоматозные полипы, аденомы и папилломы, в которых развиваются фокусы малигнизации и рак. Но есть также доброкачественные опухоли, практически никогда не трансформирующиеся в злокачественные аналоги. Предопухолевая дисплазия. Развитию большинства злокачественных опухолей предшествуют предопухолевые процессы, что наиболее детально изучено в группе эпителиальных опухолей и опухолей системы крови и лимфоидной ткани. В первом случае речь идет о предраке, во втором — о предлейкозе и предлимфоме. К предопухолевым процессам в настоящее время относят диспластические процессы, которые характеризуются развитием изменений как в паренхиматозных, так и стромальных элементах. Основными морфологическими критериями диспластических процессов считают появление признаков клеточного атипизма в паренхиме органа при сохранной структуре ткани. В строме очагов дисплазии регистрируются изменения состава экстрацеллюлярного матрикса, появление клеточного инфильтрата, фибробластическая реакция и др. При дисплазии эпителия обнаруживаются полиморфные эпителиальные клетки с гиперхромными ядрами и фигурами митозов не только в базальных отделах, утолщается базальная мембрана, накапливаются коллагены определенных типов и появляются лимфоидные инфильтраты. В случае предлейкоза увеличивается процент бластных клеток до 9. Помимо стереотипных проявлений дисплазии как пред опухолевого процесса, в разных органах и тканях имеются и свои специфические черты, о чем будет сказано в соответствующих лекциях в частном курсе патологической анатомии. В большинстве органов диспластический процесс развивается при наличии пролиферации клеточных элементов на фоне предшествующей гиперплазии в связи с хроническим воспалением и дисрегенерацией. Однако в ряде случаев дисплазия сочетается с атрофией ткани, как это бывает при атрофическом гастрите с перестройкой эпителия, а также при циррозе печени. Сочетание дисплазии и атрофии не случайно, так как и тот, и другой процессы имеют общие генетические механизмы, в которых участвует ряд клеточных онкогенов, ген-супрессор р53 и др. В одних ситуациях активация данных генов приводит к апоптозу и атрофии без или в сочетании с дисплазией, в других — к пролиферации также без или в сочетании с дисплазией. На стадии дисплазии методами иммуногистохимии и молекулярной биологии регистрируются перестройки в работе онкопро-теинов, факторов роста, интегриновых рецепторов и адгезивных молекул. Причем генетические перестройки могут значительно опережать морфологические изменения и служить ранними признаками предопухолевых изменений. Стадия неинвазивной опухоли. Прогрессирова-ние дисплазии связывают с дополнительными воздействиями, ведущими к последующим генетическим перестройкам и злокачественной трансформации. В результате возникает малигнизированная клетка, которая некоторое время делится, формируя узел (клон) из себе подобных клеток, питаясь за счет диффузии питательных веществ из тканевой жидкости прилежащих нормальных тканей и не прорастая в них. На данной стадии опухолевый узел не имеет еще своих сосудов. Причина этого неизвестна. Вероятно, малая масса опухоли обусловливает недостаточную продукцию факторов, стимулирующих ангиогенез и стромообразо-вание в опухоли. Однако, по нашему мнению, представляется более верной точка зрения об отсутствии в неинвазивной опухоли определенных генных перестроек, которые необходимы для осуществления инвазивного роста. В случае рака стадия роста опухоли "самой в себе" без разрушения базальной мембраны и без образования стромы и сосудов называется стадией рака на месте — cancer in situ, и выделяется в самостоятельную морфогенетическую стадию. Длительность течения данной стадии может достигать 10 лет и более. Стадия инвазивной опухоли. Она характеризуйся появлением инфильтрирующего роста. В опухоли появляется развитая сосудистая сеть, строма, выраженная в различной степени, границы с прилежащей неопухолевой тканью отсутству-1От за счет прорастания в нее опухолевых клеток. Инвазия опухоли протекает в три фазы и обеспечивается определенными генетическими перестройками. Первая фаза инвазии опухоли характеризуется ослаблением контактов между клетками, о чем свидетельствуют уменьшение количества меж. клеточных контактов, снижение концентрации некоторых адгезивных молекул из семейства CD44 и др. и, наоборот, усиления экспрессии других, обеспечивающих мобильность опухолевых клеток и их контакт с экстрацеллюлярным матриксом. На клеточной поверхности снижается концентрация ионов кальция, что приводит к повышению отрицательного заряда опухолевых клеток. Усиливается экспрессия интегриновых рецепторов, обеспечивающих прикрепление клетки к компонентам экстрацеллюлярного матрикса — ламинину, фибронектину, коллагенам. Во второй фазе опухолевая клетка секретирует протеолитические ферменты и их активаторы, которые обеспечивают деградацию экстрацеллюлярного матрикса, освобождая тем самым опухоли путь для инвазии. В то же время продукты деградации фибронектина и ламинина являются хемоаттрактантами для опухолевых клеток, которые мигрируют в зону деградации в третьей фазе инвазии, а затем процесс повторяется снова. Стадия метастазирования. Это заключительная стадия морфогенеза опухоли, сопровождающаяся определенными гено- и фенотипическими перестройками опухоли. Процесс метастазирования связан с распространением опухолевых клеток из первичной опухоли в другие органы по лимфатическим, кровеносным сосудам, периневрально, имплантационно, что легло в основу выделения видов метастазирования. Процесс метастазирования объясняется с помощью теории метастатического каскада,в соответствии с которой опухолевая клетка претерпевает цепь (каскад) перестроек, обеспечивающих распространение в отдаленные органы. В процессе метастазирования опухолевая клетка должна обладать определенными качествами, позволяющими ей проникать в прилежащие ткани и просветы сосудов (мелких вен и лимфатических сосудов); отделяться от опухолевого пласта в ток крови (лимфы) в виде отдельных клеток или небольших групп клеток; сохранять жизнеспособность после контакта в токе крови (лимфы) со специфическими и неспецифическими факторами иммунной защиты; мигрировать в венулы (лимфатические сосуды) и прекрепляться к их эндотелию в определенных органах; осуществлять инвазию микрососудов и расти на новом месте в новом окружении. Метастатический каскад условно может быть разделен на четыре этапа: ▲ формирование метастатического опухолевого субклона; ▲ инвазия в просвет сосуда; ▲ циркуляция опухолевого эмбола в кровотоке (лимфотоке); ▲оседание на новом месте с формированием вторичной опухоли (рис. 5).
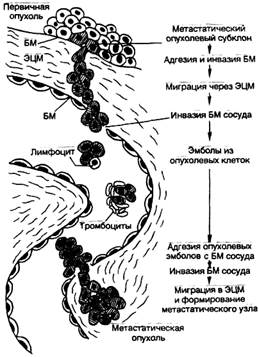
Рис. 5. Метастатический каскад [Cotran R.S., Robins L.S., 1989]. БМ — базальная мембрана; ЭЦМ — экстрацеллюлярный матрикс.
Процесс метастазирования начинается с появления метастатического субклона опухолевых клеток с измененной плазмолеммой, в результате чего клетки теряют межклеточные контакты и приобретают способность к передвижению. Затем опухолевые клетки мигрируют через экстрацеллюлярный матрикс, прикрепляясь интегриновыми рецепторами к ламинину, фибронектину, коллагеновым молекулам базальной мембраны сосуда, осуществляют ее протеолиз за счет выделения коллагеназ, катепсина, эластазы, гликозаминогидролазы, плазмина и др. Это позволяет опухолевым клеткам инвазировать базальную мембрану сосуда, прикрепляться к его эндотелию, а затем, изменяя свои адгезивные свойства (супрессия адгезивных молекул семейства САМ), отделяться как от опухолевого пласта, так и от эндотелия сосуда, "а следующем этапе формируются опухолевые эмболы, которые могут состоять только из опухолевых клеток или же из опухолевых клеток в сочетании с тромбоцитами и лимфоцитами. Фибриновое покрытие таких эмболов может защищать опухолевые клетки от элиминации клетками иммунной системы и действия неспецифических факторов защиты. На заключительном этапе опухолевые клетки взаимодействуют с эндотелием венул за счет "homing''-рецепторов и молекул семейства CD44, происходит прикрепление и протеолиз базальной мембраны, инвазия в периваскулярную ткань и рост вторичной опухоли. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|