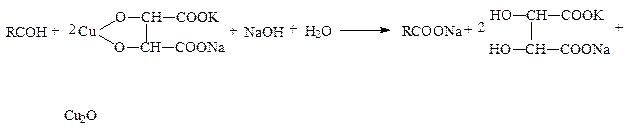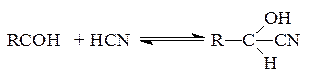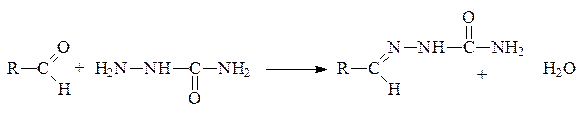|
|
Реакции карбонильной группыЛекарственные средства группы альдегидов И их производных. План: 1. Общее понятие. Номенклатура и изомерия альдегидов 2. Электронное строение альдегидной группы 3. Химические свойства альдегидов a) реакции по атому водорода альдегидной группы b) реакции по карбонильной группе альдегидов c) реакции за счет алкильного радикала 4. Лекарственные вещества производные альдегидов 5. Способы получения препаратов 6. Физико-химические свойства: описание, растворимость, физические константы 7. Реакции подлинности: общие и специфические 8. Чистота 9. Методы количественного определения 10. Хранение, применение
АЛЬДЕГИДЫ – продукты замещения в углеводородах атома водорода альдегидной группой –СОН. Альдегиды это карбонильные соединения. Общая формула альдегидов, производных от предельных углеводородов CnH2nO. Название альдегид произошло от общего способа получения альдегидов: дегидрирование спиртов. Соединение двух сокращенных латинских слов Alcohol dehydrogenatus и привело к названию альдегид. Отдельные представители называют по тем кислотам, в которые они превращаются при окислении. Так, например, первый представитель НСОН – муравьиный альдегид (или формальдегид), так как при окислении его образуется муравьиная кислота (Acidum formicum), далее CH3COH уксусный альдегид (ацетальдегид) при окислении он дает уксусную кислоту (Acidum aceticum) и т.д. По женевской номенклатуре названия альдегидов строят из названий соответствующих углеводородов, прибавляя к ним окончание «аль»: НСОН – метаналь, CH3COH – этаналь и т.д. Изомерия альдегидов обусловлена обусловлена изомерией цепи радикала.
Электронное строение альдегидной функциональной группы Электронное строение двойной связи карбонильной группы альдегидов С=О характеризуется наличием одной σ-связи и одной π-связи. Атом углерода находится в состоянии sp2-гибридизации, валентный угол около 1200 , т.е. молекула имеет плоское строение. Электронное облако π-связи расположено в плоскости, перпендикулярной плоскости, в которой расположены σ-связи атома атома углерода. Главное отличие этой двойной карбонильной связи заключается в том, что она соединяет атом углерода с электроотрицательным атомом кислорода, сильно притягивающим электроны, а поэтому эта связь сильно поляризована.
σ-связи и π-связи карбонильной группы поляризованы в разной степени: π-связь поляризована гораздо сильнее, чем σ-связь, т.е. π-электроны гораздо сильнее смещены к атому кислорода, σ-электроны (дипольный момент карбонила равен около 2,7D, т.е. он фактически в 2 раза больше дипольного момента одинарной С – О связи). Наличие в альдегидной группе сильно поляризованной двойной карбонильной связи является причиной высокой реакционной способности альдегидов. Химические свойства альдегидов Альдегиды вступают в очень большое число реакций. Эти реакции принято делить на 3 группы: 1. по атому водорода альдегидной группы, находящемуся в непосредственном соседстве с карбонилом и потому обуславливающему легкую способность альдегидов окисляться; 2. по карбонильной группе, которая обуславливает ряд реакций присоединения к карбонилу и замещения атома кислорода карбонила; 3. по радикалу, который может участвовать в реакциях, свойственных остаткам углеводородов. Реакции окисления Альдегиды очень легко окисляются – т.е. проявляют восстановительные свойства: v Аммиачным раствором оксида серебра или реактив Толлена (реакция «серебряного зеркала»)
v Реактивом Фелинга (образование красного осадка оксида меди(I)
v Реактивом Несслера
Реакции карбонильной группы А. Реакции нуклеофильного присоединения к карбонилу альдегидов 1. Присоединение водорода (гидрирование) – альдегиды превращаются в первичные спирты 2. Присоединение воды приводит к образованию гидратов
3. Присоединение спиртов приводит к образованию полуацеталей
4. Присоединение циановодорода с образованием оксинитрилов или циангидринов
5. Присоединение бисульфита натрия с образованием бисульфитных производных
6. Присоединение фуксинсернистой кислоты
7. Присоединение фенольных соединений – реакция конденсации альдегидов с фенолами. Б. Реакции замещения кислорода карбонильной группы альдегидов 1. Замещение атома кислорода на атом галогенов
2. Замещение кислорода на остаток гидроксиламина – образование оксимов
3. Замещение кислорода на остаток фенилгидразина – образование фенилгидразонов
4. Замещение кислорода остатками семикарбазида и тиосемикарбазида – образование соответственно семикарбазонов и тиосемикарбазонов

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|