|
|
Электролиз солей карбоновых кислотЭлектролиз водных растворов карбоновых кислот (анодный синтез) приводит к образованию алканов:
Первой стадией процесса является анодное окисление анионов кислот до радикалов:
На катоде образуется водород и гидроксид соответствующего металла. Реакция Кольбе применима для получения как не разветвленных так и разветвленных алканов.
Упр.4. Напишите уравнения реакций получения по способу Кольбе: (а) 2,5-диметилгексана и (б) 3,4-диметилгексана. Сочетание галогенуглеводородов (реакция Вюрца)
При взаимодействии галогеноалканов с металлическим натрием образуются алканы:
метилиодид этан При этом реакционная способность алкилгалогенидов падает в ряду: R-I > R-Br > R-Cl > R-F.
Упр. 5.Напишите уравнения реакций получения по способу Вюрца следующих алканов: (а) н-бутана, (б) н-гексана, (в) н-октана. Ответ.Для выбора исходного алкилгалогенида для получения целевого алканапо способу Вюрца его молекулу мысленно разъединяют на две части и к каждой части по месту разрыва присоединяют галоген. (a)
этилбромид бутан
Реакция Вюрца пригодна, прежде всего, для получения неразветвленных алканов с четным числом атомов углерода, т. к. при получении алканов с нечетным числом атомов углерода образуются сложные смеси продуктов:
метилиодид этилиодид пропан этан бутан
Реакции алканов
По сравнению с другими классами органических соединений алканы мало реакционноспособны. Химическая инертность алканов объясняет их название “парафины”. Причиной химической устойчивости алканов является высокая прочность не полярных σ-связей С—С и С—Н. Кроме того, связи С—С и С—Н характеризуются очень низкой поляризуемостью. В силу этого связи в алканах не проявляют склонность к гетеролитическому разрыву. На алканы не действуют концентрированные кислоты и щелочи и они не окисляются даже сильными окислителями. В то же время неполярные связи алканов способны к гомолитическому распаду. Несмотря на то, что связь С—С менее прочная, чем связь С—Н (энергия связи С—С составляет около 88 ккал/моль, а С—Н - 98 ккал/моль), последняя разрывается с большей легкостью, так как находится на поверхности молекулы и более доступна для атаки реагентом. Химические превращения алканов обычно проходят в результате гомолитического разрыва связи С—Н с последующим замещением атомов водорода другими атомами. Для алканов, таким образом, характерны реакции замещения.
Галогенирование
Метан, этан и другие алканы реагируют с фтором, хлором и бромом, но практически не реагируют с йодом. Реакцию между алканом и галогеном называют галогенированием.
А. Хлорирование метана
Практическое значение имеет хлорирование метана. Эта реакция проводится под действием освещения или при нагревании до 300оС. В результате реакции образуется смесь всех четырех возможных продуктов замещения атомов водорода на атомы хлора:
Соотношение между различными продуктами хлорирования зависит от соотношения метана и хлора. При необходимости получать метилхлорид следует брать избыток метана, а четыреххлористого углерода - хлора. Рассмотрим механизм этой реакции на примере образования метилхлорида. Под механизмом подразумевается подробное описание процесса превращения реагентов в продукты. Установлено, что хлорирование метана проходит по радикальному цепному механизму SR.
Под действием света или тепла молекула хлора распадается на два атома хлора - два свободных радикала.
Радикал хлора, взаимодействуя с молекулой метана, отщепляет от последнего атом водорода с образованием молекулы HCl и свободного радикала метила:
СН4 + Cl. ® CH3. + HCl продолжение цепи
Свободный радикал метил далее отщепляет атом хлора от молекулы хлора, в результате чего образуется молекула метилхлорида и атом хлора - новый свободный радикал: СН3. + Сl-Cl ® CH3-Cl + Cl. продолжение цепи
Атом хлора далее будет реагировать с молекулой метана и т. д. Теоретически единственный атом хлора может вызвать хлорирование бесконечного множества молекул метана, и поэтому процесс называют цепным. Цепи могут обрываться при взаимодействии радикалов друг с другом:
CH3. + CH3. ® CH3-CH3 Oбрыв цепи Cl. + Cl. ® Cl-Cl или со стенкой сосуда
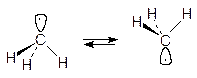
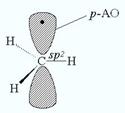
Формально свободный метильный радикал имеет тетраэдрическое строение:
Однако, вследствие малой величины барьера инверсии (переход одной формы молекулы в другую), статистически наиболее вероятным его состоянием является плоское.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
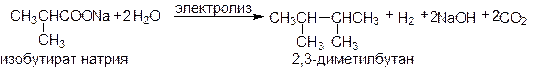


 2СH3-I + 2Na CH3-CH3 + 2NaI
2СH3-I + 2Na CH3-CH3 + 2NaI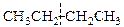

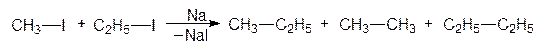
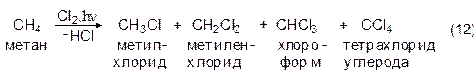
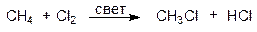
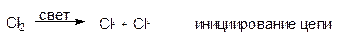
 CH3. + Cl. ® CH3-Cl
CH3. + Cl. ® CH3-Cl