|
|
Таким образом, первичным стимулом, запускающим активацию тромбоцитов, является связывание мембраны тромбоцитов с коллагеном.ФИЗИОЛОГИЯ СИСТЕМЫ КРОВИ
В обычных физиологических условиях кровь циркулирует по организму и не склонна к тромбообразованию. Почему?
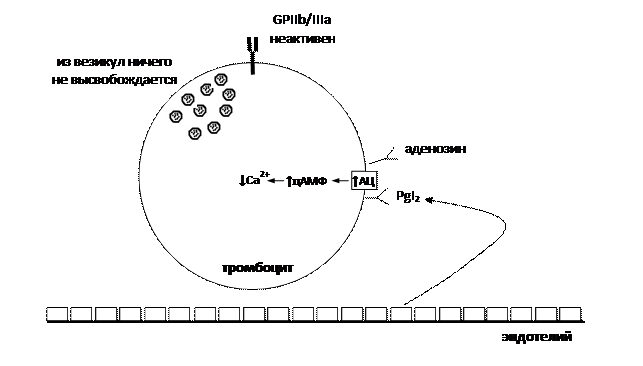
Внимание! Далее вы увидите, что выделение из везикул ряда веществ и активация гликопротеина GPIIb/IIIa имеют важное значение для агрегации тромбоцитов. Внимание! Аденилатциклаза и фосфолипаза С – это ферменты, которые расположены в клеточной мембране. Поэтому, начиная с этой распечатки, мы будем изображать их именно там (рис. 1). Кроме того, PgI2 воздействует на свои рецепторы, расположенные в стенке сосудов → ↑АЦ → ↑цАМФ → ↓Са2+ → ухудшение взаимодействия актина и миозина → расслабление мышечных клеток сосудистой стенки → расширение сосудов → затруднение образования тромбов (влияние PgI2 на сосудистую стенку на рис. 1 не показано). Аналогичным действием на тромбоциты и сосудистую стенку обладает аденозин, поскольку в перечисленных структурах он воздействует на аденозиновые рецепторы 2 типа (А2-рецепторы), которые также сопряжены с аденилатциклазой (АЦ).
Рис. 1. Физиологические механизмы, препятствующие тромбообразованию. Гемостаз
Кровь является важной частью соединительной ткани, поскольку обеспечивает поддержание обмена веществ между клетками. Потеря избыточного количества крови приводит к гибели организма. Чтобы этого не произошло, в поврежденном сосуде образуется тромб. Гемостаз протекает в два этапа: а) первичный гемостаз: спазм сосуда + агрегация тромбоцитов б) вторичный гемостаз: поддержание спазма сосуда + стабилизация тромба (образованного тромбоцитами) за счет образования нитей фибрина Давайте более подробно остановимся на каждом из видов гемостаза.
А) Первичный гемостаз (агрегация тромбоцитов)
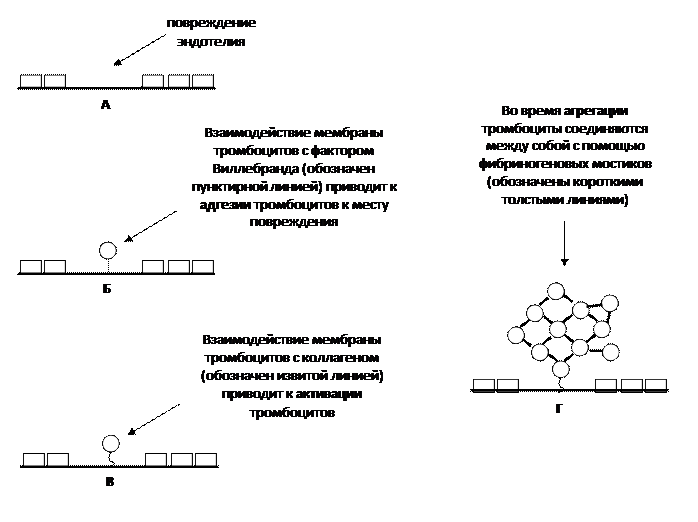
Давайте сначала посмотрим более крупным планом на те процессы, которые происходят во время первичного гемостаза. А уже затем углубимся в молекулярные взаимодействия, сопровождающие эти процессы. При повреждении эндотелия (рис. 2А) в кровь начинают быть видны молекулы гликопротеина, называемого фактором Виллебранда. Некоторое его количество находится в подэндотелиальном пространстве, некоторое количество выделяется из поврежденных эндотелиоцитов. Мембрана тромбоцитов взаимодействует с фактором Виллебранда, что обеспечивает адгезию – прилипание тромбоцитов к месту повреждения в эндотелии (рис. 2Б). Теперь мембрана тромбоцитов имеет возможность взаимодействовать с коллагеном, находящимся в месте повреждения (как вы помните их курса гистологии, коллаген находится, например, в базальной мембране) (рис. 3В). Связывание с коллагеном приводит к активации тех тромбоцитов, которые прилипли к зоне повреждения в эндотелии. А это, в свою очередь, приводит к развитию цепной реакции и активированию тех тромбоцитов, которые находятся в крови вблизи места повреждения в свободном состоянии. В результате происходит агрегация – соединение всех активированных тромбоцитов между собой с помощью фибриногеновых мостиков (рис. 2Г). В результате образуется тромб, состоящий, преимущественно, из тромбоцитов.
Внимание! Во время первичного гемостаза тромбоциты соединяются между собой именно с помощью фибриногена (не с помощью фибрина!). На рис. 2 в месте повреждения эндотелия показан один прилипший тромбоцит. В реальных условиях к месту повреждения прилипает, конечно же, несколько тромбоцитов.
Рис. 2. Взгляд крупным планом на первичный гемостаз.
Давайте теперь более детально изучим те молекулярные механизмы, которые происходят во время активации и агрегации тромбоцитов. Итак, выше мы писали, что мембрана тромбоцита связывается с коллагеном в месте повреждения эндотелия. Это служит стимулом, который а) заставляет везикулы высвобождать свое содержимое (АДФ, серотонин, тромбин и пр.) из тромбоцита в плазму крови, и б) активирует ЦОГ-1, расположенную в тромбоцитах, которая из арахидоновой кислоты образует тромбоксан ТХА2; поскольку ТХА2 является липофильной молекулой, он без особых затруднений проходит через мембрану тромбоцита и тоже оказывается в плазме крови. Важно также отметить, что из поврежденного эндотелия в плазму крови высвобождается брадикинин.
Таким образом, первичным стимулом, запускающим активацию тромбоцитов, является связывание мембраны тромбоцитов с коллагеном.
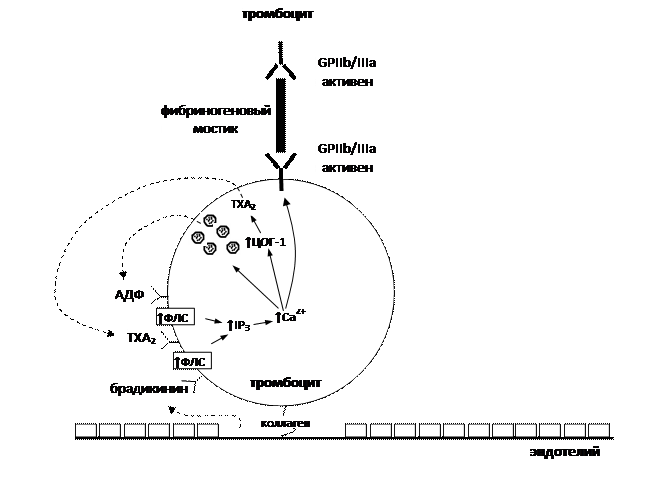
А дальше развиваются процессы, представленные на рис. 3. Молекулы АДФ, ТХА2 и брадикинина действуют на свои рецепторы, расположенные в мембране тромбоцитов. Это приводит к активации фосфолипазы С (ФЛС), которая разрушает фосфолипиды мембраны и образует из них инозитолтрифосфат (IP3). За счет того, что в цитоплазме растет концентрация IP3, увеличивается внутриклеточная концентрация ионов Са2+. Ионы Са2+ способствуют тому, что: - гликопротеин GPIIb/IIIa меняет свою конформацию и переходит в активное состояние. Теперь гликопротеин GPIIb/IIIa может соединяться с фибриногеном – ключевая реакция, необходимая для агрегации тромбоцитов. - ЦОГ-1 начинает работать еще интенсивнее, и за пределы тромбоцита выбрасывается еще большее количество ТХА2. Из везикул усиливается выброс содержащихся в них веществ – АДФ, серотонина, тромбина и пр. За счет того, что в плазме крови в районе повреждения эндотелия увеличивается содержание ТХА2 и АДФ (не стоит забывать и о брадикинине, высвобождаемом из поврежденных эндотелиоцитов), происходит вовлечение в процесс все большего количества тромбоцитов – в них тоже увеличивается концентрация ионов Са2+, что ведет к активации гликопротеина GPIIb/IIIa. В результате огромная масса тромбоцитов оказывается способной связать фибриноген, что, собственно, и приводит к агрегации тромбоцитов
Следовательно, вторичным (и главным!) стимулом, запускающим агрегацию тромбоцитов, является выделение из тех тромбоцитов, которые первыми прилипли к месту повреждения, биологически активных веществ (ТХА2 и АДФ). Вещества, выделяемые из тромбоцитов - ТХА2, АДФ, серотонин – воздействуют на свои рецепторы, расположенные в стенке сосудов → ↑ФЛС → ↑IP3 → ↑Са2+ → улучшение взаимодействия актина и миозина → сокращение мышечных клеток сосудистой стенки → сужение сосудов → облегчение образования тромбов (влияние всех перечисленных веществ на сосудистую стенку на рис. 3 не показано).
Рис. 3. Молекулярные механизмы, обеспечивающие первичный гемостаз. Б) Вторичный гемостаз (свертывание крови)
Тромб, образованный из тромбоцитов, является мягким и нестабильным. Вторичный гемостаз необходим для того, чтобы сделать тромб твердым и стабильным. Суть вторичного гемостаза (свертывания крови) сводится к тому, что поврежденный эндотелий активирует каскад реакций, в ходе которых одни факторы крови активируют другие (рис. 4). Последними реакциями данного каскада являются: - образование из протромбина (II фактор) тромбина (IIa фактор); - под влияние тромбина (IIa фактор) фибриноген (I фактор) превращается в фибрин (Ia фактор), который затем под влиянием XIIIa фактора полимеризуется в фибриновые нити, хаотично располагающиеся между тромбоцитами и охватывающие их снаружи. В таком состоянии тромб становится плотным и стабильным. Дополнительная стабилизация тромба достигается за счет того, что в мелких ячейках, образованных фибриновыми нитями, застревают другие форменные элементы крови (эритроциты и пр.). Когда мы с вами рассматривали первичный гемостаз, то говорили, что в нормальных условиях существуют факторы, препятствующие агрегации тромбоцитов – например, PgI2, аденозин. Точно также существуют факторы, которые в нормальных условиях препятствуют свертыванию крови. Например, антитромбин II, антитромбин III угнетают активность XIIa, XIa, Xa, IXa и IIа факторов свертывания крови, тем самым нарушая тромбообразование.
Внимание! Рис. 4 дан скорее для общего ознакомления, чем для тщательного запоминания. 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 Дело в том, что циклооксигеназа 1 типа (ЦОГ-1), расположенная в клетках эндотелия, образует из арахидоновой кислоты простациклин PgI2. Некоторое количество простациклина выделяется в кровь и оказывает влияние на свои рецепторы, расположенные в тромбоцитах. Это приводит к активации аденилатциклазы (АЦ), которая из АТФ образует большое количество циклического аденозинмонофосфата (цАМФ). Чем больше в цитоплазме цАМФ, тем большее количество ионов Са2+ уходит в эндоплазматический ретикулум. В результате в цитоплазме снижается концентрация ионов Са2+. В этих условиях везикулы ничего не секретируют за пределы тромбоцитов, а гликопротеин GPIIb/IIIa находится в неактивном состоянии (рис. 1).
Дело в том, что циклооксигеназа 1 типа (ЦОГ-1), расположенная в клетках эндотелия, образует из арахидоновой кислоты простациклин PgI2. Некоторое количество простациклина выделяется в кровь и оказывает влияние на свои рецепторы, расположенные в тромбоцитах. Это приводит к активации аденилатциклазы (АЦ), которая из АТФ образует большое количество циклического аденозинмонофосфата (цАМФ). Чем больше в цитоплазме цАМФ, тем большее количество ионов Са2+ уходит в эндоплазматический ретикулум. В результате в цитоплазме снижается концентрация ионов Са2+. В этих условиях везикулы ничего не секретируют за пределы тромбоцитов, а гликопротеин GPIIb/IIIa находится в неактивном состоянии (рис. 1).