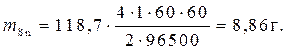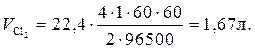|
|
Электрохимическая коррозия металлов
Коррозией металлов называют самопроизвольное разрушение металлов под действием различных окислителей из окружающей среды. В реальных условиях коррозии обычно подвергаются технические металлы, содержащие примеси других металлов и неметаллических веществ. Механизм электрохимической коррозии в таких металлах аналогичен механизму процессов, протекающих в короткозамкнутых гальванических элементах, в которых на участках с более отрицательным потенциалом идет процесс окисления (разрушение металлов), а на участках с более положительным потенциалом процесс восстановления окислителя (коррозионной среды). Наиболее часто встречаются окислители (деполяризаторы): · ионы водорода (коррозия с водородной деполяризацией) 2Н + + 2 ē = Н 2 (в кислой среде), 2Н2О + 2 ē = Н2 + 2ОН — (в нейтральной и щелочной средах); · молекулы кислорода O2 + 4 ē + 4Н + = 2Н2О (в кислой среде); О2 +4 ē + 2Н2О = 4ОН — (в щелочной и нейтральной средах). Методика рассмотрения работы гальванопары при электрохимической коррозии. · Составляют схему гальванопары: Ме1 / среда / Ме2 . · Выписывают стандартные потенциалы металлов и окислителей коррозионной среды (табл.П.7), определяют восстановитель (меньший потенциал), окислитель (больший потенциал). · Записывают уравнения процессов окисления и восстановления и суммарное уравнение окислительно-восстановительной реакции, протекающей при гальванокоррозии. · Указывают направление движения электронов. Пример 1.Гальванопара алюминий -железо в воде (среда нейтральная). В воде растворен кислород. · Схема гальванопары Al / H2O, O2 / Fe · Потенциалы
Восстановитель – Al, окислитель - О2.
4Al + 3О 2 + 6Н2О = 4Al(OH)3 · Направление движения электронов от участка с меньшим потенциалом к участку с большим потенциалом:
ē
Пример 2. Определить процессы, протекающие при коррозии луженого железа (среда – влажный воздух, содержащий кислород, пары воды и ионы Н+ ), если нарушена сплошность покрытия. · Схема гальванопары: Fe / Н2 О, О2, Н+ / Sn · Потенциалы:
Восстановитель – железо, окислитель – кислород.
2Fe + О2 + 4Н+ = 2Fe2+ + 2Н2О 2Fe + О2 + 4НCl = 2FeCl2 + 2Н2О При нарушении целостности покрытия будет разрушаться Fe. · Электроны движутся от участка с меньшим потенциалом к участку с большим потенциалом: · ē
Пример 3. Рассмотреть коррозию детали из железа и алюминия в щелочной среде (КОН), если растворенный кислород отсутствует. · Схема гальванопары: Al / КОН/ Fe · Потенциалы:
· Fe(+): 3 2 H2O + 2 ē = 2 OH — + H2 – процесс восстановления 2 Al + 2 OH — + 2H2O = 2 AlO2— + 3 H2 2 Al + 2 КOH + 2H2O = 2КAlO2 + 3 H2 Разрушается алюминий. · Направление перемещения электронов в системе: ē
Задание к подразделу 4.4
Рассмотрите коррозию гальванопары, используя потенциалы (табл. П.7), укажите анод и катод соответствующей гальванопары в различной коррозионной среде, рассчитайте ЭДС, напишите уравнения анодного и катодного процессов, молекулярное уравнение реакции коррозии, укажите направление перемещения электронов в системе.
Электролиз растворов
Электролиз – это совокупность окислительно-восстановительных процессов, происходящих при прохождении электрического тока через электрохимическую систему, состоящую из двух электродов и электролита. Электрод, на котором происходит восстановление, называется катодом, он заряжен отрицательно. Электрод, на котором происходит окисление, называется анодом, он заряжен положительно. При электролизе водных растворов могут протекать процессы, связанные с электролизом воды, т.е. растворителя.
Катодные процессы На катоде возможно восстановление: · катионов металла Ме n+ + nē = Me; · катиона водорода (свободного или в составе молекул воды): 2H + + 2ē = H 2 ( в кислой среде) ; 2H2O + 2 ē =H 2+ 2 OH — ( в нейтральной и щелочной средах). Для выбора приоритетного процесса следует сравнить стандартные электродные потенциалы металла и водорода (табл. П.6, П.7). Потенциал восстановления катионов водорода необходимо использовать с учетом перенапряжения, 1. Активные металлы (Li - Al) из-за низкой окислительной способности их ионов на катоде не осаждаются, вместо них идет восстановление ионов водорода. 2. Металлы средней активности (Mn, Zn, Fe, Sn) могут осаждаться на катоде с одновременным выделением водорода. 3. Малоактивные металлы (стоящие в ряду напряжений после водорода) из-за высокой окислительной способности их ионов осаждаются на катоде без выделения водорода. Анодные процессы На аноде возможны процессы окисления: · материала анода Ме - nē = Me n+ · молекул воды 2H2O - 4ē =О 2+ 4H + · анионов солей 2Cl — - 2ē = Cl2 NO2— - 2ē + H2O = NO3— + 2H + Анионы кислородосодержащих кислот, имеющие в своем составе атом элемента в высшей степени окисления (SO4 2—, NO3— и др.), при электролизе водных растворов на аноде не разряжаются. С учетом перенапряжения величину потенциала выделения кислорода нужно считать равной 1,8 В. Пример 1. Электролиз водного раствора сульфата калия с инертными электродами: K2SO4 = 2K + + SO42—
Так как происходит восстановление воды: 2H2O - 4ē = O2 + 4 H + 2H2O +2ē = H 2+ 2 OH — среда щелочная среда кислая
Пример 2. Электролиз водного раствора хлорида олова с инертными электродами: SnCl 2 = Sn 2+ + 2Cl —
Так как ионов олова: Sn2+ + 2 ē = S n 2Cl — - 2 ē = Cl 2 Пример 3. Электролиз сульфата меди с медным анодом: CuSO4 =Cu2+ + SO42-
Так как происходит восстановление Так как ионов меди:Cu 2+ +2ē = Cu анод растворяется: Cu - 2ē = Cu 2+
Количественные соотношения при электролизе определяют в соответствии с законами, открытыми М. Фарадеем (1834). Обобщенный закон Фарадея связывает количество вещества, образовавшегося при электролизе, со временем электролиза и силой тока:
где m - масса образовавшегося вещества , г; М - молярная масса вещества, г/ моль; n - количество электронов, участвующих в электродном процессе; I - сила тока, А; t - время электролиза, с; F - константа Фарадея (96500 Кл/моль). Для газообразных веществ, выделяющихся при электролизе, формулу использют в виде где V- объем газа, выделяющегося на электроде; V 0 - объем 1 моль газообразного вещества при нормальных условиях (22,4 л/моль).
Пример 4. Рассчитать массу олова и объем хлора при нормальных условиях, выделившихся при электролизе раствора хлорида олова с инертными электродами в течение 1 часа при силе тока 4А.
Решение.
Задание к подразделу 4.5
Рассмотрите катодные и анодные процессы при электролизе водных растворов веществ. Процессы на электродах обоснуйте значениями потенциалов (табл. П.6,7,8). Составьте схемы электролиза с инертными электродами водных растворов предложенных соединений (отдельно два раствора) с инертными электродами либо растворимым анодом. Рассчитайте массу или объем (при нормальных условиях для газов) продуктов, выделяющихся на электродах при пропускании через раствор в течение 1 часа тока силой 1 А.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 = -1,88 B;
= -1,88 B; 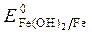 = -0,46B;
= -0,46B; = + 0,814B.
= + 0,814B. · Al(-): 4 Al - 3 ē + 3Н2О = Al(OH)3+ 3Н+ -процесс окисления;
· Al(-): 4 Al - 3 ē + 3Н2О = Al(OH)3+ 3Н+ -процесс окисления; Fe(+): 3 О2 + 4 ēē + 2Н2 О = 4ОН — -процесс восстановления
Fe(+): 3 О2 + 4 ēē + 2Н2 О = 4ОН — -процесс восстановления
 (-) Al/ Fе (+) ē
(-) Al/ Fе (+) ē О2 , Н2О
О2 , Н2О 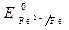 = -0,44 B;
= -0,44 B;  = -0,136 B;
= -0,136 B;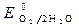 = + 1,228 B.
= + 1,228 B. ·Fe(-): 2 Fe - 2ē = Fe 2+ – процесс окисления
·Fe(-): 2 Fe - 2ē = Fe 2+ – процесс окисления Sn(+): 1 О2 + 4 ē + 4Н+ =2Н2О – процесс восстановления
Sn(+): 1 О2 + 4 ē + 4Н+ =2Н2О – процесс восстановления
 (-) Fe/ Sn (+) ē
(-) Fe/ Sn (+) ē  О2 , Н+
О2 , Н+ 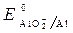 = -2,36 B;
= -2,36 B; 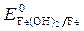 = -0,874 B;
= -0,874 B;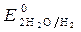 = - 0,827 B. Восстановитель -алюминий, окислитель - вода.
= - 0,827 B. Восстановитель -алюминий, окислитель - вода. Al(-): 2 Al - 3ē + 4OH — = AlO2— + 2H2O – процесс окисления
Al(-): 2 Al - 3ē + 4OH — = AlO2— + 2H2O – процесс окисления
 (-) Al/ Fe (+) ē
(-) Al/ Fe (+) ē H2O, KOH
H2O, KOH 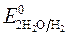 » -1 В.Все металлы по своему поведению при электролизе водных растворов можно разделить на 3 группы.
» -1 В.Все металлы по своему поведению при электролизе водных растворов можно разделить на 3 группы. (-) Kатод K+ H2O(+) Aнод SO4 2— H2O
(-) Kатод K+ H2O(+) Aнод SO4 2— H2O = - 2,92 B ;
= - 2,92 B ; 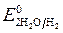 = -1 B. Сульфат-ионы не разряжаются.
= -1 B. Сульфат-ионы не разряжаются.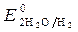 >
>  ,
, 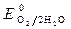 » 1,8 B.
» 1,8 B. (-) Kатод Sn 2 +, H2O(+) Aнод Cl —, H2O
(-) Kатод Sn 2 +, H2O(+) Aнод Cl —, H2O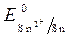 = - 0,136 B ;
= - 0,136 B ;  = -1B.
= -1B. 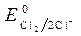 = 1,36 В ;
= 1,36 В ;  » 1,8 B.
» 1,8 B.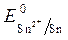 >
> 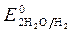 , Так как
, Так как  <
<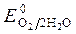 ,идет идет процесс восстановления процесс окисления ионов Сl -:
,идет идет процесс восстановления процесс окисления ионов Сl -: (-) Kатод Cu 2+ H2O (+) Aнод -Сu SO4 2— H2O
(-) Kатод Cu 2+ H2O (+) Aнод -Сu SO4 2— H2O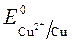 = + 0,34 B ;
= + 0,34 B ; 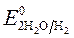 = -1 B.
= -1 B.  = + 0,34 B;
= + 0,34 B; 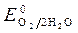 » 1,8 B.
» 1,8 B.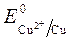 >
> 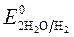 , Сульфат-ионы не разряжаются.
, Сульфат-ионы не разряжаются.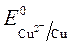 <
< ,
, ,
, ,
,