
|
|
Электролитическая диссоциация. Ионно-молекулярные уравнения
Электролитами называют вещества, растворы и расплавы которых про- водят электрический ток. К электролитам относятся неорганические кислоты, а также основания, амфотерные гидроксиды и соли. Они распадаются в водных растворах и расплавах на катионы (Кn+) и анионы (Аm-). Процесс распада молекул электролитов на ионы в среде растворителя получил название электролитической диссоциации (или ионизации). Для количественной характеристики силы электролита используют понятие степени электролитической диссоциации (ионизации) - α, которая равна отношению числа молекул, распавшихся на ионы (n), к общему числу молекул электролита, введенных в раствор (N): α = n / N. Такимобразом, α выражаютв долях единицы. По степени диссоциации электролиты условно подразделяют на сильные (α » 1) и слабые (α <0,3). Сильные электролиты
· Соли (средние, кислые, основные): А12(SO4)3, NаHCO3, СuОНСl. · Неорганические кислоты: НNO3, H2SO4, НС1, НВг, НI, НСlО4. и др. · Гидроксиды щелочных и щелочноземельных металлов: КОН, NаОН, Са(ОН)2, Ва(ОН)2 и др. Сильные электролиты диссоциируют в водном растворе практически нацело: А12(SO4)3 = 2А13++3 SO42– NаHCO3 = Nа+ +НСО3– НNО3 = H++NО3– Н2SO4 = 2Н++SО42– СuОНСl = CuOH++Cl– Ва(ОН)2 = Ва2++2ОН– Слабые электролиты · Почти все органические кислоты: CH3COOH , H2C2O4 и др.. · Некоторые неорганические кислоты: H2CO3, H2S, HCN, H2SiO3, HNO2, H2SO3 , H3PO4, HClO и др. · Гидроксиды металлов основного характера (кроме щелочных и щелочноземельных) и гидроксид аммония NH4OH. · Амфотерные гидроксиды: Al(OH)3, Zn(OH)2 , Cr(OH)3, Sn(OH)2, Pb(OH)2 и др. Для слабых электролитов диссоциация – обратимый процесс, для которого справедливы общие законы равновесия. Диссоциацию слабых электролитов характеризует константа равновесия, называемая константой диссоциации (ионизации) КД (табл.П.3): CH3COOH
Многоосновные кислоты и многокислотные основания диссоциируют ступенчато, и каждую ступень равновесного состояния характеризует своя константа диссоциации (причем Кд1 всегда больше Кд2 и т.д.), например при диссоциации H2S :1-я ступень H2S 2-я ступень HS– где [ ] ─ равновесные концентрации ионов и молекул. Диссоциация Сu(OH)2: 1-я ступень Сu(OH)2 2-я ступень Cu(OH)+ Амфотерные гидроксиды, напримерPb(OH)2 ,диссоциируют по основному типу: Pb(OH)2 PbOH+ и кислотному: H2PbO2 HPbO2– В растворах электролитов реакции протекают между ионами. Для записи ионных реакций применяют ионные уравнения. При составлении ионных уравнений реакций все слабые электролиты, газы и труднорастворимые электролиты записывают в молекулярной форме, все сильные электролиты (кроме труднорастворимых солей) в ионной форме. Примеры составления ионных уравнений реакций: · образование труднорастворимых соединений: Рb(NО3)2 + 2КI = ¯РbI2 + 2КNО3 Рb2+ +2I – = ¯РbI2 · реакции с участием слабодиссоциирующих соединений: СН3СООNa + НС1 = СН3COOH + NаС1 СН3COO – + Н+ = СН3COOH НС1 + NаОН = NаС1 + Н2O Н+ + ОН – = Н2O НС1 + NН4OН = NН4С1+ H2O Н+ + NH4OH =NH4+ + Н2O СН3COOH +NН4OН = СН3COONH4 + Н2О СН3COOH + NН4OН = CН3COO – + NH4+ + Н2O · образование газообразных веществ: Nа2СО3 + 2НС1 = 2NаС1 + СО2 + Н2О СО32–+ 2Н+ = СO2+ Н2O Пример 1. Осуществить превращения NаОН ® NаНSО3 ® Nа2SO3 . Решение.NаОН + Н2SO3 = NаНSO3 + Н2O ОН– + Н2SO3 = НSО3– +Н2О NаHSO3 +NаОН = Nа2SO3 + Н2O НSО3– + ОН – = SO32 – + Н2О Пример 2.Осуществить превращения Ni(ОН)2 ® (NiOH)2SO4 ® NiSO4. Решение. 2Ni(ОH)2 + Н2SO4 = (NiOН)2SO4 + Н2O ¯2Ni(ОН)2 + 2Н+ + SO42 – = ¯(NiОН)2SO4 + Н2O ¯(NiОН)2SO4 + Н2SO4 = 2NiSO4 + 2Н2О ¯(NiOН)2SO4 + 2Н+ = 2Ni 2+ + 2SO42– + 2Н2О Внимание! Основные соли, как правило, нерастворимы в воде, поэтому при написании ионных уравнений их не расписывают на ионы. Задания к подразделу 3.2 Задания 121-140. Напишите в молекулярной и ионной формах уравнения возможных реакций предложенных оксидов с H2O, Na2O, KOH, HNO3.
Задания 141-160. Напишите для предложенных соединений уравнения диссоциации, а также в молекулярной и ионной формах уравнения возможных реакций взаимодействия их с H2SO4 и NaOH.
Задания 161-180. Напишите уравнения диссоциации солей и назовите их.
Задания 181-200. Напишите в молекулярной и ионной формах уравнения реакций для следующих превращений. 181.Ni(OH)2 (NiOH)2SO4 NiSO4 Ni(OH)2; H3PO4 KH2PO4 182.CuSO4 (CuOH)2SO4 Cu(OH)2 CuOHNO3; NaHSO3 Na2SO3 183.Bi(NO3 )3 BiOH(NO3)2 Bi(OH)3 Bi2O3; Ca3(PO4)2 Ca3(H2PO4)2 184.Co(OH)2 CoOHCl CoCl2 Co(NO3)2; NaOH NaHSO3 185.Pb(NO3 )2 PbOHNO3 Pb(OH)2 K2PbO2; Na2Te NaHTe 186.NiCl2 Ni(OH)2 NiOHCl NiCl2; Ba(HS)2 BaS 187.CrOHCl2 CrCl3 Cr(OH)3 CrOHSO4; H2SiO3 NaHSiO3 188.(SnOH)2SO4 SnSO4 Sn(OH)2 Na2SnO2; K2SO3 KHSO3 189.NiBr2 NiOHBr Ni(OH)2 NiSO4; NaHSiO3 Na2SiO3 190.CoSO4 Co(OH)2 (CoOH)2SO4 Co(NO3)2; H2S Ca(HS)2 191.Cr2(SO4)3 CrOHSO4 Cr2(SO4)3 CrCl3; Mg3(PO4)2 MgHPO4 192.NiSO4 (NiOH)2SO4 Ni(OH)2 NiBr2; NaHCO3 Na2CO3 193.FeOHSO4 Fe2(SO4)3 Fe(OH)3 FeCl3; MgCO3 Mg(HCO3)2 194.Sn(OH)2 SnOHСl K2SnO2 Sn(OH)2; H3AsO4 KH2AsO4 195.NiBr2 Ni(OH)2 NiOHCl NiCl2; BaSO3 Ba(HSO3)2 196.Al(OH)3 Al(OH)2Cl AlCl3 Al(NO3)3; NaH2AsO3 Na3AsO3 197.CoCl2 Co(OH)2 (CoOH)2SO4 CoSO4; H2CO3 NaHCO3 198.Bi(OH)3 Bi(OH)2NO3 Bi(OH)3 Bi2O3; K2HPO4 H3PO4 199.Cu(OH)2 CuOHCl CuCl2 Cu(NO3)2; H2Se KHSe 200.CoSO4 (CoOH)2SO4 Co(OH)2 Co(NO3)2; K2SO3 KHSO3 Гидролиз солей Гидролиз солей – это процесс взаимодействия ионов соли с молекулами воды, приводящий к смещению ионного равновесия воды и изменению рН среды. Гидролиз является обратимым процессом. В реакциях гидролиза участву- ют ионы слабых электролитов: катионы слабых оснований и анионы слабых кислот. Причина гидролиза – образование слабодиссоциированных или труднорастворимых продуктов. Следствием гидролиза является нарушение равновесия в системе H2O · Соль, образованная сильным основанием и слабой кислотой, подвергается гидролизу по аниону. Реакция среды щелочная (pH > 7). Первая ступень гидролиза: Na2CO3 + HOH · Соль, образованная слабым основанием и сильной кислотой, подвергается гидролизу по катиону. Реакция среды кислая (pH < 7). Первая ступень гидролиза: Cu(NO3)2 + HOH · Соль, образованная слабым основанием и слабой кислотой, подвергается гидролизу по катиону и аниону. Характер среды определяется константами диссоциации образовавшихся слабых электролитов. CH3COONH4 + HOH CH3COO— + NH4+ + HOH · При совместном гидролизе двух солей образуются слабое основание и слабая кислота: 2FeCl3 + 3Na2S +6H2O = 2Fe(OH)3 ¯ + 3H2S + 6NaCl 2Fe3+ + 2S2— + 6H2O = 2Fe(OH)3 ¯ + 3H2S · Соль, образованная сильной кислотой и сильным основанием, гидролизу не подвергается, реакция среды нейтральная: KNO3 + HOH ¹ Ионы K+ и NO3— не образуют с водой слабодиссоциирующих продуктов (KOH и HNO3 – сильные электролиты).
Задания к подразделу 3.3
Задания 201-220. Напишите в молекулярной и ионной формах уравнения реакций гидролиза солей, укажите значения рН растворов этих солей (больше или меньше семи).
Задания 221-240. Напишите в молекулярной и ионной формах уравнения реакций совместного гидролиза предложенных солей.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 CH3COO– + H+
CH3COO– + H+
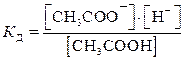
 6ּ10-8;
6ּ10-8; 1·10-14,
1·10-14,