
|
|
ФИЗИЧЕСКИЕ ОСНОВЫ ТЕРМОДИНАМИКИ12
Основные формулы · Связь между молярной (Cm) и удельной (с) теплоемкостями газа Cm=cM,где М — молярная масса газа. · Молярные теплоемкости* при постоянном объеме и постоянном давлении соответственно равны Cv=iR/2; Cp=(i+2)R/2 где i — число степеней свободы; R — молярная газовая постоянная. · Удельные теплоемкости при постоянной объеме и постоянном давлении соответственно равны
· Уравнение Майера Cр—Сv=R. · Показатель адиабаты
· Внутренняя энергия идеального газа U=N<e> или U=vCvT, где <e>—средняя кинетическая энергия молекулы; N—число молекул газа; v — количество вещества. · Работа, связанная с изменением объема газа, в общем случае вычисляется по формуле
где V1 — начальный объем газа; V2 — его конечный объем. Работа газа: а) при изобарном процессе (p=const) A=p(V2 - V1); б) при изотермическом процессе (T=const)
* Здесь и далее в целях упрощения записи в индексах обозначений молярной теплоемкости при постоянном давлении и постоянном объеме букву «m» будем опускать.
в) при адиабатном процессе
где T1 — начальная температура газа; T2 — его конечная температура. · Уравнение Пуассона (уравнение газового состояния при адиабатном процессе)
· Связь между начальным и конечным значениями параметров состояний газа при адиабатном процессе:
· Первое начало термодинамики в общем случае записывается в виде Q=DU+A, где Q – количество теплоты, сообщённое газу; DU—изменение его внутренней энергии; А — работа, совершаемая газом против внешних сил. Первое начало термодинамики: а) при изобарном процессе
б) при изохорном процессе (A=0)
в) при изотермическом процессе (DU=0)
г) при адиабатном процессе (Q=0)
· Термический коэффициент полезного действия (КПД) цикла в общем случае
где Q1—количество теплоты, полученное рабочим телом (газом) от нагревателя; Q2—количество теплоты, переданное рабочим телом охладителю. КПД цикла Карно
где T1 — температура нагревателя; T2 — температура охладителя. · Изменение энтропии
где A и B — пределы интегрирования, соответствующие начальному и конечному состояниям системы. Так как процесс равновесный, то интегрирование проводится по любому пути. · Формула Больцмана S=k×lnW, где S — энтропия системы; W — термодинамическая вероятность ее состояния; k — постоянная Больцмана. Примеры решения задач Пример 1. Вычислить удельные теплоемкости неона и водорода при постоянных объеме (сv) и давлении (cp), принимая эти газы за идеальные. Решение. Удельные теплоемкости идеальных газов выражаются формулами
Для неона (одноатомный газ) i1=3, M1=20×10-з кг/моль. Подставив в формулы (1) и (2) значения i1, M1 и R и произведя вычисления, найдем: сv1= 624 Дж/(кг×К); сp1=1,04 кДж/(кг×К). Для водорода (двухатомный газ) i2=5, M2=2×10-3 кг/моль. Вычисление по формулам (1) и (2) дает следующие значения удельных теплоемкостей водорода: сv2=10,4 кДж/(кг×K); сp2=14,6 кДж/(кг×K). Пример 2. Вычислить удельные теплоемкости сv и сp смеси неона и водорода. Массовые доли газов соответственно равны w1=0,8 и w2=0,2. Значения удельных теплоемкостей газов взять из примера 1. Решение. Удельную теплоемкость смеси при постоянном объеме сv найдем из следующих рассуждений. Теплоту, необходимую для нагревания смеси на DT, выразим двумя соотношениями: Q=сv(m1+m2)DT (1) где сv — удельная теплоемкость смеси; m1 — масса неона; m2 — масса водорода, и Q=(сv1m1+ сv2m2)DT (2) где сv1 и сv2 — удельные теплоемкости неона и водорода соответственно. Приравняв правые части выражений (1) и (2) и разделив обе части полученного равенства наDT, найдем сv(m1+m2)=сv1m1+ сv2m2, откуда
Отношения w1=m1/(m1+m2) и w1=m2/(m1+m2) выражают массовые доли соответственно неона и водорода. С учетом этих обозначений последняя формула, примет вид сv=сv1w1+ сv2w2. Подставив в эту формулу числовые значения величин, найдем сv=2,58 кДж/(кг×К). Рассуждая таким же образок, получим формулу для вычисления удельной теплоёмкости смеси при постоянном давлении: cp=сp1w1+ сp2w2 Произведя вычисления по этой формуле, найдем cp=3,73 кДж/(кг×К). Пример 3. Определить количество теплоты, поглощаемой водородом массой m=0,2 кг при нагревании его от температуры t1=0°С до температуры t2=100 °С при постоянном давлении. Найти также изменение внутренней энергии газа и совершаемую им работу. Решение. Количество теплоты Q, поглощаемое газом при изобарном нагревании, определяется по формуле Q=mcpDT, (1) где m — масса нагреваемого газа; cp — его удельная теплоемкость при постоянном давлении; DT — изменение температуры газа. Как известно,
Произведя вычисления по этой формуле, найдем Q=291 кДж. Внутренняя энергия выражается формулой
После подстановки в эту формулу числовых значений величин и вычислений получим DU=208 кДж.
Работу расширения газа определим по формуле, выражающей первое начало термодинамики: Q=DU+A, откуда A=Q - DU. Подставив значения Q и DU, найдем А =83 кДж. Пример 4. Кислород занимает объем V1=1 м3 и находится под давлением р1=200 кПа. Газ нагрели сначала при постоянном давлении до объема V2=3 м2, a затем при постоянном объеме до давления Рис 11.1 р2=500 кПа. Построить график процесса и найти: 1) изменение DU внутренней энергии газа; 2) совершенную им работу A; 3) количество теплоты Q, переданное газу. Решение. Построим график процесса (рис. 11.1). На графике точками 1, 2, 3 обозначены состояния газа, характеризуемые параметрами (р1, V1, T1), (р1, V2, T2),(р2, V2, T3). 1. Изменение внутренней энергии газа при переходе его из состояния 1 в состояние 3 выражается формулой DU=cvmDT, где cv — удельная теплоемкость газа при постоянном объеме; m — масса газа; DT — разность температур, соответствующих конечному 3и начальному 1 состояниям, т. е. DT=T3— T1. Так как где М — молярная масса газа, то
Температуры T1 и T3 выразим из уравнения Менделеева — Клапейрона (
С учетом этого равенство (1) перепишем в виде DU=(i/2)(p2V2-p1V1). Подставим сюда значения величин (учтем, что для кислорода, как двухатомного газа, i=5) и произведем вычисления: DU=3,25 МДж. 2. Полная работа, совершаемая газом, равна A=A1+A2, где A1 — работа на участке 1—2; A2 — работа на участке 2—3, На участке 1—2 давление постоянно (p=const). Работа в этом случае выражается формулой A1=p1DV=p1(V2—V1). На участке 2—3 объем газа не изменяется и, следовательно, работа газа на этом участке равна нулю (A2=0). Таким образом, A=A1=p1(V2—V1). Подставив в эту формулу значения физических величин, произведем вычисления: A=0,4 МДж
3. Согласно первому началу термодинамики, количество теплоты Q, переданное газу, равно сумме работы A, совершенной газом, и изменению DU внутренней энергии: Q=A+DU, или Q=3,65 МДж. Пример 5. Идеальный двухатомный газ, содержащий количество вещества v=l моль, находится под давлением p1=250кПа и занимает объем V1==10 л. Сначала газ изохорно нагревают до температуры T2=400 К. Далее, изотермически расширяя, доводят его до первоначального давления. После этого путем изобарного сжатия возвращают газ в начальное состояние. Определить термический КПД h цикла. Решение. Для наглядности построим сначала график цикла, который состоит из изохоры, изотермы и изобары. В координатах р, Vэтот цикл имеет вид. представленный на рис. 11.2. Характерные точки цикла обозначим 1, 2, 3. Термический КПД любого цикла определяется выражением h=(Q1 – Q2)/Q1, или h=l – Q2/Q1, (1) где Q1 — количество теплоты, полученное газом за цикл от нагревателя; Q2 — количество теплоты, отданное газом за цикл охладителю. Заметим, что разность количеств теплоты Q1 – Q2 равна работе A, совершаемой газом за цикл. Эта работа на графике в координатах р, V (рис. 11.2) изображается площадью цикла (площадь цикла заштрихована). Рабочее вещество (газ) получает количество теплоты Q1 на двух участках: Q1-2 на участке 1—2 (изохорный процесс) и Q2-3 на участке 2—3 (изотермический процесс). Таким образом, Q1=Q1-2+Q2-3. Количество теплоты, полученное газом при изохорном процессе, равно Q1-2=Cvv(T2 – T1), где Cv — молярная теплоемкость газа при постоянном объеме; v — количестве вещества. Температуру T1 начального состояния газа найдем, воспользовавшись уравнением Клапейрона — Менделеева: T1=p1V1/(vR). Подставив числовые значения и произведя вычисления, получим
Количество теплоты, полученное газом при изотермическом процессе, равно Q2-3=vRT2ln(V2/V1), где V2 — объем, занимаемый газом при температуре T2 и давлении p1 (точка 3 на графике). На участке 3—1 газ отдает количество теплоты Q2, равное Q2=Q3-1=Cpv(T2 –T1), где Cp — молярная теплоемкость газа при изобарном процессе. Подставим найденные значения Q1 и Q2 в формулу (1):
В полученном выражении заменим отношение объемов V2/V1, согласно закону Гей-Люссака, отношением температур (V2/V1=T2/T1) и выразим Cv и Cp через число степеней свободы молекулы [Cv=iR/2, Cp=(i+2)R/2]. Тогда после сокращения на v и R/2получим
Подставив значения i, T1, T2 и R и произведя вычисления, найдем
Пример 6. В цилиндре под поршнем находится водород массой m=0,02 кг при температуре T1=300K. Водород начал расширяться адиабатно, увеличив свой объем в пять раз, а затем был сжат изотермически, причем объем газа уменьшился в пять раз. Найти температуру Т2, в конце адиабатного расширения и работу А, совершенную газом. Изобразить процесс графически. Решение. Температуры и объемы газа, совершающего адиабатный процесс, связаны между собой соотношением
где g— показатель адиабаты (для водорода как двухатомного газа g=1,4). Отсюда получаем выражение для конечной температуры T2:
Подставляя числовые значения заданных величин, находим
Прологарифмируем обе части полученного выражения: lgT2=lg300+0,4(lgl - lg5)=2,477+0,4( -0,699)=2,477—0,280=2,197. Зная lgT2, по таблицам антилогарифмов находим искомое значение T2: T2=157 К. Работа A1 газа при адиабатном расширении определяется по формуле
Подставив сюда числовые значения величин, после вычисления получим
Работа A2 газа при изотермическом сжатии выражается формулой A2=RT2(m/M)ln(V2/V1). Произведя вычисления по этой формуле, найдем A2= -21 кДж. Знак минус показывает, что при сжатии газа работа совершена внешними силами. Общая работа, совершенная газом при рассмотренных процессах, А=A1+A2=29,8кДж + (-21 кДж)=8,8 кДж. График процесса приведен на рис. 11.3. Пример 7. Нагреватель тепловой машины, работающей по обратимому циклу Карно, имеет температуру t1==200°С. Определить температуру Т2, охладителя, если при получении от нагревателя количества теплоты Q1= 1 Дж машина совершает работу A=0,4 Дж? Потери на трение и теплоотдачу не учитывать.
Решение. Температуру охладителя найдем, использовав выражение для термического КПД машины, работающей по циклу Карно, h=(T1— T2)/T1. Отсюда T2= T1(1-h). (1) Термический КПД тепловой машины выражает отношение количества теплоты, которое превращено в механическою работу A, к количеству теплоты Q1, которое получено рабочим телом тепловой машины из внешней среды (от нагревателя), т. е. h=A/Q1. Подставив это выражение в формулу (1), найдем T2= T1(1-A/Q). (2) Учтя, что T1=473 К, после вычисления по формуле (2) получим T2=284 К. Пример 8. Найти изменение DS энтропии при нагревании воды массой m=100 г от температуры t1=0°C до температуры t2=100 °С и последующем превращении воды в пар той же температуры. Решение. Найдем отдельно изменение энтропии DS' при нагревании воды и изменение энтропии DS" при превращении ее в пар. Полное изменение энтропии выразится суммой DS' и DS". Как известно, изменение энтропии выражается общей формулой
При бесконечно малом изменении dT температуры нагреваемого тела затрачивается количество теплоты dQ=mcdT, где m — масса тела; с — его удельная теплоемкость. Подставив выражение dQ в равенство (1), найдем формулу для вычисления изменения энтропии при нагревании воды:
Вынесем за знак интеграла постоянные величины и произведем интегрирование, тогда получим DS'=mcln(T2/T1). После вычислений найдем DS'=132 Дж/К. При вычислении по формуле (1) изменения энтропии во время превращения воды в пар той же температуры постоянная температуpa T 'выносится за знак интеграла. Вычислив интеграл, найдем
где Q — количество теплоты, переданное при превращении нагретой воды в пар той же температуры. Подставив в равенство (2) выражение количества теплоты Q=lm, где l — удельная теплота парообразования, получим
Произведя вычисления по формуле (3), найдем DS"=605 Дж/К. Полное изменение энтропии при нагревании воды и последующем превращении ее в пар DS=DS'+DS"=737 Дж/К. Пример 9. Определить изменение DS энтропии при изотермическом расширении кислорода массой m=10 г от объема V1=25 л до объема V2=100 л. Решение. Так как процесс изотермический, то в общем выражении энтропии
Количество теплоты Q, полученное газом, найдем по первому началу термодинамики: Q=DU+A. Для изотермического процесса DU=0, следовательно, Q=A, (2) а работа А для этого процесса определяется по формуле A=(m/M)RT ln(V2/V1). (3) С учетом (2) и (3) равенство (1) примет вид DS=(m/M)R ln(V2/V1). (4) Подставив в (4) числовые значения и произведя вычисления, получим DS=(10×10-3/(32×10-3)) ×8,31 ln(100×10-3/(25×10-3)) Дж/К=3,60 Дж/К. Задачи

12 Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 ,
,  .
.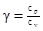 , или
, или  , или
, или  .
.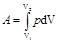 ,
, ;
; , или
, или  ,
, .
. .
.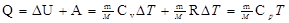
 ;
; ,
, .
.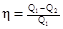 ,
, ,
,


 , следовательно, изменение внутренней энергии
, следовательно, изменение внутренней энергии .
.
 . (1)
. (1) ):
):


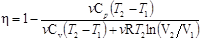
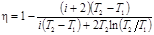 .
.
 ,
, .
. .
. .
.

 (1)
(1) .
. (2)
(2)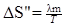 (3)
(3) температуру выносят за знак интеграла. Выполнив это, получим
температуру выносят за знак интеграла. Выполнив это, получим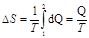 (1)
(1)