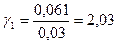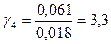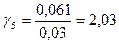|
|
Влияние некоторых факторов на эффективность действия ингибиторовНа эффективность действия ингибиторов коррозии влияют внутренние и внешние факторы коррозии металлов, причем к наиболее важным относятся кислотность коррозионной среды и концентрация ингибитора. В реальных коррозионных системах упомянутые факторы могут взаимодействовать между собой, что затрудняет выявление механизма действия ингибиторов и проектирование ингибиторной защиты. Концентрация ингибитора является важным параметром, определяющим эффективность защиты. В принципе максимальный коэффициент ингибирования должен достигаться при введении в коррозионную среду ингибитора в количестве, достаточном, чтобы покрыть поверхность металла мономолекулярным слоем. Для большинства органических ингибиторов характерно, что по мере роста их концентрации до какого-то предельного значения наблюдается увеличение защитного действия, при дальнейшем же увеличении их концентрации эффективность действия не меняется. Известны случаи, когда по мере роста концентрации ингибитора его защитное действие возрастает, достигая максимума, а затем уменьшается (например, в воде этот эффект обнаруживают полифосфаты, в серной кислоте — тиомочевина). При увеличении концентрации некоторых ненасыщенных органических соединений (например, производных ацетилена, находящихся в кислых средах) наблюдается постоянный рост защитного действия. Совсем другая зависимость между защитным действием и концентрацией ингибитора обнаруживается в случае неорганических анодных ингибиторов — пассиваторов. При малых концентрациях этих ингибиторов наблюдается рост скорости общей коррозии (ингибиторы действуют как деполяризаторы катодного процесса), и только после достижения некоторой критической концентрации наступает резкое уменьшение скорости коррозии вследствие пассивации металла. Для каждой конкретной системы оптимальную концентрацию ингибитора определяют эмпирически. Установленная в лабораторных исследованиях концентрация ингибитора может оказаться недостаточной в промышленных условиях, так как ингибитор может абсорбироваться на образующихся в работающих аппаратах продуктах коррозии, может разрушаться (например, микроорганизмами), осаждаться из раствора или испаряться. Поэтому на практике в первый момент «пуска» ингибиторной защиты вводят в коррозионную среду избыточное количество ингибиторов, а в дальнейшем контролируют их концентрацию и по мере необходимости восполняют убыль. Кислотность среды, т. е. значение рН, тоже важно учитывать — подавляющее число ингибиторов действует эффективно только при определенном значении рН. Это связано со стойкостью защитных пленок или ингибитора. Пленкообразующие (экранирующие) ингибиторы проявляют защитное действие только в таких средах, в которых возможно образование труднорастворимых осадков. Для неорганических карбонатов и фосфатов реакция среды должна быть близкой к нейтральной. Стабильность многих соединений, в частности окислителей, зависит от рН среды. Так, например, хроматы, стабильные и эффективные в нейтральных средах, в кислых восстанавливаются на поверхности металла
ускоряя катодную реакцию и, соответственно, коррозию металла. Эффективное действие в кислых средах проявляет множество органических соединений — так называемых ингибиторов травления. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ Приготовление растворов. В ходе данной лабораторной работы используют растворы с различными концентрациями. В качестве исходного раствора берут 0,25 Н HCl. В качестве ингибиторов коррозии стали в соляной кислоте выбрают тиомочевину, формальдегид и т.д. Готовят рабочие растворы на основе 0,25 Н HCl с концентрацией ингибиторов, равной 0,01; 0,1; 0,5; 1,0; 2,0 г/л. (Рабочие растворы могут быть уже готовыми). Подготовка образцов стали. В качестве исследуемого образца используют сталь-20 нарезанную в форме дисков. Диски перед каждым опытом зачищают наждачной бумагой, промывают дистиллированной водой и затем обезжиривают спиртом и взвешивают на весах с точностью до второго знака после запятой (m0). Методика эксперимента. Диски, подготовленные согласно пункту 2.2. помещают в стакан с коррозионной средой, в которую добавлен ингибитор различной концентрации. В качестве контроля используют стакан с неингибированной 0.25н HCl. Объём раствора в стакане составляет 100 - 150 мл. Длительность опыта составляет не менее 5-ти суток. После окончания испытания образцы взвешивают (m), результаты заносят в таблицу 1, рассчитывают скорость коррозии. Окончательный результат представляют графически в виде диаграммы зависимости скорости коррозии от концентрации ингибитора в растворе, отмечая на этой диаграмме точку, соответствующую скорости коррозии в чистой неингибированной кислоте согласно данным контрольного опыта. Пользуясь значением этой скорости, рассчитывают величины коэффициентов Z и γ, характеризующих эффективность действия ингибиторов.
υi - скорость коррозии в присутствии ингибитора υ - скорость коррозии в эталоне 0.25н HCl
Таблица 1.
На основании полученных данных построить график зависимости скорости коррозии от концентрации ингибитора υi=f(c). КОНТРОЛЬНЫЕ ВОПРОСЫ
ПРИМЕР РАСЧЁТОВ Таблица 1.
Вычисление: 1. Определение потери массы образца.
3. Степень эффективности ингибиторного действия. 4. Коэффициент ингибирования.
Рис. Зависимость скорости коррозии стали от концентрации ингибитора в 0,25н HCl .

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
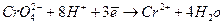







 =0,061г/сутки
=0,061г/сутки