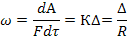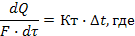|
|
Условия равновесия стационарного процесса.ЛЕКЦИЯ 1. Химическая технология – область технологии, которая изучает процессы изменения составов внутренней структуры вещества в ходе химического превращения. Наука о методах и средствах массовой химической переработки сырья, предметах потребления и средства производства. Типовые стадии химической технологии: 1. Подготовка сырья; 2. Химико-технологический процесс (ХТП); 3. Выделение целевого продукта; 4. Очистка выбросов. Все типовые стадии могут быть осуществлены за счет типовых процессов. 1 группа типовых процессов – механические (1); В результате механических процессов изменяется форма и размеры материалов без изменения химических свойств (дробление, сортировка, классификация); 2 группа типовых процессов – гидромеханические (гидростатика и гидромеханика), (3,4); Расчет основан на законах гидростатики и гидромеханики. Они включают в себя: перемещение жидкости по трубопроводам и аппаратам, гидро- и пневмотранспорт твердых материалов, разделение неоднородных смесей в системах жидкость/твердое, газ/твердое, жидкость/жидкость. 3 группа типовых процессов – тепловые (1,2,3,4); Процессы переноса тепла от одной среды к другой нагревание и охлаждение, испарение и конденсация, выпаривание, перегонка. 4 группа типовых процессов – массообменные (2,3,4); Перенос вещества из одной фазы в другую: абсорбция, десорбция, адсорбция, ректификация, дистилляция, сушка 5 группа типовых процессов– химические (2); Изменение химических свойств и внутреннего строения вещества. Теоретические основы ПАХТ. 1.Математическое описание процесса (основано на законах сохранения). Включает: · Расчет материального баланса процесса (ЗСМ), · Составление теплового баланса (ЗСЭ), · Баланс сил, · Статика и кинетика процесса. 2.Физико-химические основы · Основы термодинамики, · Основы гидродинамики и гидростатики, · Основы теплопередачи, · Основы массопередачи. 3. Принципы моделирования: · Физическое моделирование, · Математическое моделирование, · Математическое подобие процесса в маленьком процессе и большом. 4.Теория размерности. Применение основных физических законов к изучению физических процессов. I. Материальный баланс (основан на законе сохранения масс)
Хсм – концентрация твердого вещества в смеси [кг/кг], Хосв - концентрация твердого вещества в осветленной жидкости, Хос - концентрация твердого вещества в осадке. Gсм,Gосв,Gос –материальные потоки [кг/с].
Gc=Gocв+Gос 2.Баланс по компоненту (по твердому веществу): GcXc=GосвХосв+GосХос 3. Баланс по жидкости: Gc(1-Xc)=Gосв(1-Хосв)+Gос(1-Хос) 4. II. Тепловой баланс.
1.Общий тепловой баланс: Q1+Qп=Q2+Qk+Qпот Прежде чем составлять тепловой баланс процесса составляют материальный баланс. Q1=G1C1t1; Qп=DIп; I(i) - энтальпия
ЛЕКЦИЯ 2. Условия равновесия стационарного процесса. Любой процесс протекает до тех пор, пока не установится равновесие (и в химических, и в физических процессах). Физическое равновесие: dt=0
t1<t2 t1<t3<t2
dр=0 Условия равновесия характеризуют статику процесса и показывают пределы, до которых может протекать данный процесс. Отклонения системы от состояния равновесия выражает движущую силу процесса. Изучение статики необходимо для: 1. Определения предела проведения процесса; 2. Определения движущей силы процесса; 3. Определения направления процесса. Условия равновесия характеризуются равенством нулю полного дифференциала параметров системы. Для массообменных процессов dc=0 (концентрация). Кинетика процесса. Чем больше отклонение системы от равновесия, тем выше скорость процесса. Скорость процесса не одинакова на различных его стадиях, т.к. постоянно изменяется движущая сила процесса в сторону уменьшения. Изменение какой-либо величины А, характеризует результат процесса в 1 времени через 1 поверхности. С другой стороны, скорость процесса пропорциональна движущей силе. К – коэффициент скорости процесса; ∆ - средняя движущая сила процесса; R=1/К – коэффициент сопротивления процесса. 1. Скорость гидродинамического процесса:
Кг – коэффициент скорости гидродинамического процесса; ∆р – движущая сила процесса. 2. Тепловой процесс:
Кт – коэффициент теплопередачи. 3. Массообменный процесс:

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
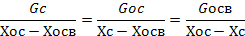
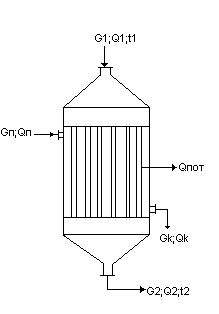 Кожухотрубчатый теплообменник.
Кожухотрубчатый теплообменник.