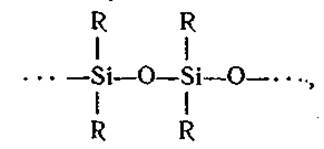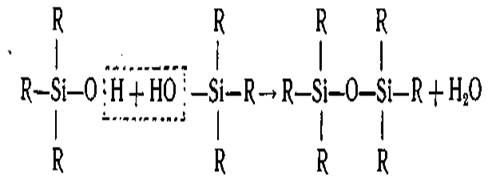|
|
Выбор состава связующего раствора на этилсиликате.СМЕСИ С ЭТИЛСИЛИКАТОМ Увеличение точности и чистоты поверхности отливок требует применения мелкозернистых наполнителей и высокой адгезионной и когезионной прочности связующих. Между чистотой поверхности отливок и зернистостью формовочного материала существует прямая зависимость: чем мельче зерна формовочного материала, тем выше чистота поверхности. Однако применение мелкозернистых материалов ограничено в связи с их плохой газопроницаемостью, которая приводит к появлению таких дефектов литья, как газовые раковины и т. д. Для обеспечения необходимой прочности связующее мелкозернистого наполнителя должно обладать достаточной адгезионной и когезионной прочностью. Из практики известно, что подобному условию отвечают необратимо твердеющие связующие с параметрами кристаллической решетки, близкими к параметрам решетки формовочного материала. В случае применения пылевидного кварца (маршаллита) используют связующие – водные растворы этилсиликата – эфира ортокремниевой кислоты – Si(OC2H5)4 (прозрачную, слегка окрашенную в желтый или бурый цвет жидкость с характерным запахом, с температурой кипения 438,5°. К при атмосферном давлении) Они образуют при твердении полисилоксаны (силиконы) или гели кремниевых кислот. Материал модели необходимо выбирать с учетом обеспечения хорошей смачиваемости связующим. Если адгезия связующего к зернам наполнителя превышает адгезию связующего к поверхности модели 0 > 90°, то связующее под действием сил поверхностного натяжения и усадки втягивается в поры между зернами наполнителя, образуя на поверхности формы различные углубления.
Этилсиликат получают в результате двухстадийной реакции этерификации и осаждения гидрата окиси кремния соляной кислотой из четыреххлористого кремния:
Они требуют повышенных температур и концентрации реагирующих веществ. Из первых двух реакций, протекающих последовательно, вторая более медленная, она и определяет длительность процесса. Реакция этерификации — реакция второго порядка. Константа скорости может быть определена по формуле:
где а и b — мольные концентрации спирта и кислоты; х — мольная концентрация образующегося эфира; τ — время от начала реакции. Значения х, τ и К определяют экспериментально. При получении эфиров из простейших спиртов К ≈ 0,25. Для увеличения выхода эфира: - повышают концентрации одного из исходных веществ (обычно спирта); - удаляют воду из зоны реакции
В конечной реакции образования этилсиликата вода не участвует, хотя ее присутствие коренным образом изменяет течение реакции. Реакция этерификации обратима: эфир взаимодействует с водой, образуя ряд полисилоксанов (силиконов):
То есть, этилсиликат состоит из ряда полисилоксанов. Схема строения молекул полисилоксанов:
где R — углеводородный радикал (этоксигруппа –OC2H5), Различают: -моноэфир Si(ОС2Н5)4 (тетраэтоксисилан):
-диэфир Si2O (ОС2Н5)6 (гексаэтоксидисилоксан)
-триэфир Si3O2 (OC2H5)8 (октаэтокситрисилоксан)
Для получения этилсиликата из четыреххлористого кремния (SiCl4) можно использовать спирт с разным содержанием воды и получать эфиры (полисилоксаны) различной сложности: - обезвоженный спирт – этилсиликат содержит 70—80% моноэфира и 20—30% полиэфиров (полисилоксанов). Такой этилсиликат называют техническим. Он содержит 28—30% SiO2 (в пересчете на окись кремния). -спирт ректификат, содержащего 4% воды, увеличивается выход полисилоксанов и содержание SiO2 – 30—37%.) -гидролизный спирт, содержащего 7—9% воды, еще более увеличивается выход полисилоксанов и SiO2 – 38-43%. Для проявления связующих свойств необходимо перевести этилсиликат в коллоидное состояние с последующим его превращением в золь путем гидролиза, при котором этоксигруппы (—ОС2Н5) частично или полностью заменяются гидроксильными группами (—ОН). Например, гидролиз моноэфира можно представить следующей схемой:
По мере замещения этоксигрупп гидроксильными состав продуктов гидролиза приближается к составу ортокремневой кислоты
Структурная схема ортокремневой кислоты в свежеприготовленном гидролизованном растворе имеет следующий вид:
В присутствии электролита (например, кислоты) молекулы ортокремневой кислоты соединяются поперечными химическими связями и образуют трехмерную сетку с выделением воды. Образуется коагуляционная структура с высокими вязкопластическими свойствами. По мере удаления воды развивается конденсированные структуры с упруго-хрупкими свойствами, и раствор переходит в гель, который после просушивания и прокаливания имеет кристаллическую структуру.
Итак, полный процесс гидролиза моноэфира с образованием золя SiO2 описывается реакциями:
Т.о., при гидролизе 1. моля моноэфира 2 молями воды образуется золь кремневой кислоты, не содержащий свободной воды. Количество воды, рассчитанное по этим реакциям, является теоретически необходимым количеством для гидролиза этилсиликата или стехиометрической нормой воды. - При гидролизе моноэфира меньшим количеством воды образуются продукты неполного гидролиза: - При гидролизе большим количеством воды образуются различные кремневые кислоты малорастворимые в воде. Их устойчивость зависит от рН среды. При рН = 5-6 распадаются с образованием геля, переходящего в золь. Одновременно с процессом гидролиза эфиров в растворе протекают процессы конденсации и полимеризации. Например, молекулы гидролизованного моноэфира частично укрупняются и
Получившийся диэфир (гексаэтоксидисилоксан) гидролизуется выделившейся при конденсации водой, в результате образуется пентаэтоксидигидросилоксан:
Это соединение может конденсироваться дальше с образованием
Тетраэфир вновь омыляется водой и полимеризуется, образуя полисилоксаны
Если гидролиз, конденсация и полимеризация протекают при комнатной температуре, образуется сетчатая структура с очень хорошими связующими свойствами:
Искусственный подогрев раствора способствует образованию линейных структур, имеющих меньшую прочность. Реакция гидролиза этилсиликата сопровождается выделением большого количества тепла и повышением температуры раствора. Регулированием температуры реакции гидролиза, например изменением количества вводимой воды, можно управлять структурой получающегося связующего — полисилоксана. Катализаторами гидролиза и полимеризации полисилоксанов являются вещества изменяющие рН раствора (соляная и серная кислоты и их соли, щелочи, аммониевые основания другие соли)
Зависимость времени гелеобразования тетракремневой кислоты от рН раствора
В качестве катализатора гидролиза широко применяют гидрат окиси аммония NH4OH. Его действие заключается в омылении этоксильных групп и перевода их в гель:
В результате полного гидролиза полисилоксанов образуется гель кремневой кислоты. Из реакций гидролиза и полимеризации полисилоксанов следует, что сложные эфиры, образующиеся в процессе получения этилсиликата с применением гидролизного спирта и спирта-ректификата, являются продуктами полимеризации моноэфира водой. Таким образом, количество воды, необходимое для гидролиза, рассчитывают по содержанию этилсиликата мономера.
Выбор состава связующего раствора на этилсиликате. Гель кремневой кислоты является связующим кремнезема. Связующие свойства геля зависят от концентрации исходных растворов и скорости коагуляции. Экспериментально установлено, что концентрация кремнезема в растворе в пересчете на SiO2 не должна превышать 18—20%, таким образом, для гидролиза необходимо применять разбавленный раствор этилсиликата. В качестве растворителей этилсиликата применяют спирт, ацетон, эфироальдегидную фракцию и др. Растворитель должен растворять как этилсиликат, так и воду, а также смачивать материал модели. В случае применения в качестве растворителя спирта оболочки получаются максимальной прочности. Неплохие результаты получают при замене органических растворителей водой. Этилсиликат и вода взаимно нерастворимы. При смешении они расслаиваются, и реакция гидролиза идет только на поверхности раздела фаз. Изменением интенсивности перемешивания раствора можно регулировать величину поверхности раздела, а тем самым и скорость реакции. Получающийся в результате реакции спирт способствует хотя и ограниченной, но взаимной растворимости воды и этилсиликата с образованием коллоидной системы. Количество воды, необходимое для гидролиза, определяется технологическим процессом приготовления оболочковых форм на этилсиликате. Применение до 1 моля воды на 1 моль моноэфира недостаточно для полного гидролиза этилсиликата. В связи с тем, что реакция этерификации обратима, оболочки, изготовленные на таком растворе, не высыхают на воздухе и способны набухать при смачивании их связующим раствором или растворителем в процессе нанесения последующих слоев. Чтобы сделать оболочки более прочными, их подвергают сушке в атмосфере влажного аммиака (в парах нашатырного спирта NH4OH). Преимущество этого метода заключается в высокой эластичности оболочек после сушки их аммиаком. При использовании для гидролиза более 2 молей воды на 1 моль моноэфира несколько снижается прочность оболочки, однако не требуется подсушка в среде влажного аммиака. В качестве катализатора при применении органических растворителей этилсиликата в раствор вводят 0,2—0,3% НСl и для водных растворов — 0,6—0,8% НС1. Количество раствора этилсиликата рассчитывают из условия получения сплошной пленки геля на поверхности зерен наполнителя.( 30—50 мкм). Для облицовочных слоев приготавливают суспензию условной вязкости 35—45 для последующих слоев 25—30 (по вискозиметру ВЗ-4 с калибровочным отверстием диаметром 4 мм). Облицовочный слой делается менее вязким с целью лучшего воспроизведения поверхности модели, последующие слои придают оболочке необходимую прочность. Практически нерационально наносить более 5 слоев. В противном случае целесообразно изготовлять оболочку целиком на этилсиликате (Шоу-процесс).
Шоу-процесс. При Шоу-процессе используют приготовленный по обычной технологии гидролизованный раствор этилсиликата, отверждение которого завершается за 10—12 ч в тонком слое и за значительно более длительное время — в толстом слое. Скорость коагуляции гидролизованного раствора этилсиликата может быть увеличена нейтрализацией двойного электрического слоя на поверхности частиц SiO2 (мицелл SiO2). Это осуществляется введением в раствор электролита коагулятора - натриевая щелочь NaOH, вводимая в виде водного раствора. После приготовления раствора им заполняют опоки или стержневые ящики, где он выдерживается до студнеобразного состояния. Коагуляция в данном случае сопровождается явлением синерезиса. В результате изменения объема раствора в нем возникают напряжения от усадки. При быстрой коагуляции напряжения не успевают снижаться за счет эластичности формы, что приводит к появлению трещин. Коагуляция и синерезис раствора, приготовленного на воздухе, ведут к появлению сравнительно небольшого числа крупных трещин. Подогрев формы приводит к образованию большого числа мелких трещин, которые незначительно снижают чистоту поверхности отливок. Нагрев формы происходит за счет сгорания спирта, выделяющегося в результате реакции гидролиза этилсиликата, а также подогрева стержней и форм газовыми горелками. После удаления растворителя и необратимого перехода геля в золь стержни и формы направляют на сборку (после охлаждения). Перед заливкой готовые формы прокаливают для окончательного удаления растворителя и влаги, так как смесь для Шоу-процесса, хоть и мало, но склонна, к набуханию. Температура прокалки определяется технологией изготовления отливки и составом заливаемого металла, но должна быть не ниже 670° К. Прочность формы для Шоу-процесса невелика и колеблется в значительном диапазоне (из-за наличия трещин): 5—20 кПа (кн/м2) в студнеобразном состоянии и 50—300 кПа после сушки. Увеличение прочности в студнеобразном состоянии для крупных стержней может быть достигнуто введением термореактивных связующих (пульвербакелита, МФ-17, МФБ и т. д.).

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|