
|
|
Фенол, его строение, химические свойства, применение.Молекулярная формула: C6H5 – OH. Строение молекулы: в молекуле фенола гидроксильная группа атомов связана с бензольным кольцом (ядром).
С другой стороны, гидроксильная группа влияет на бензольное кольцо (ядро) так, что в нем происходит перераспределение электронной плотности и атомы водорода в положениях 2,4,6 становятся более подвижными, чем в молекуле бензола. Поэтому в реакциях замещения для фенола характерно замещение трех атомов водорода в положениях 2,4,6 (в бензоле замещается только один атом водорода). Таким образом, в молекуле фенола наблюдается взаимное влияние гидроксильной группы и бензольного кольца друг на друга. Физические свойства: фенол – бесцветное кристаллическое вещество с характерным запахом, на воздухе бывает розового цвета, т.к. окисляется. Температура плавления – 42 ºC. Фенол – ядовитое вещество! При попадании на кожу вызывает ожоги! Химические свойства: хим. свойства обусловлены гидроксильной группой и бензольным кольцом (ядром). · Реакции, идущие по гидроксильной группе: Атом водорода в гидроксильной группе фенола более подвижен, чем в спиртах, поэтому фенол проявляет св-ва слабой кислоты (второе название – карболовая кислота) и взаимодействует не только с активными металлами, как спирты,но также со щелочами (спирты со щелочами не реагируют!). 2C6H5OH + 2Na → 2C6H5ONa + H2. C6H5OH + NaOH → C6H5ONa + H2O фенол гидроксид натрия фенолят натрия · Реакции, идущие по бензольному кольцу (ядру): Фенол энергично (без нагревания и катализаторов) взаимодействует с бромом и азотной кислотой, при этом в бензольном кольце замещаются три атома водорода в положениях 2,4,6.
фенол бром 2,4,6 – трибромфенол бромоводород
фенол азотная кислота 2,4,6-тринитрофенол Применение: Фенол используется для производства лекарственных веществ, красителей, веществ для дезинфекции (антисептиков), пластмасс (фенопластов), взрывчатых веществ и т.д. Получение: из каменноугольной смолы и из бензола.
Альдегиды, их строение и свойства. Получение, применение муравьиного и уксусного альдегидов. Альдегиды – органические вещества, содержащие функциональную альдегидную группу
Общая формула альдегидов: Строение молекул. В молекуле альдегида между атомами углерода и водорода существуют σ-связи, а между атомами углерода и кислорода – одна σ-связь и одна π-связь. Электронная плотность смещена от атома углерода к более электроотрицательному атому – атому кислорода. Т.о. атом углерода альдегидной группы приобретает частичный положительный (δ+), а атом кислорода – частичный отрицательный заряд (δ–). Номенклатура. Названия альдегидам даются: 1) от исторических названий соответствующих органических кислот, в которые они превращаются при окислении – муравьиный альдегид, уксусный альдегид и т.д. 2) по международной номенклатуре – от названий соответствующих углеводородов + суффикс -аль. Например, O H – C или Н – СНО муравьиный альдегид, или метаналь H O СH3 – C или СН3 – СНО уксусный альдегид, или этаналь H Физические свойства. Метаналь – бесцветный газ с резким запахом, этаналь и следующие адьдегиды – жидкости, высшие альдегиды – твердые вещества. Химические свойства. Реакции окисления. Качественные реакции на альдегиды: 1) реакция «серебряного зеркала» – окисление альдегидов аммиачным раствором оксида серебра при нагревании: CH3 – C НО + Ag2O → CH3 – CООН + 2Ag ↓ Уксусный альдегид уксусная кислота окислитель оксид серебра восстановливается до серебра, которое оседает на стенках пробирки, а альдегид окисляется в соответствующую кислоту 2) Окисление альдегидов гидроксидом меди (II) при нагревании. H – C НО + 2 Cu(OH)2 → H – CООН + 2CuOH + H2O голубой желтый муравьиный альдегид муравьиная кислота 2CuOH → Cu2O + H2O желтый красный окислителем является медь со степенью окисления +2, которая восстанавливается до меди со степенью окисления +1. Реакции присоединения. 3) Альдегиды при нагревании и в присутствии катализатора присоединяют водород за счет разрыва двойной связи в альдегидной группе. При этом альдегид восстанавливается – превращается в соответствующий спирт. Например, метаналь превращается в метанол: H– C НО + H2 → CH3 – OH метаналь метиловый спирт (метанол) Получение. Альдегиды можно получить: 1. Окислением первичных спиртов, например, 2CH3OH + O2 → 2H – C НО + 2H2O метиловый спирт муравьиный альдегид (метаналь). 2. метаналь можно также получить непосредственным окислением метана: CH4 + O2 → H – CНО + H2O 3. Уксусный альдегид можно получить гидратацией этилена в присутствии катализатора (солей ртути) – реакция М.Г. Кучерова: H – C ≡ C – H + H2O → CH3 – CНО
Применение. Наибольшее применение имеют метаналь и этаналь. · Метаналь используется для получения фенолформальдегидной смолы, из которой делают пластмассы — фенопласты. · При растворении этой смолы в ацетоне или спирте получают различные лаки. · Метаналь используется для производства некоторых лекарственных веществ и красителей. · Широко используется 40%-ный водный раствор метаналя – формалин. Он применяется при дублении кож (свертывает белок – кожа твердеет и не поддается гниению), для сохранения биологических препаратов, для дезинфекции и протравления семян. · Этаналь в основном используется для производства уксусной кислоты.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
 Ароматический радикал фенил (C6H5 –) или бензольное ядро, в отличие от радикалов предельных углеводородов обладает свойством оттягивать к себе электроны кислородного атома гидроксильной группы, поэтому в молекуле фенола химическая связь между атомами кислорода и водорода становится более полярной, а атом водорода – более подвижным, чем в молекулах спиртов, и фенол проявляет свойства слабой кислоты (его называют карболовой кислотой).
Ароматический радикал фенил (C6H5 –) или бензольное ядро, в отличие от радикалов предельных углеводородов обладает свойством оттягивать к себе электроны кислородного атома гидроксильной группы, поэтому в молекуле фенола химическая связь между атомами кислорода и водорода становится более полярной, а атом водорода – более подвижным, чем в молекулах спиртов, и фенол проявляет свойства слабой кислоты (его называют карболовой кислотой).

 , связанную с углеводородным радикалом или атомом водорода.
, связанную с углеводородным радикалом или атомом водорода.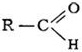 или R – CОН
или R – CОН