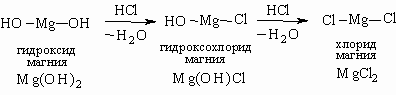|
|
Основные соли, помимо ионов металла и кислотного остатка, содержат гидроксильные группы.Соли. Названия и классификация солей. В предыдущих параграфах этой главы вы постоянно встречались с реакциями, в которых образуются соли. Солями называются вещества, в которых атомы металла связаны с кислотными остатками. Исключением являются соли аммония, в которых с кислотными остатками связаны не атомы металла, а частицы NH4+. Примеры типичных солей приведены ниже. NaCl – хлорид натрия, Na2SO4 – сульфат натрия, СаSO4 – сульфат кальция, СаCl2 – хлорид кальция, (NH4)2SO4 – сульфат аммония. Формула соли строится с учетом валентностей металла и кислотного остатка. Практически все соли – ионные соединения, поэтому можно говорить, что в солях связаны между собой ионы металла и ионы кислотных остатков: Na+Cl– – хлорид натрия Ca2+SO42– – сульфат кальция и т.д. Названия солей составляются из названия кислотного остатка и названия металла. Главным в названии является кислотный остаток. Названия солей в зависимости от кислотного остатка показаны в таблице 8-6. Таблица 8-6. Построение названий солей. В верхней части таблицы приведены кислородсодержащие кислотные остатки, в нижней – бескислородные.
Из таблицы 8-6 видно, что названия кислородсодержащих солей имеют окончания "ат", а названия бескислородных солей – окончания "ид". В некоторых случаях для кислородсодержащих солей может использоваться окончание "ит". Например, Na2SO3 – сульфит натрия. Это делается для того, чтобы различать соли серной кислоты (H2SO4) и сернистой кислоты (H2SO3) и в других таких же случаях. ** Все соли разделяются на средние, кислые и основные. Средние соли содержат только атомы металла и кислотного остатка. Например, все соли из таблицы 8-6 являются средними солями. Любую соль можно получить соответствующей реакцией нейтрализации. Например, сульфит натрия образуется в реакции между сернистой кислотой и основанием (едким натром). При этом на 1 моль кислоты требуется взять 2 моля основания:
Если взять только 1 моль основания – то есть меньше, чем требуется для полной нейтрализации, то образуется кислая соль – гидросульфит натрия:
Кислые соли образуются многоосновными кислотами. Одноосновные кислоты кислых солей не образуют. Кислые соли, помимо ионов металла и кислотного остатка, содержат ионы водорода. Названия кислых солей содержат приставку "гидро" (от слова hydrogenium – водород). Например: NaHCO3 – гидрокарбонат натрия, K2HPO4 – гидрофосфат калия, KH2PO4 – дигидрофосфат калия. Основные соли образуются при неполной нейтрализации основания. Названия основных солей образуют с помощью приставки "гидроксо". Ниже приведен пример, показывающий отличие основных солей от обычных (средних):
Основные соли, помимо ионов металла и кислотного остатка, содержат гидроксильные группы. Основные соли образуются только из многокислотных оснований. Одноокислотные основания таких солей образовать не могут. В таблице 8-6 приведены международные названия солей. Однако полезно знать также русские названия и некоторые исторически сложившиеся, традиционные названия солей, имеющих важное значение (таблица 8-7). Таблица 8-7. Международные, русские и традиционные названия некоторых важных солей.
Например, ни в коем случае нельзя путать соду Na2CO3 и питьевую соду NaHCO3. Если нечаянно использовать в пищу соду вместо питьевой соды, можно получить тяжелый химический ожог. В химии и в технике до сих пор сохраняется много старинных названий. Например, каустическая сода – вовсе не соль, а техническое название гидроксида натрия NaOH. Если обыкновенной содой можно почистить раковину или посуду, то каустическую соду ни при каких обстоятельствах брать в руки или использовать в быту нельзя! Эти простые знания могут пригодиться в жизни – мало ли с какими веществами придется столкнуться в будущем. ** Строение солей аналогично строению соответствующих кислот и оснований. Ниже приведены структурные формулы типичных средних, кислых и основных солей.
В заключение приведем строение и название основной соли, формула которой, на первый взгляд, выглядит очень сложной: [Fe(OH)2]2CO3 – дигидроксокарбонат железа (III). На самом деле, при рассмотрении структурной формулы такой соли становится ясно, что эта соль – продукт частичной нейтрализации гидроксида железа (III) угольной кислотой:
Задачи. 8.23. Закончите уравнения реакций. Определите, какие соли (средние, кислые, основные) получаются при данном мольном соотношении реагентов. Назовите эти соли. а) 2NaOH + H2SO4 = б) KOH + H2SO4 = в) 3Ca(OH)2 + 2H3PO4 = г) Ca(OH)2 + H3PO4 = д) Ca(OH)2 + HBr = е) Ca(OH)2 + 2HBr = 8.24. Напишите уравнения реакций нейтрализации, в которых получаются следующие соли: Na2CO3, NaHCO3, Na3PO4, Na2HPO4, NaH2PO4, AlCl3, Al(OH)Cl2, Al(OH)2Cl. Назовите эти соли. ** 8.25 (ФМШ). К раствору H2SO4 добавили раствор NaOH. Образовалось 3,6 г гидросульфата натрия NaHSO4 и 2,84 г сульфата натрия Na2SO4. Определите, сколько было в растворе серной кислоты и сколько прибавлено едкого натра (в граммах). ** 8.26 (ФМШ). К раствору, содержащему 1,96 г фосфорной кислоты H3PO4, прибавили раствор, содержащий 2,8 г гидроксида калия KOH. Какие соли и в каком количестве образовались в результате реакции нейтрализации?

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|