
|
|
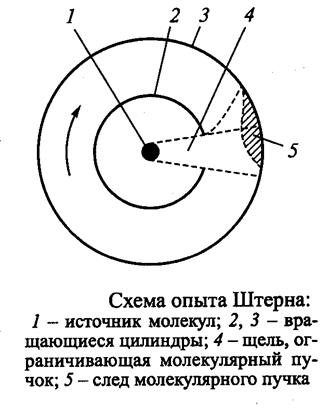
Экспериментальное подтверждение молекулярно-кинетической теории
Лекция 12 Теплоёмкость идеального газа Теплоёмкостью макросистемы (тела или некоторого количества газа) называют количество тепла, которое нужно сообщить макросистеме, чтобы повысить её температуру на один кельвин:
Молярной теплоёмкостью называют количество тепла, которое необходимо сообщить одному молю вещества, чтобы повысить его температуру на один кельвин:
В справочных таблицах обычно указывают удельную теплоёмкость с, Дж/кг.К с = С/М , где М – молярная масса.
Теплоёмкость также как и
Для анализа различных процессов в газах удобно пользоваться молярной теплоёмкостью. Особое значение имеют молярные теплоёмкости для двух процессов: при постоянном объёме СV и при постоянном давлении Ср .
При постоянном объёме dV = 0. Следовательно δА = р.dV = 0 и имеем
Так как теплоёмкость в широком интервале температур практически не меняется, то получаем
Ранее было показано, что
Молярная теплоёмкость произвольного процессa
Если процесс изобарический (p = const), то из уравнения состояния следует, что р(dV/dT) = ν.R , и соответствующая молярная теплоёмкость
Важной характеристикой газов является отношение
Для изменения внутренней энергии ν молей идеального газа получаем:
Адиабатический процесс Адиабатическим называют процесс, который проходит без теплообмена с окружающей средой. Для идеального газа получаем:
После интегрирования получаем уравнение адиабаты в переменных р , V или уравнение Пуассона:
В переменных Т, V для уравнения адиабаты получаем (используя p.V = ν.R.T):
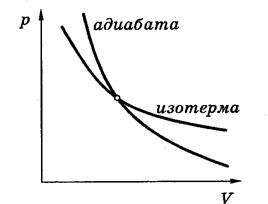
Адиабата в координатах р , V идёт круче изотермы (рV = const) Политропический процесс Политропическими называют процессы, уравнение которых в переменных р , V имеет вид
п –произвольное число, как положительное, так и отрицательное, а также равное нулю. Например, политропическими являются изохорический (V = const, п Теплоёмкость всех политропических процессов остаётся постоянной:
Для получения выражения для Сп воспользуемсяуравнением политропы в переменных Т, V:
Продифференцируем это уравнение:
Подставляя это выражение в формулу для теплоёмкости
. Используя формулу
Видно, что если п = γ,то Сп = 0 как и должно быть из определения адиабатического процесса. При п = 1 получаем Сп
Работа газа при политропических процессах
Работу газа при любом процессе можно вычислять и при помощи первого начала термодинамики:
Из формулы
В изотермическом процессе вычислять работу по этой формуле не удобно так как в этом случае
Газ Ван-дер-Ваальса С ростом давления уравнение состояния идеального газа требует корректировки при описании поведения реальных газов. При р = 1000 атм (108 Па) произведение р.V становится вдвое больше, чем предписывает модель идеального газа для конкретной температуры (газ не «сжимается»). Причин для такого отклонения две:
1) собственный размер молекул, уменьшающий объём, доступный для движения молекул (при нормальных условиях он составляет ~ 0,07% объёма сосуда с газом, а при 100 атм уже 70%);
На рисунке приведена типичная кривая зависимости потенциальной энергии взаимодействия UВЗмолекул от расстояния между их центрами. На малых расстояниях (r < ro)молекулы отталкиваются, на больших (r > ro)притягиваются.
Для описания реального (неидеального) газа пользуются уравнением Ван-дер-Ваальса:
aи b – постоянные Ван-дер-Ваальса (для разных газов они имеют свои значения). Поправка Поправка b связана с собственным объёмом молекул.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|

 .
. ,
,  Дж/моль.К.
Дж/моль.К. зависит от процесса и является функцией процесса.
зависит от процесса и является функцией процесса. .
. .
. , поэтому можно считать, что для идеального газа
, поэтому можно считать, что для идеального газа 
 .
. (соотношение Майера).
(соотношение Майера). , которое обозначают буквой γи называют постоянной адиабаты.
, которое обозначают буквой γи называют постоянной адиабаты.
 .
.
 .
. ,
, ,
, ,
, .
.
 .
.
 , где
, где ), изобарический (р = const, п = 0), изотермический (рV =const, п = 1) и адиабатический (п = γ) процессы.
), изобарический (р = const, п = 0), изотермический (рV =const, п = 1) и адиабатический (п = γ) процессы.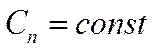 .
. .
. или
или .
. , получаем:
, получаем: .
. , получаем ещё одно выражение:
, получаем ещё одно выражение: .
.
 получаем
получаем  . Тогда работа газа в политропическом процессе:
. Тогда работа газа в политропическом процессе: .
. и А = 0/0. Поэтому в изотермическомпроцессе
и А = 0/0. Поэтому в изотермическомпроцессе .
. 2) сложный характер взаимодействия между молекулами.
2) сложный характер взаимодействия между молекулами. , где
, где обусловлена силами притяжения между молекулами. Она имеет размерность давления, и её иногда называют внутренним давлением.
обусловлена силами притяжения между молекулами. Она имеет размерность давления, и её иногда называют внутренним давлением.