
|
|
Вероятностная теория цепных реакцийВ рамках вероятностной теории скорость цепной реакции зависит от концентрации активных частиц, продолжительности жизни цепи и числа ее звеньев, вероятности обрыва цепи, вероятности разветвления цепи. С концентрацией активных частиц скорость цепной реакции связана простым уравнением:
где τ – время между двумя последовательными стадиями процесса. При постоянных температуре и исходной концентрации реагирующих веществ, и если продукты реакции полностью удаляются из реакционной зоны, скорость цепной реакции определяется изменением концентрации активных частиц:
где n – концентрация активных частиц, n0 – скорость возникновения активных частиц (n0 = const при T = const),
Если учитывать только концентрацию активных частиц, то скорость цепного неразветвленного процесса определяется уравнением:
При
если не будет происходить обрыва цепи или ее разветвления. Вероятность обрыва цепи обратно пропорциональна среднему числу звеньев цепи:
С учетом вероятности обрыва скорость цепного процесса для неразветвленной цепи:
Для разветвленных цепных реакций вероятность обрыва цепи будет меньше из-за наличия процесса разветвления цепи:
здесь δ – вероятность разветвления цепи. Скорость цепной разветвленной реакции:
При
При Горение и взрыв Горением называют химические реакции окисления, сопровождающиеся свечением и значительным выделением теплоты. Взрывом называют процесс быстрого выделения энергии, вязаного с внезапным изменением состояния вещества, в результате чего в среде образуется ударная или взрывная волна. Различают цепной и тепловой взрывы. Цепной взрыв или воспламенение Возникновение цепного воспламенения объясняется лавинообразным нарастание числа активных частик при постоянной температуре в результате протекания разветвленной цепной реакции. Цепной взрыв или воспламенение наблюдается при протекании цепных реакций с разветвленными цепями. Эти реакции характеризуются верхним и нижним пределами воспламенения, которые зависят от температуры, формы сосуда и содержания примесей в газовой смеси. Зависимость верхнего и нижнего пределов воспламенения от температуры показана на рисунке. Вне области самовоспламенения реакция течет стационарно. Ниже температуры ТА самовоспламенение не наступает ни при каких давлениях. Температуре Т’ соответствует нижний и верхний предел давления самовоспламенения.
Область самовоспламенения и стационарного течения процесса при цепной реакции Область самовоспламенения характерна для реакций с разветвленными цепями. В пределах от Рmin до Pmax будут интенсивно протекать процессы развития цепей и их разветвления. Скорость процесса растет по ех. Происходит взрыв. Если цепная реакция протекает при давлении, меньшем, чем нижний предел самовоспламенения, то цепной процесс обрывается из-за гибели активных частиц на стенках реактора. Поэтому нижняя граница взрыва зависит от состава смеси, размера реактора, и материала стенок реактора. От температуры значение нижнего предела воспламенения зависит незначительно. Если цепная реакция протекает при давлении, большем верхнего предела, то развитие цепей и их разветвление обрывается из-за роста числа столкновений с примесями. Верхний предел воспламенения зависит от температуры, природы и количества примесей. Мало зависит от формы, размера и материала реактора. Тепловой взрыв
Кривая 1 + линия 2. Если температура проведения процесса Т < TA, то скорость тепловыделения больше скорости теплоотдачи, система будет разогреваться, дойдет до точки A’, после чего начнется самопроизвольное охлаждение, т.к. скорость тепловыделения станет меньше скорости теплоотдачи. Если к системе подвести внешнее дополнительное тепло и разогреть ее до температуры, большей ТС, то скорость теплоотдачи будет меньше скорости тепловыделения и может произойти взрыв. Кривая 1 + линия 3. Здесь есть критическая ситуация в точке В, которая называется температурой воспламенения данной реакционной смеси. Кривая 1 + линия 4. Зависимости не пересекаются. Скорость тепловыделения всегда больше скорости теплоотдачи. Опасность взрыва, т.к. процесс идет с саморазогревом.

Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
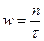 ,
,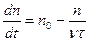 ,
,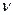 – среднее число звеньев цепи;
– среднее число звеньев цепи; 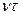 – продолжительность жизни цепи,
– продолжительность жизни цепи, ‒ скорость исчезновения активных частиц.
‒ скорость исчезновения активных частиц.
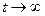 скорость цепного процесса будет стремиться к некоторому постоянному значению
скорость цепного процесса будет стремиться к некоторому постоянному значению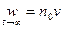 ,
,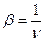

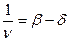
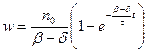
 , то
, то 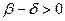 и при
и при 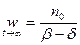
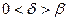 , то
, то 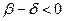 и при
и при 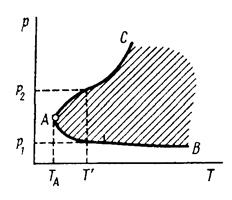
 Тепловой взрыв возникает при обычной (не цепной) экзотермической реакции, когда выделение теплоты при химической реакции становится больше теплоотдачи. При медленном протекании экзотермической химической реакции теплота отводится в окружающее пространство и температура в зоне реакции окисления лишь немного выше температуры окружающей среды. При быстром протекании теплота не успевает отводиться в окружающую среду, температура в реакционной зоне увеличивается, скорость реакции и, следовательно, скорость тепловыделения растут по ех. Происходит взрыв.
Тепловой взрыв возникает при обычной (не цепной) экзотермической реакции, когда выделение теплоты при химической реакции становится больше теплоотдачи. При медленном протекании экзотермической химической реакции теплота отводится в окружающее пространство и температура в зоне реакции окисления лишь немного выше температуры окружающей среды. При быстром протекании теплота не успевает отводиться в окружающую среду, температура в реакционной зоне увеличивается, скорость реакции и, следовательно, скорость тепловыделения растут по ех. Происходит взрыв.