
|
|
Константа равновесия и энергия изменения Гиббса.Для реакции, протекающей в изобарно-изотермических условиях, в некотором неравновесном исходном состоянии энергии Гиббса или химические потенциалы реагирующих веществ и продуктов реакции в общем случае не одинаковы, их разность (ΔGT) может быть рассчитана по уравнению:
где Это уравнение называют уравнением изотермы химической реакции. Оно позволяет рассчитать изменение энергии Гиббса при протекании процесса и определить направление протекания реакции: при при при Стандартная константа равновесия связана со стандартной энергией Гиббса реакции соотношением:
Стандартная энергия Гиббса реакции в газовой смеси — энергия Гиббса реакции при стандартных парциальных давлениях всех компонентов, равных 0,1013 МПа (1 атм). Стандартная энергия Гиббса реакции в растворе — энергия Гиббса при стандартном состоянии раствора, за которое принимают гипотетический раствор со свойствами предельно разбавленного раствора, но с концентрацией всех реагентов, равной единице. Величина стандартной энергии Гиббса реакции может быть использована для приближенной оценки термодинамической возможности протекания реакции в данном направлении, если начальные условия не сильно отличаются от стандартных. Кроме того, сравнивая величины стандартной энергии Гиббса нескольких реакций, можно выбрать наиболее предпочтительные, для которых Зависимость константы равновесия от температуры. Зависимость константы равновесия реакции от температуры может быть описана уравнением изобары химической реакции (изобары Вант-Гоффа):
и изохоры химической реакции (изохоры Вант-Гоффа):
Здесь Методы расчета константы равновесия. Расчётные методы определения константы равновесия реакции обычно сводятся к вычислению тем или иным способом стандартного изменения энергии Гиббса в ходе реакции (ΔG0), а затем использованию формулы:
При этом следует помнить, что энергия Гиббса — функция состояния системы, то есть она не зависит от пути процесса, от механизма реакции, а определяется лишь начальным и конечным состояниями системы. Следовательно, если непосредственное определение или расчёт ΔG0 для некоторой реакции по каким-либо причинам затруднены, можно подобрать такие промежуточные реакции, для которых ΔG0 известно или может быть легко определено, и суммирование которых даст рассматриваемую реакцию (см. Закон Гесса). В частности, в качестве таких промежуточных реакций часто используют реакции образования соединений из элементов. Расчетное задание Химическая Реакция:2HJ=J2+H2 Исходное вещество:2HJ; продукты реакции: H2 и J2. Справочные данные:
Расчет
ΔH°298 = ΔH°298 (H2) + ΔH°298 (J2) – ΔH°298 (HJ) = 0 + 62240 – (2· 25940) = 10360 Дж/моль
ΔS°298 = ΔS°298 (H2) + ΔS°298 (J2) – ΔS°298 (HJ) = 130,6 + 260,58 – 206,3 = -21,24 Дж/моль·К ΔG°298=ΔH°298 - TΔS°298 = 10360 – 298 · (-21,24) = 16743,16 Дж/моль Расчет Δa= 27,28 + 37,4 - 2·26,32= 12,04; Δb = (3,26 + 0,59 – 2 · 5,94)10-3 = -0,000803 = -0,803 * 10; Δ’c = (0,502 – 0,71 - 2· 0,92)105 = -204800;
ΔC°298 = ΣCpпрод – ΣCpисх= Δa + ΔbT + Δc’T-2‑ = 12,04 + 0,000803 ·298 – 204800/2982 = 9,495 Расчет
Результаты расчета
Графики зависимостей:
Расчет параметра 2HJ = H2 + J2
2(1*β)p (1- β)p (1- β)p
Kp = β2*p2/2(1- β)p = β2*p/2(1- β)= 0,0025117
При p = 1 атм и Т = 800К β =
При β= 0,9 p =
При p = 5 атм β = 
Не нашли, что искали? Воспользуйтесь поиском по сайту: ©2015 - 2026 stydopedia.ru Все материалы защищены законодательством РФ.
|
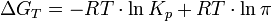
 — отношение парциальных давлений участников реакции в исходном состоянии в степенях, равных их стехиометрическим коэффициентам; R — универсальная газовая постоянная.
— отношение парциальных давлений участников реакции в исходном состоянии в степенях, равных их стехиометрическим коэффициентам; R — универсальная газовая постоянная.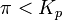
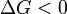 — реакция идёт в прямом направлении, слева направо;
— реакция идёт в прямом направлении, слева направо;
 — реакция достигла равновесного состояния;
— реакция достигла равновесного состояния;
 — реакция идёт в обратном направлении.
— реакция идёт в обратном направлении.
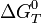 имеет наибольшую по модулю отрицательную величину.
имеет наибольшую по модулю отрицательную величину.

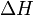 и
и  — тепловой эффект реакции, протекающей, соответственно, при постоянном давлении или при постоянном объёме. Если
— тепловой эффект реакции, протекающей, соответственно, при постоянном давлении или при постоянном объёме. Если 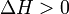 (тепловой эффект положителен, реакция эндотермическая), то температурный коэффициент константы равновесия
(тепловой эффект положителен, реакция эндотермическая), то температурный коэффициент константы равновесия 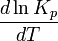 тоже положителен, то есть с ростом температуры константа равновесия эндотермической реакции увеличивается, равновесие сдвигается вправо (что вполне согласуется с принципом Ле Шателье).
тоже положителен, то есть с ростом температуры константа равновесия эндотермической реакции увеличивается, равновесие сдвигается вправо (что вполне согласуется с принципом Ле Шателье). , где
, где  — универсальная газовая постоянная.
— универсальная газовая постоянная.

 Дж/моль
Дж/моль
 Дж/(моль*К)
Дж/(моль*К)
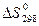 ,
, 



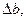
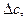
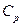 :
: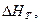
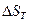 :
: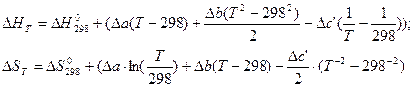
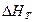






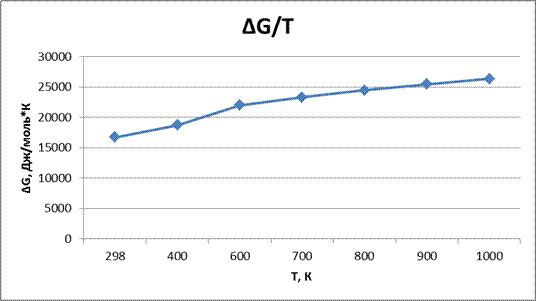
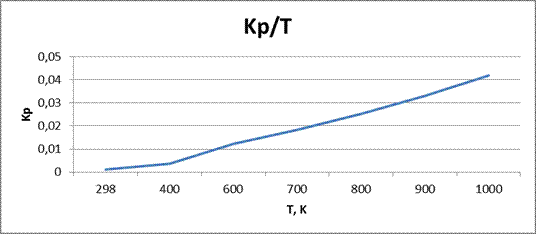
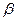 .
.